能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要___ ,形成化学键要___ 。
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g) 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;
②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是____ 。
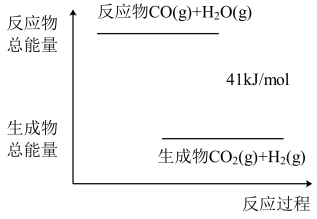
(3)已知一定条件下,CO(g)+H2O(g) CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为___ 反应(填“吸热”或“放热”)。
(4)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为_____ 。
A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
(1)从能量的角度看,断开化学键要
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g)
 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是
(3)已知一定条件下,CO(g)+H2O(g)
 CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
(4)已知热化学方程式:SO2(g)+
 O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
更新时间:2020-11-24 08:58:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】空气污染问题日益引起全民关注。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式____________________________
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为____________________________ 、 ______________________________
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为___________________________
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式___________________________
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。
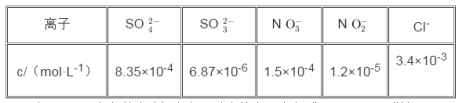
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_____________________________ 。增加压强,NO的转化率_______ (填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________ (填“提高”、“不变”或“减小”)。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。

①写出NaClO2溶液脱硝过程中主要反应的离子方程式
②随着吸收反应的进行,吸收剂溶液的pH逐渐
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂H2O2。当它们混合发生反应时,立即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol肼与足量H2O2反应,生成水蒸气和氮气,放出256.625 kJ的热量。
(1)该反应的热化学方程式为:_________________ 。
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是_________________ 。
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:_________________ 。
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:_________________ 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=_________ 。
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1______ ΔH2。(填“>”“<”或“=”)
(1)该反应的热化学方程式为:
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学反应的过程,既是物质的转化过程,也是化学能与热、电等其他形式能量的转化过程。化学反应所提供的能量大促进了社会的发展,所以与研究化学反应中的物质变化一样,研究化学反应中的能量变化同样具有重要意义。
(1)某化学兴趣小组利用反应Zn+2FeCl3=ZnCl2+2FeCl2,设计了如图所示的原电池装置。
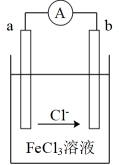
①b电极为_______ 极(填“正”或“负”)。
②a电极反应式为_______ ,发生_______ (填“氧化”或“还原”)反应。
③若电路中有0.4mol电子通过时,溶液质量增加_______ g。
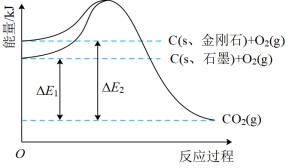
(2)如下图,在通常状况下,金刚石和石墨相比_______ (填“金刚石”或“石墨”)更稳定。石墨和金刚石之间的转化是_______ (填“物理”或“化学”)变化。
(3)已知一些化学键的键能数据如表所示:
请根据键能数据计算:CH4(g)和F2(g)反应生成CF4(g)和HF(g)的ΔH=_______ 。
(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳的排放。有一种用CO2生产甲醇燃料的方法:
已知:①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-akJ·mol-1
②CH3OH(g)=CH3OH(1) ΔH=-bkJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH=-ckJ·mol-1
④H2O(g)=H2O(1) ΔH=-dkJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
(1)某化学兴趣小组利用反应Zn+2FeCl3=ZnCl2+2FeCl2,设计了如图所示的原电池装置。

①b电极为
②a电极反应式为
③若电路中有0.4mol电子通过时,溶液质量增加
(2)如下图,在通常状况下,金刚石和石墨相比

(3)已知一些化学键的键能数据如表所示:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳的排放。有一种用CO2生产甲醇燃料的方法:
已知:①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-akJ·mol-1
②CH3OH(g)=CH3OH(1) ΔH=-bkJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH=-ckJ·mol-1
④H2O(g)=H2O(1) ΔH=-dkJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知化学反应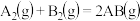 的能量变化如图所示,回答下列问题:
的能量变化如图所示,回答下列问题:
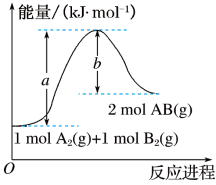
①该反应的△H_____ 0(填“大于”“小于”或“等于”)。
②反应物的总键能为_____ 。
③写出该反应的热化学方程式___________ 。
(2)已知拆开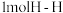 键、
键、 键、1molN≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则
键、1molN≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为 ___________ 。
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①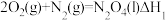
②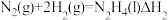
③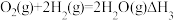
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为△H4=___________ ,联氨和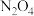 可作为火箭推进剂的主要原因为
可作为火箭推进剂的主要原因为 ____________ 。(至少答两条)
(1)已知化学反应
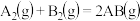 的能量变化如图所示,回答下列问题:
的能量变化如图所示,回答下列问题:
①该反应的△H
②反应物的总键能为
③写出该反应的热化学方程式
(2)已知拆开
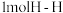 键、
键、 键、1molN≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则
键、1molN≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为 (3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①
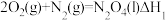
②
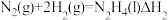
③
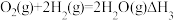
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为△H4=
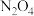 可作为火箭推进剂的主要原因为
可作为火箭推进剂的主要原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学变化过程中均存在物质变化与能量变化。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。
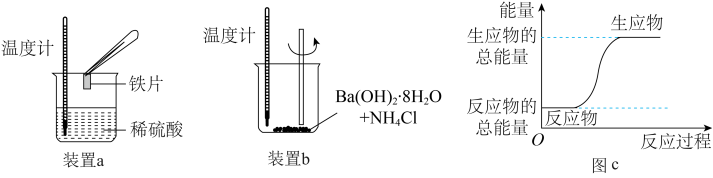
请回答下列问题:
①进行实验时,装置a中溶液变色,装置b中能闻到___________ ;装置a中温度计中水银液面变化是___________ (填“升高”或“降低”,下同);装置b中温度计中水银液面变化是___________ 。
②下列化学反应中的能量变化关系与图c相符合的是___________ 。
A.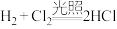
B.天然气的燃烧
C.
D.
(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)___________ kJ热量,该反应的反应物的总能量___________ (填“大于”、“等于”或“小于”)生成物的总能量。

(3)有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入2 mol/L H2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如下图所示。
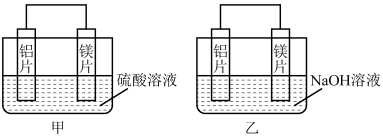
①甲池中,镁片上发生___________ (填“氧化”或“还原”)反应。
②乙池中铝片为___________ 极,写出铝电极的电极反应式:___________ 。
(1)某化学兴趣小组进行如图所示实验装置,以验证此结论。

请回答下列问题:
①进行实验时,装置a中溶液变色,装置b中能闻到
②下列化学反应中的能量变化关系与图c相符合的是
A.
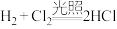
B.天然气的燃烧
C.

D.

(2)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,若反应生成2 mol NO气体(选“吸收”或“放出”)

(3)有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入2 mol/L H2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如下图所示。

①甲池中,镁片上发生
②乙池中铝片为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮的固定意义重大,氮肥的使用大面积提高了粮食产量。
(1)目前人工固氮最有效的方法是___________ (用一个化学方程式表示)。
(2)自然界发生的一个固氮反应是N2(g)+O2(g) 2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946 kJ∙mol-1、498 kJ∙mol-1、632 kJ∙mol-1,则该反应的ΔH =
2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946 kJ∙mol-1、498 kJ∙mol-1、632 kJ∙mol-1,则该反应的ΔH =___________ kJ∙mol-1.该反应在放电或极高温下才能发生,原因是___________ 。
(3)100kPa时,反应2NO(g)+O2(g) 2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)
2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)  N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。
N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。

①图1中A、B、C三点表示不同温度、压强下2NO(g)+O2(g) 2NO2(g)达到平衡时NO的转化率,则
2NO2(g)达到平衡时NO的转化率,则___________ 点对应的压强最大。
② 100kPa、25℃时,2NO2(g) N2O4(g)平衡体系中N2O4的物质的量分数为
N2O4(g)平衡体系中N2O4的物质的量分数为___________ ,N2O4的分压p(N2O4)=___________ kPa,列式计算平衡常数Kp=___________ 。(Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③ 100kPa、25℃时,VmL NO与0.5V mLO2混合后最终气体的体积为___________ mL。
(4)室温下,用注射器吸入一定量NO2气体,将针头插入胶塞密封(如图3),然后迅速将气体体积压缩为原来的一半并使活塞固定,此时手握针筒有热感,继续放置一段时间。从活塞固定时开始观察,气体颜色逐渐___________ (填“变深”或“变浅”),原因是___________ 。[已知2NO2(g)  N2O4(g)在几微秒内即可达到化学平衡]
N2O4(g)在几微秒内即可达到化学平衡]

(1)目前人工固氮最有效的方法是
(2)自然界发生的一个固氮反应是N2(g)+O2(g)
 2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946 kJ∙mol-1、498 kJ∙mol-1、632 kJ∙mol-1,则该反应的ΔH =
2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946 kJ∙mol-1、498 kJ∙mol-1、632 kJ∙mol-1,则该反应的ΔH =(3)100kPa时,反应2NO(g)+O2(g)
 2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)
2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)  N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。
N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。
①图1中A、B、C三点表示不同温度、压强下2NO(g)+O2(g)
 2NO2(g)达到平衡时NO的转化率,则
2NO2(g)达到平衡时NO的转化率,则② 100kPa、25℃时,2NO2(g)
 N2O4(g)平衡体系中N2O4的物质的量分数为
N2O4(g)平衡体系中N2O4的物质的量分数为③ 100kPa、25℃时,VmL NO与0.5V mLO2混合后最终气体的体积为
(4)室温下,用注射器吸入一定量NO2气体,将针头插入胶塞密封(如图3),然后迅速将气体体积压缩为原来的一半并使活塞固定,此时手握针筒有热感,继续放置一段时间。从活塞固定时开始观察,气体颜色逐渐
 N2O4(g)在几微秒内即可达到化学平衡]
N2O4(g)在几微秒内即可达到化学平衡]
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知下列反应的反应热数值正确,回答下列问题:
①
②
③
④
⑤
(1)上述热化学方程式中,不正确的有___________ 。(填序号,下同)
(2)上述反应中,表示燃烧热的热化学方程式是_________________________________ ;
上述反应中,表示中和热的热化学方程式是______________________ 。
已知热化学方程式: ;
;

(3)则金刚石转化为石墨的热化学方程式为___________ ,由热化学方程式可知更稳定的碳的同素异形体是___________ 。
(4)已知 ,用
,用 配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式
配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式_______________________ 。
(5)已知:

 、
、 和
和 键的键能分别为
键的键能分别为 、
、 和
和 ,则a的值为
,则a的值为________ 。
①

②

③

④

⑤

(1)上述热化学方程式中,不正确的有
(2)上述反应中,表示燃烧热的热化学方程式是
上述反应中,表示中和热的热化学方程式是
已知热化学方程式:
 ;
;
(3)则金刚石转化为石墨的热化学方程式为
(4)已知
 ,用
,用 配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式
配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式(5)已知:


 、
、 和
和 键的键能分别为
键的键能分别为 、
、 和
和 ,则a的值为
,则a的值为
您最近一年使用:0次
【推荐1】(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
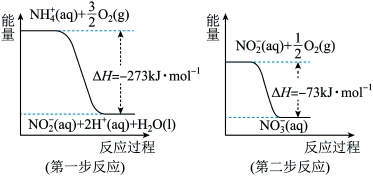
①第一步反应是______ (填“放热”或“吸热”)反应。
②1mol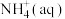 全部氧化成
全部氧化成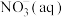 的热化学方程式是
的热化学方程式是______________________ 。
(2)已知红磷比白磷稳定,则反应①:P4(白磷,s)
 ;反应②:4P(红磷,s)
;反应②:4P(红磷,s)
 ;
; 和
和 的关系是
的关系是
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)在298K、101kPa时,已知:①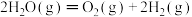
 ;
;
②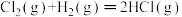

③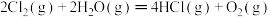

则 与
与 和
和 之间的关系正确的是
之间的关系正确的是______ (填字母代号)。
A. B.
B.
C.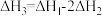 D.
D.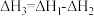
(4)已知:
①
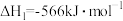
②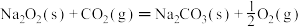

则CO(g)与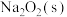 反应放出509kJ热量时,电子转移数目为
反应放出509kJ热量时,电子转移数目为______ 。
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1mol
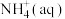 全部氧化成
全部氧化成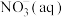 的热化学方程式是
的热化学方程式是(2)已知红磷比白磷稳定,则反应①:P4(白磷,s)

 ;反应②:4P(红磷,s)
;反应②:4P(红磷,s)
 ;
; 和
和 的关系是
的关系是
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)在298K、101kPa时,已知:①
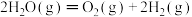
 ;
;②
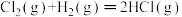

③
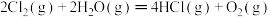

则
 与
与 和
和 之间的关系正确的是
之间的关系正确的是A.
 B.
B.
C.
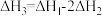 D.
D.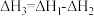
(4)已知:
①

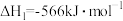
②
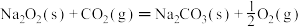

则CO(g)与
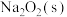 反应放出509kJ热量时,电子转移数目为
反应放出509kJ热量时,电子转移数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)已知: 、
、 燃烧热分别为
燃烧热分别为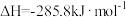 、
、 ,
,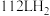 和
和 的混合气体(标准状况下)完全燃烧生成
的混合气体(标准状况下)完全燃烧生成 和液态水时放出
和液态水时放出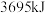 的热量,则混合气体中
的热量,则混合气体中 和
和 的物质的量之比是
的物质的量之比是___________ 。(整数比)
(2)某些共价键的键能数据如下表(单位: ):
):
把 分解为气态原子时,需要
分解为气态原子时,需要___________ (填“吸收”或“放出”)243kJ能量。由表中所列化学键形成的单质分子中,最稳定的是___________ ;
(3)发射火箭时用气态肼 作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知
作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知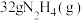 完全发生上述反应放出
完全发生上述反应放出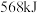 的热量,热化学方程式是:
的热量,热化学方程式是:___________ 。
(1)已知:
 、
、 燃烧热分别为
燃烧热分别为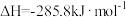 、
、 ,
,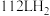 和
和 的混合气体(标准状况下)完全燃烧生成
的混合气体(标准状况下)完全燃烧生成 和液态水时放出
和液态水时放出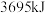 的热量,则混合气体中
的热量,则混合气体中 和
和 的物质的量之比是
的物质的量之比是(2)某些共价键的键能数据如下表(单位:
 ):
):| 共价键 |  |  |  |  |  |  |  |  |  |
| 键能 | 436 | 243 | 194 | 432 | 299 | 153 | 946 | 463 | 391 |
 分解为气态原子时,需要
分解为气态原子时,需要(3)发射火箭时用气态肼
 作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知
作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知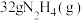 完全发生上述反应放出
完全发生上述反应放出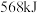 的热量,热化学方程式是:
的热量,热化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池:

Cu电极是___ (填“正”或“负”)极,其电极反应式为___ ;电子由___ 极流出。
(2)利用(1)图中的电极和电解液,在增加电源后可以实现电能转化为化学能,Fe接入电源负极,Cu接入电源正极,电解过程电极质量增加的是___ (填“Fe”或“Cu”),Fe的腐蚀速度比正常在空气中的腐蚀速度___ (填“快”或“慢”),溶液中c(Cu2+)___ (填“增大”、“减小”或“不变”)。
(3)利用氢气与氧气的燃烧反应2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1,作为燃料电池的反应原理,可以提高能量的利用率,填充H2的电极是____ (填“正”或“负”)极;当有11.2L(折算成标准状况下的体积)H2反应,会放出___ kJ热量;如果2H2(g)+O2(g)=2H2O(g) ΔH=-a kJ·mol-1,则a___ 571.6(填“>”、“<”或“=”)
(1)如图所示,组成一个原电池:

Cu电极是
(2)利用(1)图中的电极和电解液,在增加电源后可以实现电能转化为化学能,Fe接入电源负极,Cu接入电源正极,电解过程电极质量增加的是
(3)利用氢气与氧气的燃烧反应2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1,作为燃料电池的反应原理,可以提高能量的利用率,填充H2的电极是
您最近一年使用:0次


 的电子式
的电子式
 的
的


