空气污染问题日益引起全民关注。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式____________________________
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为____________________________ 、 ______________________________
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为___________________________
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式___________________________
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。
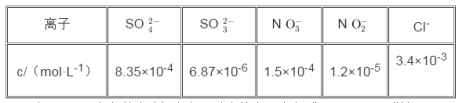
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_____________________________ 。增加压强,NO的转化率_______ (填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________ (填“提高”、“不变”或“减小”)。
(1)汽车尾气中存在大量的CO、NO、NO2和碳氢化合物,可采用铂等贵金属作为催化剂,使CO和NO转化为无毒的气体,请写出其化学方程式
(2)科研工作者研究出利用石灰乳除工业燃煤尾气中的硫 (SO2、SO3)和氮 (NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4 和Ca(NO3)2 。

①硫酸型酸雨的形成过程是大气中的SO2 溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为
②CaSO4 可以调节水泥的硬化时间。尾气中 SO2 与石灰乳反应生成CaSO4 的化学方程式为
③ Ca(NO3)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO3)2的化学方程式
(3)还可用NaClO2溶液(溶液呈碱性)作为吸收剂,对含有SO2和NOX的燃煤烟气进行脱硫、脱硝。(已知:酸性条件下,ClO2-会转化成ClO2和Cl-。ClO2是黄绿色、易溶于水的气体,具有强氧化性,能氧化SO2或NOX)在鼓泡反应期中通入含SO2和NO的烟气,反应温度为323K,NaClO2溶液的浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。

①写出NaClO2溶液脱硝过程中主要反应的离子方程式
②随着吸收反应的进行,吸收剂溶液的pH逐渐
更新时间:2018-10-30 21:56:20
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为________(填标号)。
(2)配平下列方程式:_____ 
(3)工业上可利用 制备亚氯酸钠
制备亚氯酸钠 ,反应体系中涉及下列物质:
,反应体系中涉及下列物质: 、
、 写出反应的化学方程式:
写出反应的化学方程式:________ 。
(4)某温度下将 通入
通入 溶液里,反应后得到
溶液里,反应后得到 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为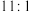 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为________ 。
(5)已知氧化性: ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:________ 。
(6)已知反应:
①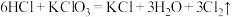
②
③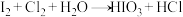 (未配平)
(未配平)
a)使用双线桥法标出反应①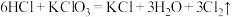 的电子转移方向和数目
的电子转移方向和数目________ 。
b)根据以上三个方程式判断,下列说法正确的是________
A.还原性由强到弱顺序:
B.氧化性由强到弱顺序: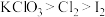
C.反应③中氧化剂和还原剂的系数之比为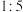
(1)亚氯酸钠
 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为________(填标号)。A.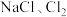 | B. |
C.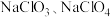 | D.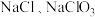 |

(3)工业上可利用
 制备亚氯酸钠
制备亚氯酸钠 ,反应体系中涉及下列物质:
,反应体系中涉及下列物质: 、
、 写出反应的化学方程式:
写出反应的化学方程式:(4)某温度下将
 通入
通入 溶液里,反应后得到
溶液里,反应后得到 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为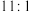 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知氧化性:
 ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:(6)已知反应:
①
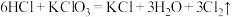
②

③
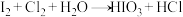 (未配平)
(未配平)a)使用双线桥法标出反应①
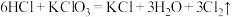 的电子转移方向和数目
的电子转移方向和数目b)根据以上三个方程式判断,下列说法正确的是
A.还原性由强到弱顺序:

B.氧化性由强到弱顺序:
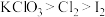
C.反应③中氧化剂和还原剂的系数之比为
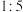
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢化铝锂(LiAlH4)是化工生产中广泛应用于药物合成的常用试剂。
(1)LiAlH4可将乙醛转化为乙醇,LiAlH4作该反应的______ 剂(选填“氧化”“还原”“催化”),用____ (填试剂名称)可检验乙醛已完全转化。
(2)配平化学反应方程式。
______ LiAlH4+______ H2SO4→______ Li2SO4+_______ Al2(SO4)3+_______ H2↑
该反应中H2SO4体现________ 性。若上述反应中电子转移数目为0.2NA个,则生成标准状况下氢气体积为_____________ 。
(3)现有两种浓度的LiOH溶液,已知a溶液的pH大于b溶液,则两种溶液中由水电离的c(H+)大小关系是:a_____ b(选填“>”、“<”或“=”)。
(4)铝和氧化铁高温下反应得到的熔融物通常为铁铝合金,设计实验证明其含金属铝。
_____________________________
(1)LiAlH4可将乙醛转化为乙醇,LiAlH4作该反应的
(2)配平化学反应方程式。
该反应中H2SO4体现
(3)现有两种浓度的LiOH溶液,已知a溶液的pH大于b溶液,则两种溶液中由水电离的c(H+)大小关系是:a
(4)铝和氧化铁高温下反应得到的熔融物通常为铁铝合金,设计实验证明其含金属铝。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)向Fe(OH)3胶体中逐滴加入氢碘酸。
现象:____________________________________________________________
离子方程式:________________________________________________
(2)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与ClO 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为_________ ;离子方程式为_________________________________ 。
(3)H2与Cl2混合点燃,充分反应后,将气体通入含有40gNaOH的溶液中恰好完全反应,则混合气体中Cl2质量为________ 。
(4)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式________________________________________________ 。
现象:
离子方程式:
(2)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与ClO
 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为(3)H2与Cl2混合点燃,充分反应后,将气体通入含有40gNaOH的溶液中恰好完全反应,则混合气体中Cl2质量为
(4)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2023年5月30日,搭载神舟十六号载人飞船的长征二号F遥十六运载火箭在酒泉卫星发射中心成功发射,标志着中国航天事业的又一重大进展。长征系列运载火箭使用偏二甲肼作燃料, 作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
(1)偏二甲肼的分子式是___________ 。
(2)有关偏二甲肼说法正确的是___________。(不定项)
(3)偏二甲肼与四氧化二氮的化学反应方程式是___________ 。
(4)偏二甲肼可用肼( )来制备,
)来制备, 的结构式是
的结构式是___________ 。
(5)肼也可作为火箭发功机的燃料,与氧化剂 反位生成氮气和水蒸气。
反位生成氮气和水蒸气。
已知①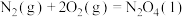
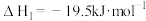
②
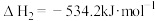
则肼和 反应的热化学方程式是
反应的热化学方程式是___________ 。
 作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。(1)偏二甲肼的分子式是
(2)有关偏二甲肼说法正确的是___________。(不定项)
A.碳原子采用 杂化 杂化 | B.分子中既有极性键又有非极性键 |
| C.偏二甲肼分子是非极性分子 | D.偏二甲肼的沸点低于异丁烷 |
(4)偏二甲肼可用肼(
 )来制备,
)来制备, 的结构式是
的结构式是(5)肼也可作为火箭发功机的燃料,与氧化剂
 反位生成氮气和水蒸气。
反位生成氮气和水蒸气。已知①
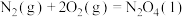
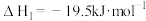
②

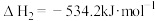
则肼和
 反应的热化学方程式是
反应的热化学方程式是
您最近一年使用:0次
【推荐2】Ⅰ.利用温室气体CO2和CH4制备燃料合成器,计算机模拟单个二氧化碳分子与甲烷分子的反应历程如图所示:

已知:leV为1电子伏特,表示一个电子(所带电量为-1.6×10-19C)经过1伏特的电位差加速后所获得的动能。
(1)制备合成气CO、H2总反应的热化学方程式为_______ 。
(2)向密闭容器,中充入等体积的CO2和CH4,测得平衡时压强对数lg p(CO2)和lg p(H2)的关系如图所示。(压强的单位为MPa)

①T1_______ T2(填“>” “<”或“=”)。
②温度为T1时,该反应的压强平衡常数Kp=_______ MPa2。
Ⅱ.丙烯是重要的有机合成原料。由丙烷制备丙烯是近年来研究的热点,主要涉及如下反应:
反应i:2C3H8(g)+O2(g)⇌2C3H6(g) +2H2O(g) kJ/mol
kJ/mol
反应ii:2C3H8(g)+7O2(g)⇌6CO(g)+8H2O(g) kJ/mol
kJ/mol
(3)在压强恒定为100 kPa条件下,按起始投料n(C3H8):n(O2)=2∶1匀速通入反应器中,在不同温度下反应相同时间,测得丙烷和氧气的转化率如下图。

①线_______ (填“L1”或“L2”)表示丙烷的转化率。
②温度高丁T1K后曲线L2随温度升高而降低的原因为_______ 。
③当温度高于T2K时,L1和L2重合的原因可能是_______ 。
Ⅲ.综合利用CO2有利于实现碳中和,在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
i.CO2(g) +H2(g)⇌CO(g)+ H2O(g) kJ·mol-1
kJ·mol-1
ii.CO(g) + 2H2(g)⇌CH3OH(g) kJ·mol-1
kJ·mol-1
iii.CO2(g) +3H2(g)⇌CH3OH(g) +H2O(g) kJ·mol-1
kJ·mol-1
(4)5MPa时,往某密闭容器中按投料比n(H2)∶n(CO2)=3∶1充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。

①图中Y代表_______ (填化学式)。
②在上图中画出反应达到平衡时,n(H2)/n(CO2)随温度变化趋势图_______ (只用画220℃以后)。

已知:leV为1电子伏特,表示一个电子(所带电量为-1.6×10-19C)经过1伏特的电位差加速后所获得的动能。
(1)制备合成气CO、H2总反应的热化学方程式为
(2)向密闭容器,中充入等体积的CO2和CH4,测得平衡时压强对数lg p(CO2)和lg p(H2)的关系如图所示。(压强的单位为MPa)

①T1
②温度为T1时,该反应的压强平衡常数Kp=
Ⅱ.丙烯是重要的有机合成原料。由丙烷制备丙烯是近年来研究的热点,主要涉及如下反应:
反应i:2C3H8(g)+O2(g)⇌2C3H6(g) +2H2O(g)
 kJ/mol
kJ/mol反应ii:2C3H8(g)+7O2(g)⇌6CO(g)+8H2O(g)
 kJ/mol
kJ/mol(3)在压强恒定为100 kPa条件下,按起始投料n(C3H8):n(O2)=2∶1匀速通入反应器中,在不同温度下反应相同时间,测得丙烷和氧气的转化率如下图。

①线
②温度高丁T1K后曲线L2随温度升高而降低的原因为
③当温度高于T2K时,L1和L2重合的原因可能是
Ⅲ.综合利用CO2有利于实现碳中和,在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
i.CO2(g) +H2(g)⇌CO(g)+ H2O(g)
 kJ·mol-1
kJ·mol-1ii.CO(g) + 2H2(g)⇌CH3OH(g)
 kJ·mol-1
kJ·mol-1iii.CO2(g) +3H2(g)⇌CH3OH(g) +H2O(g)
 kJ·mol-1
kJ·mol-1(4)5MPa时,往某密闭容器中按投料比n(H2)∶n(CO2)=3∶1充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。

①图中Y代表
②在上图中画出反应达到平衡时,n(H2)/n(CO2)随温度变化趋势图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一定温度条件下,N2与H2反应生成NH3的过程中能量变化曲线如下图。

(1)曲线_______ (填“a“或“b”")是加入催化剂时的能量变化曲线, N≡N键能为946kJ/mol,N-H键能为391kJ/mol,则H-H建能为_______ kJ/mol。
(2)水的自偶电离方程式为2H2O H3O++OH-,液氨也能发生自偶电离,写出液氨的自偶电离方程反应过程式
H3O++OH-,液氨也能发生自偶电离,写出液氨的自偶电离方程反应过程式_________ ;NH2-电子式为________ 。
(3)次氯酸钠溶液中离子浓度由大到小顺序为________ ;将氨气通入到次氯酸钠溶液中可制得联氨(N2H4),写出反应的离子方程式__________ ;用四氧化二氮作助燃剂,联氨可作火箭燃料。已知:N2(g)+2O2(g)= 2NO2(g),ΔH,= +67.7kJ/mol;N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;N2O4(g)=2NO2(g),ΔH3=+ 57kJ/mol,写出气态的联氨在四氧化二氮气体中燃烧生成两种无污染气态产物的热化学方程式______ 。
(4)将2.04mol/L的氨水与0.02mo/L的硝酸银溶液等体积混合得到混合溶液,混合体系中存在平衡:Ag+(aq) +2NH3·H2O(aq) Ag(NH3)2+(aq)+2H2O(1),平衡常数表达式K=
Ag(NH3)2+(aq)+2H2O(1),平衡常数表达式K=_________ ;在常温时K=1×107,由于氨水过量,银离子几乎反应完全,计算此时混合溶液中c(Ag+)=_________ mol/ L。

(1)曲线
(2)水的自偶电离方程式为2H2O
 H3O++OH-,液氨也能发生自偶电离,写出液氨的自偶电离方程反应过程式
H3O++OH-,液氨也能发生自偶电离,写出液氨的自偶电离方程反应过程式(3)次氯酸钠溶液中离子浓度由大到小顺序为
(4)将2.04mol/L的氨水与0.02mo/L的硝酸银溶液等体积混合得到混合溶液,混合体系中存在平衡:Ag+(aq) +2NH3·H2O(aq)
 Ag(NH3)2+(aq)+2H2O(1),平衡常数表达式K=
Ag(NH3)2+(aq)+2H2O(1),平衡常数表达式K=
您最近一年使用:0次



