(1)向Fe(OH)3胶体中逐滴加入氢碘酸。
现象:____________________________________________________________
离子方程式:________________________________________________
(2)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与ClO 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为_________ ;离子方程式为_________________________________ 。
(3)H2与Cl2混合点燃,充分反应后,将气体通入含有40gNaOH的溶液中恰好完全反应,则混合气体中Cl2质量为________ 。
(4)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式________________________________________________ 。
现象:
离子方程式:
(2)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与ClO
 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为(3)H2与Cl2混合点燃,充分反应后,将气体通入含有40gNaOH的溶液中恰好完全反应,则混合气体中Cl2质量为
(4)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式
更新时间:2020-11-16 09:24:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
(1)下列制备氢氧化铁胶体的操作方法正确的是____________ (填字母);
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c. 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液
d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式__________________________ ;
(3)下列与胶体性质无关的是_____________ (填字母);
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫_____________ 。
(1)下列制备氢氧化铁胶体的操作方法正确的是
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c.
 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式
(3)下列与胶体性质无关的是
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】杨老师化学兴趣小组在实验室取一定量Fe2O3粉末(红棕色)加入适量某浓度的盐酸中,得到呈棕黄色的饱和FeCl3溶液,利用此溶液进行以下实验:
(1)写出生成饱和FeCl3溶液时所发生反应的离子方程式为_______ 。
(2)将FeCl3溶液加到沸水中,加热至整个体系呈_______ 色为止,即制得Fe(OH)3胶体。小何同学想证明Fe(OH)3胶体已经制备成功,他可以利用_______ (最简单的方法)进行鉴别。
(3)小宁同学制备时加热时间过久,结果未能得到胶体,而得到的是Fe(OH)3悬浊液,那么分离Fe(OH)3与水的悬浊液常用的方法是_______ (填写操作名称)。
(4)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是_______
A.两者颜色相同
B.两者稳定性相同
C.两者的分子直径均大于100nm
D.滴加稀盐酸后,两者现象完全相同
E.胶体微粒能透过滤纸,但不能透过半透膜。
(5)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2 +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为_______ ,该离子反应中氧化剂与还原剂的个数比为_______ ,生成1个高铁酸钠转移_______ 个电子。
(1)写出生成饱和FeCl3溶液时所发生反应的离子方程式为
(2)将FeCl3溶液加到沸水中,加热至整个体系呈
(3)小宁同学制备时加热时间过久,结果未能得到胶体,而得到的是Fe(OH)3悬浊液,那么分离Fe(OH)3与水的悬浊液常用的方法是
(4)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是
A.两者颜色相同
B.两者稳定性相同
C.两者的分子直径均大于100nm
D.滴加稀盐酸后,两者现象完全相同
E.胶体微粒能透过滤纸,但不能透过半透膜。
(5)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2
 +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】从不同的角度对物质进行分类有利于研究物质的组成与性质。现有以下5种物质:①Cu;②NaCl;③饱和硫酸铁溶液;④KHSO4;⑤干冰;回答下列问题:
(1)以上物质能导电的有___________ (填序号)。
(2)以上物质属于电解质的有___________ (填序号,下同),属于非电解质的是___________ 。
(3)分别写出②、④在水中的电离方程式___________ 。
(4)①可溶解在③中,产物中金属元素均为+2价,该反应的离子方程式为___________ 。
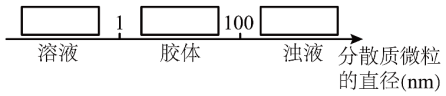
(5)将少量③分别滴加到下列物质中,得到三种分散系a、b、c。
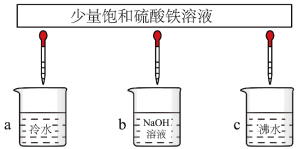
试将a、b、c符号以及对应的分散质具体的化学式填入下列方框中:___________ 。
(1)以上物质能导电的有
(2)以上物质属于电解质的有
(3)分别写出②、④在水中的电离方程式
(4)①可溶解在③中,产物中金属元素均为+2价,该反应的离子方程式为
(5)将少量③分别滴加到下列物质中,得到三种分散系a、b、c。

试将a、b、c符号以及对应的分散质具体的化学式填入下列方框中:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)下列物质 ①烧碱、②Fe(OH)3 胶体、③NaCl、④CO2、⑤铁片、⑥石墨、⑦甲烷、⑧HNO3、⑨CaCO3,其中属于混合物的是(填序号) ___________ ;属于酸的是 ___________ ;属于盐的是 ___________ ;属于非电解质的是 ___________ 。
(2)写出下列反应的离子方程式:
①AgNO3 溶液与 KCl 溶液混合:___________
②硫酸和氢氧化钡溶液混合:___________
③氢氧化钠溶液与盐酸溶液混合:___________
④锌投入硫酸铜溶液中:___________ 。
(2)写出下列反应的离子方程式:
①AgNO3 溶液与 KCl 溶液混合:
②硫酸和氢氧化钡溶液混合:
③氢氧化钠溶液与盐酸溶液混合:
④锌投入硫酸铜溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求作答。
(1)①写出MgO的名称
(2)写出NaHCO3受热分解的化学方程式
(3)写出Cl2与NaOH溶液反应的离子方程式
(4)海带中提取碘的过程中,将I-氧化生成I2时,若加入过量的氯水,则Cl2将I2氧化生成HIO3,同时还有一种强酸生成,写出该反应的化学方程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据要求回答下列问题:
(1)现有以下物质:①熔融 ;②干冰;③Cu;④
;②干冰;③Cu;④ 固体;⑤
固体;⑤ 固体;⑥NaOH固体,其中属于电解质并且此状态下能够导电的是
固体;⑥NaOH固体,其中属于电解质并且此状态下能够导电的是_______ ,(填序号,下同);属于酸性氧化物的是_______ 。
(2)酸性高锰酸钾溶液能与 溶液反应,且有气体产生,这说明
溶液反应,且有气体产生,这说明 具有
具有_______ 性(填“氧化”或“还原”)。
(3)“84”消毒液是一种家用消毒剂,原因是 具有强
具有强_______ 性,但不能与洁厕灵(含盐酸)混用,否则会生成有毒物质,该反应的离子反应为_______ 。
(4)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼( )。
)。
①肼的摩尔质量是_______ 。
②16g肼中含有氮原子的数目与_______ g 中含有的氮原子数相等。
中含有的氮原子数相等。
(1)现有以下物质:①熔融
 ;②干冰;③Cu;④
;②干冰;③Cu;④ 固体;⑤
固体;⑤ 固体;⑥NaOH固体,其中属于电解质并且此状态下能够导电的是
固体;⑥NaOH固体,其中属于电解质并且此状态下能够导电的是(2)酸性高锰酸钾溶液能与
 溶液反应,且有气体产生,这说明
溶液反应,且有气体产生,这说明 具有
具有(3)“84”消毒液是一种家用消毒剂,原因是
 具有强
具有强(4)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼(
 )。
)。①肼的摩尔质量是
②16g肼中含有氮原子的数目与
 中含有的氮原子数相等。
中含有的氮原子数相等。
您最近一年使用:0次
【推荐1】磷及其化合物有重要的用途,回答下列问题:
(1)工业上将磷酸钙、石英砂和碳粉混和在电弧炉中焙烧来制取白磷,配平方程式:
______  +
+______  +
+______ 
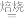
______ 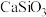 +
+______  +
+______  。
。
(2)白磷易自燃,保存的方法是__________________ ,白磷有毒,皮肤上沾有少量的白磷,可以用硫酸铜溶液处理,发生的反应是: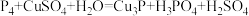 ,该反应的氧化剂是
,该反应的氧化剂是________________________ (填化学式)。
(3) 俗称为膦,电子式为:
俗称为膦,电子式为:________________________ ,沸点比较:
__________  (填”“高于”或“低于”)。
(填”“高于”或“低于”)。
(4)P2O5是常见的气体干燥剂,下列气体能用它干燥的是_______________ 。
A B
B C SO2 D CO2
C SO2 D CO2
也可以发生反应: ,该反应中
,该反应中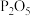 表现的性质是
表现的性质是_________ 。
(1)工业上将磷酸钙、石英砂和碳粉混和在电弧炉中焙烧来制取白磷,配平方程式:
 +
+ +
+
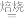
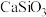 +
+ +
+ 。
。(2)白磷易自燃,保存的方法是
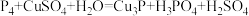 ,该反应的氧化剂是
,该反应的氧化剂是(3)
 俗称为膦,电子式为:
俗称为膦,电子式为:
 (填”“高于”或“低于”)。
(填”“高于”或“低于”)。(4)P2O5是常见的气体干燥剂,下列气体能用它干燥的是
A
 B
B C SO2 D CO2
C SO2 D CO2也可以发生反应:
 ,该反应中
,该反应中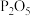 表现的性质是
表现的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】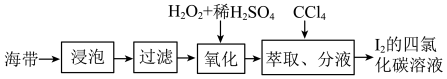
2.选择
 作萃取剂的现象为
作萃取剂的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为________ 。
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为________ mol;产生“气泡”的化学方程式为___________________ 。
(3)FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2+NaNO2,,上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2,,上述反应配平后FeO·Cr2O3与NaNO3的系数比为________ 。该步骤不能使用陶瓷容器,原因是_________ 。
(4)已知FePO4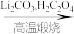 LiFePO4,写出该反应的化学方程式
LiFePO4,写出该反应的化学方程式_______ 。
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(3)FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2+NaNO2,,上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2,,上述反应配平后FeO·Cr2O3与NaNO3的系数比为(4)已知FePO4
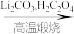 LiFePO4,写出该反应的化学方程式
LiFePO4,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)实验室里可以用KMnO4与浓盐酸反应制取氯气,其反应的离子方程式为: ________
(2)某温度下,将Cl2通入NaOH 溶液中,反应得到含有C1O-与C1O3-物质的量之比为1: 1的混合液,
反应的化学方程式是________________________ 。
(3)“流感”成为2017 年冬季最可怕的流行病,历城二中要求每班每天必须用“84”消毒液进行消
毒,已知某品牌“84”消毒液的有效成分为NaClO,写出向该溶液中通入过量的CO2所发生的有关离子方程式________________________
(4)氰(CN) 2的化学性质和卤素(X2) 很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:_______
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当
于多少克Cl2的氧化能力。NaClO2的有效氯含量为_________ 。(计算结果保留两位小数)
(2)某温度下,将Cl2通入NaOH 溶液中,反应得到含有C1O-与C1O3-物质的量之比为1: 1的混合液,
反应的化学方程式是
(3)“流感”成为2017 年冬季最可怕的流行病,历城二中要求每班每天必须用“84”消毒液进行消
毒,已知某品牌“84”消毒液的有效成分为NaClO,写出向该溶液中通入过量的CO2所发生的有关离子方程式
(4)氰(CN) 2的化学性质和卤素(X2) 很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当
于多少克Cl2的氧化能力。NaClO2的有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产,生活、科研具有重要意义。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,工业上可利用反应NHI3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备。
①一氯胺(NH2Cl)在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质,该物质的电子式为___________ 。
②氨气也是工业上制备硝酸的主要原料,制备硝酸的过程中涉及NO2与水的反应。该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)SO2、NO2两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收SO2能得到含 (NH4)2SO3和NH4HSO3的吸收液,写出生成(NH4)2SO3的离子方程式:___________ 。若向吸收液中通入过量NO2,NH4HSO3能与NO2发生反应生成N2和(NH4)2SO4,写出该反应的离子方程式:___________ 。
(3)Cl2与NaOH溶液反应可制取“84”消毒液。用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3,),此时ClO-的浓度为c0 mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①写出溶液中NaClO分解生成NaClO3的化学方程式:___________ 。
②t时刻溶液中c(Cl-)=___________ mol/L(用含c0、c1的代数式表示)。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,工业上可利用反应NHI3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备。
①一氯胺(NH2Cl)在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质,该物质的电子式为
②氨气也是工业上制备硝酸的主要原料,制备硝酸的过程中涉及NO2与水的反应。该反应中氧化剂与还原剂的物质的量之比为
(2)SO2、NO2两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收SO2能得到含 (NH4)2SO3和NH4HSO3的吸收液,写出生成(NH4)2SO3的离子方程式:
(3)Cl2与NaOH溶液反应可制取“84”消毒液。用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3,),此时ClO-的浓度为c0 mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①写出溶液中NaClO分解生成NaClO3的化学方程式:
②t时刻溶液中c(Cl-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是___________ (填化学式);用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是___________ (用化学方程式表示)。
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是___________ ;漂白粉也能用于消毒,其有效成分生效的化学方程是___________ 。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是
您最近一年使用:0次



