碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知: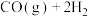
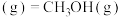
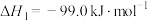 。
。
(1)该反应的熵变
_______ 0(填“>”“<”“=”),该反应自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
_______  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、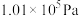 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式_______ 。
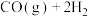
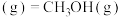
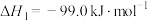 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、
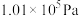 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
更新时间:2023-08-12 07:21:49
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:_______ ;又已知H2O(l)=H2O(g) ΔH=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______ kJ。
(2)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:_______ 。若1g水蒸气转化成液态水放热2.444kJ,写出表示氢气燃烧热的热化学方程式:_______ 。
(3)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为_______ ,则KOH与H2SO4反应的中和热为_______ 。
(4)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:
(2)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:
(3)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为
(4)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
【推荐2】请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是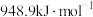 ,
, 键的键能是
键的键能是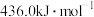 ,
, 键的键能是
键的键能是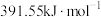 ,则
,则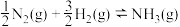

___________ 。
(3)已知:①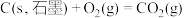

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①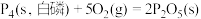

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
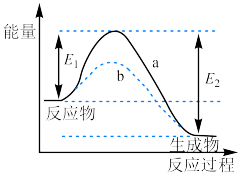
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是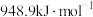 ,
, 键的键能是
键的键能是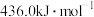 ,
, 键的键能是
键的键能是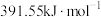 ,则
,则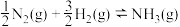

(3)已知:①
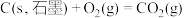

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
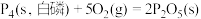

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为___________ 。
(2)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
①直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g),∆H1=172kJ·mol-1,Kp1=1.0×10-2Pa
②碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g),∆H2=-51kJ·mol-1,Kp2=1.2×1012Pa
反应2C(s)+O2(g)=2CO(g)的∆H为___________ kJ·mol-1,Kp=___________ Pa。
(3)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g),ΔH1=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g),ΔH2=94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g),ΔH3=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)+O2(g)=S2(g)+2H2O(g)的ΔH4=___________ kJ·mol-1
(1)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为
(2)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
①直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g),∆H1=172kJ·mol-1,Kp1=1.0×10-2Pa
②碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g),∆H2=-51kJ·mol-1,Kp2=1.2×1012Pa
反应2C(s)+O2(g)=2CO(g)的∆H为
(3)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g),ΔH1=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g),ΔH2=94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g),ΔH3=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)+O2(g)=S2(g)+2H2O(g)的ΔH4=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组设计用50 mL 0.50 mol/L盐酸跟50 mL0.55 mol/L 氢氧化钠溶液在如图装置中进行中和反应,测得的中和热为ΔH1。试回答下列问题:

(1)仪器A的名称___________ 。
(2)本实验中在大小烧杯间填充泡沫塑料的作用是___________ 。
(3)若用等浓度的醋酸与NaOH溶液反应,测得的中和热为ΔH2,若用浓硫酸与NaOH溶液反应,测得的中和热为ΔH3,下列说法正确的是___________。
(4)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。
目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) △H1
(NH4)2CO3(aq) △H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) △H2
NH4HCO3(aq) △H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) △H3
2NH4HCO3(aq) △H3
则△H3与△H1、△H2之间的关系是:△H3=___________ 。

(1)仪器A的名称
(2)本实验中在大小烧杯间填充泡沫塑料的作用是
(3)若用等浓度的醋酸与NaOH溶液反应,测得的中和热为ΔH2,若用浓硫酸与NaOH溶液反应,测得的中和热为ΔH3,下列说法正确的是___________。
| A.ΔH1>ΔH2>ΔH3 | B.ΔH3>ΔH1>ΔH2 | C.ΔH2>ΔH1>ΔH3 | D.ΔH1=ΔH2>ΔH3 |
目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) △H1
(NH4)2CO3(aq) △H1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) △H2
NH4HCO3(aq) △H2反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) △H3
2NH4HCO3(aq) △H3则△H3与△H1、△H2之间的关系是:△H3=
您最近一年使用:0次
【推荐2】氨气是一种重要的化学物质,可用于制取化肥和硝酸等。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
表中a为___________ 。
(2)合成氨原料气由天然气在高温下与水和空气反应而得。涉及的主要反应如下:
I.CH4(g)+H2O(g)→CO(g)+3H2(g)
II.2CH4(g)+O2(g)→2CO(g)+4H2(g)
III.CO(g)+H2O(g)→H2(g)+CO2(g)
假设反应产生的CO全部转化为CO2,CO2被碱液完全吸收,剩余的H2O通过冷凝干燥除去。进入合成氨反应塔的原料气为纯净的N2和H2。
①为使原料气中N2和H2的体积比为1:3,推出起始气体中CH4和空气的比例___________ (设空气中O2和N2的体积比为1:4,所有气体均按理想气体处理)。
②已知:IV.C(s)+2H2(g)→CH4(g) ∆H4=-74.8kJ∙mol-1
V.C(s)+ O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
计算反应II的反应热___________ 。
(3)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III.C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为___________ 。
②根据反应I、II、III,下列说法正确的是___________ (填选项字母)。
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
 。
。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol| N-H | H-H | N≡N | |
| 断开1 mol化学键需要吸收的能量/kJ | a | 436 | 946 |
表中a为
(2)合成氨原料气由天然气在高温下与水和空气反应而得。涉及的主要反应如下:
I.CH4(g)+H2O(g)→CO(g)+3H2(g)
II.2CH4(g)+O2(g)→2CO(g)+4H2(g)
III.CO(g)+H2O(g)→H2(g)+CO2(g)
假设反应产生的CO全部转化为CO2,CO2被碱液完全吸收,剩余的H2O通过冷凝干燥除去。进入合成氨反应塔的原料气为纯净的N2和H2。
①为使原料气中N2和H2的体积比为1:3,推出起始气体中CH4和空气的比例
②已知:IV.C(s)+2H2(g)→CH4(g) ∆H4=-74.8kJ∙mol-1
V.C(s)+
 O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1计算反应II的反应热
(3)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III.C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为
②根据反应I、II、III,下列说法正确的是
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
 。
。
您最近一年使用:0次
【推荐3】用“>”“<”或“=”填空:
(1)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1________ ΔH2。
(2)相同条件下,2 mol氢原子所具有的能量______ 1 mol氢分子所具有的能量。
(3)已知常温下红磷比白磷稳定,比较下列反应中(反应条件均为点燃)ΔH的大小:ΔH1______ ΔH2。
①P4(白磷,s)+5O2(g)===2P2O5(s) ΔH1,
②4P(红磷,s)+5O2(g)===2P2O5(s) ΔH2。
(4)已知:101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则碳的燃烧热数值________ 110.5 kJ·mol-1。
(5)已知:稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量________ 57.3 kJ;稀硫酸和稀氢氧化钡溶液中和生成1 mol 水放出的热量_______________ 57.3 kJ。
(6)已知一定条件下合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.0 kJ·mol-1,相同条件下将1 mol N2和3 mol H2放在一密闭容器中充分反应,测得反应放出的热量(假定热量无损失)
2NH3(g) ΔH=-92.0 kJ·mol-1,相同条件下将1 mol N2和3 mol H2放在一密闭容器中充分反应,测得反应放出的热量(假定热量无损失)________ 92.0 kJ。
(1)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1
(2)相同条件下,2 mol氢原子所具有的能量
(3)已知常温下红磷比白磷稳定,比较下列反应中(反应条件均为点燃)ΔH的大小:ΔH1
①P4(白磷,s)+5O2(g)===2P2O5(s) ΔH1,
②4P(红磷,s)+5O2(g)===2P2O5(s) ΔH2。
(4)已知:101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则碳的燃烧热数值
(5)已知:稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量
(6)已知一定条件下合成氨反应:N2(g)+3H2(g)
 2NH3(g) ΔH=-92.0 kJ·mol-1,相同条件下将1 mol N2和3 mol H2放在一密闭容器中充分反应,测得反应放出的热量(假定热量无损失)
2NH3(g) ΔH=-92.0 kJ·mol-1,相同条件下将1 mol N2和3 mol H2放在一密闭容器中充分反应,测得反应放出的热量(假定热量无损失)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
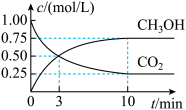
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____ mol/(L·min)。
②该反应的平衡常数表达式为K=_________ 。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________ 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案_______ (填“是”、“否”)可行,理由是:_______ 。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②该反应的平衡常数表达式为K=
③下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知甲烷隔绝空气在不同温度下有可能发生如下两个裂解反应:①CH4(g)→C(s)+2H2(g);②2CH4(g)→C2H2(g)+3H2(g)某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆中查到了如下热力学数据:
反应①的ΔH(298K)=+74.848kJ·mol-1,ΔS(298K)=+80.674J·mol-1·K-1。
反应②的ΔH(298K)=+376.426kJ·mol-1,ΔS(298K)=+220.211J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题:
(1)这两个反应在___________ (填“高温”或“低温”)下自发进行。
(2)反应①在常温下___________ (填“能”或“不能”)自发进行。
(3)制取炭黑的允许温度范围为___________ 。
(4)为了提高甲烷的炭化程度,下面四个温度中最合适的是___________(填字母)
反应①的ΔH(298K)=+74.848kJ·mol-1,ΔS(298K)=+80.674J·mol-1·K-1。
反应②的ΔH(298K)=+376.426kJ·mol-1,ΔS(298K)=+220.211J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题:
(1)这两个反应在
(2)反应①在常温下
(3)制取炭黑的允许温度范围为
(4)为了提高甲烷的炭化程度,下面四个温度中最合适的是___________(填字母)
| A.905.2K | B.927K | C.1273K | D.2000K |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为____________________ ,其中氮的化合价为________ 。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________________ 。
(3)①2O2(g)+N2(g)===N2O4(l) ΔH1
②N2(g)+2H2(g)===N2H4(l) ΔH2
③O2(g)+2H2(g)===2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH4=-1048.9 kJ·mol-1
上述反应热效应之间的关系式为ΔH4=____________ ,联氨和N2O4可作为火箭推进剂的主要原因为__________________________________ 。
Ⅱ.煤燃烧排放的烟气含SO2和NO2,形成酸雨,污染大气。现用NaClO、Ca(ClO)2处理,得到较好的烟气脱硫效果。
(4)已知下列反应:
SO2(g)+2OH-(aq)===SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq)===SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)===Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)===CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=________ 。
Ⅲ.(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25 ℃,101 kPa时:
CaO(s)+H2SO4(l)===CaSO4(s)+H2O(l)'ΔH=-271 kJ/mol
5CaO(s)+3H3PO4(l)+HF(g)===Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是__________________ 。
Ⅳ.(6)氢气可用于制备H2O2。已知:
H2(g)+A(l)===B(l) ΔH1
O2(g)+B(l)===A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+O2(g)===H2O2(l)的ΔH________ 0(填“>”“<”或“=”)。
(1)联氨分子的电子式为
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
(3)①2O2(g)+N2(g)===N2O4(l) ΔH1
②N2(g)+2H2(g)===N2H4(l) ΔH2
③O2(g)+2H2(g)===2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH4=-1048.9 kJ·mol-1
上述反应热效应之间的关系式为ΔH4=
Ⅱ.煤燃烧排放的烟气含SO2和NO2,形成酸雨,污染大气。现用NaClO、Ca(ClO)2处理,得到较好的烟气脱硫效果。
(4)已知下列反应:
SO2(g)+2OH-(aq)===SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq)===SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)===Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)===CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
Ⅲ.(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25 ℃,101 kPa时:
CaO(s)+H2SO4(l)===CaSO4(s)+H2O(l)'ΔH=-271 kJ/mol
5CaO(s)+3H3PO4(l)+HF(g)===Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
Ⅳ.(6)氢气可用于制备H2O2。已知:
H2(g)+A(l)===B(l) ΔH1
O2(g)+B(l)===A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+O2(g)===H2O2(l)的ΔH
您最近一年使用:0次



