H、C、N、O、F、S等是重要的非金属元素,回答下列问题:
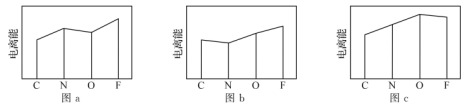
(1)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是_______ (填标号),判断的根据是_______ 。
(2)已知C—H、C—F的键能分别为413.4 、485
、485 。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(
。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。
)的共聚物(ETFE)制成。 、
、 分子的稳定性关系:前者
分子的稳定性关系:前者_______ 后者(填“大于”或“小于”),原因是_______ 。
(3)相同条件下, 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是_______ (写分子式),理由是_______ 。
(4)已知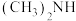 比
比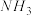 接收质子的能力强,可能的原因是
接收质子的能力强,可能的原因是_______ 。
(1)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是

(2)已知C—H、C—F的键能分别为413.4
 、485
、485 。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(
。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。
)的共聚物(ETFE)制成。 、
、 分子的稳定性关系:前者
分子的稳定性关系:前者(3)相同条件下,
 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是(4)已知
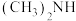 比
比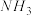 接收质子的能力强,可能的原因是
接收质子的能力强,可能的原因是
更新时间:2023-03-20 14:21:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ/mol则M、N相比,较稳定的是________ 。

(2)已知CH3OH(l)的燃烧热为-726.5 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a________ 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_______________________________ 。
(4) 已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1;CO(g)+l/2O2(g)=CO2(g)△H=-283. 0kJ • mol-1;C(石墨)+O2(g)=CO2(g)△H=-393.5kJ • mol-1。则4Fe (s)+3O2(g) =2Fe2O3(s)△H=____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ/mol则M、N相比,较稳定的是

(2)已知CH3OH(l)的燃烧热为-726.5 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4) 已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ • mol-1;CO(g)+l/2O2(g)=CO2(g)△H=-283. 0kJ • mol-1;C(石墨)+O2(g)=CO2(g)△H=-393.5kJ • mol-1。则4Fe (s)+3O2(g) =2Fe2O3(s)△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为___________ 。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。。
(1)H2燃烧热的热化学方程式为
(2)燃烧1gH2生成液态水,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中的主要污染物是NOx和CO,它们是现代化城市中的重要大气污染物。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是_______ ,图1中对应反应的热化学方程式为_______ 。 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。_______ ,该反应的△H=_______ ;
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H_______ (填“增大”“减小”或“不变”)。
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:
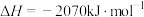 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为_______ kJ。
(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①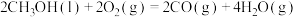 △H =-a kJ/mol
△H =-a kJ/mol
② △H =-b kJ/mol
△H =-b kJ/mol
③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是

 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。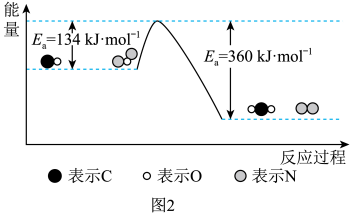
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:

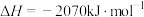 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①
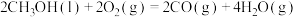 △H =-a kJ/mol
△H =-a kJ/mol②
 △H =-b kJ/mol
△H =-b kJ/mol ③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁镁合金是一种性能优异的储氢材料。关于铁镁两种元素,请回答下列问题:
(1)同周期元素中,第一电离能小于镁的元素有___________ 种。
(2)基态Fe原子的简化电子排布式为___________ ,其中电子的空间运动状态有___________ 种,Fe位于元周期表的___________ 区。
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有___________ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是___________ (填标号)。 易被氧化为
易被氧化为
___________ 。
(1)同周期元素中,第一电离能小于镁的元素有
(2)基态Fe原子的简化电子排布式为
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
a.[Ar] 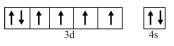 b.[Ar]
b.[Ar]
c.[Ar] d.[Ar]
d.[Ar]
 易被氧化为
易被氧化为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】运用物质结构与性质的相关知识,回答下列问题:
(1)下列状态的铝中,电离最外层一个电子所需能量最大的是_______。
(2)Mo的价层电子排布式为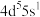 ,Mo在周期表中的位置为
,Mo在周期表中的位置为_______ ,Mo3+价层电子轨道表示式为_______ 。
(3) 气态为单分子,根据价层电子对互斥理论,该分子的立体构型为
气态为单分子,根据价层电子对互斥理论,该分子的立体构型为_______ ;
(4)如图为 的结构,硫原子之间形成的是
的结构,硫原子之间形成的是_______ 共价键(填“极性”或“非极性”),硫原子采用的轨道杂化类型为_______ ,成键轨道之间以_______ 方式重叠形成_______ 键。

氨硼烷( )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(5)根据对角线规则,B的一些化学性质与元素_______ 的相似。
(6) 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(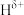 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(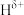 ),电负性大小顺序是
),电负性大小顺序是_______ 。
(1)下列状态的铝中,电离最外层一个电子所需能量最大的是_______。
A. | B.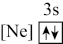 | C. | D.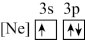 |
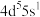 ,Mo在周期表中的位置为
,Mo在周期表中的位置为(3)
 气态为单分子,根据价层电子对互斥理论,该分子的立体构型为
气态为单分子,根据价层电子对互斥理论,该分子的立体构型为(4)如图为
 的结构,硫原子之间形成的是
的结构,硫原子之间形成的是
氨硼烷(
 )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(5)根据对角线规则,B的一些化学性质与元素
(6)
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(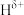 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(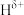 ),电负性大小顺序是
),电负性大小顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)向盛有CuSO4水溶液的试管里加入氨水,首先形成蓝色沉淀,继续加氨水,沉淀溶解,得到深蓝色的透明溶液,加入乙醇时,产生深蓝色的晶体。则:
①“首先形成蓝色沉淀”对应的离子方程式为____ 。
②实验过程中生成物中存在配离子____ (填离子符号)。其配体的中心原子的杂化类型为____ 。
(2)Cu2+可形成多种配合物,与Cu2+形成配合物的分子或离子应具备的结构特征是____ 。
(3)已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____ 。
(1)向盛有CuSO4水溶液的试管里加入氨水,首先形成蓝色沉淀,继续加氨水,沉淀溶解,得到深蓝色的透明溶液,加入乙醇时,产生深蓝色的晶体。则:
①“首先形成蓝色沉淀”对应的离子方程式为
②实验过程中生成物中存在配离子
(2)Cu2+可形成多种配合物,与Cu2+形成配合物的分子或离子应具备的结构特征是
(3)已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】螯合树脂吸附法处理废水具有吸附容量大、速度快以及选择性好等特点,已成为近年来的研究热点。螯合树脂M与Cu2+形成新的螯合物Q,从而达到去除Cu2+的效果,吸附机理如图所示。
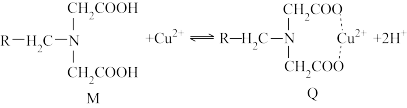
资料:
①吸附原理
螯合树脂M中的—COOH解离出H+,变成—COO-,而且树脂中含有N原子,在与Cu2+接触时,树脂中的—COO-、N原子与Cu2+形成配位键,形成新的螯合物Q,从而达到去除Cu2+的目的。
②在体系酸性较强情况下,氮原子与氢离子具有较强的配位能力。
(1)M中四种元素电负性由大到小的顺序为(用元素符号表示)____ 。
(2)M中N原子的杂化轨道类型为____ 。
(3)Q中存在配位键,其中提供空轨道的是____ 。
(4)在螯合树脂M处理含铜废水过程中,发现体系pH对Cu2+的吸附量有影响,实验结果如图所示。

①吸附去除Cu2+的过程中需保持体系处于适宜的pH,其中pH约为____ 时吸附效果最好。
②解释体系碱性过强时,吸附能力下降的原因____ 。
③从结构角度解释:体系酸性较强时,吸附能力下降的原因____ 。
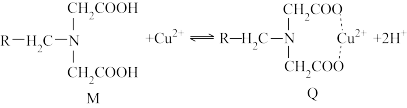
资料:
①吸附原理
螯合树脂M中的—COOH解离出H+,变成—COO-,而且树脂中含有N原子,在与Cu2+接触时,树脂中的—COO-、N原子与Cu2+形成配位键,形成新的螯合物Q,从而达到去除Cu2+的目的。
②在体系酸性较强情况下,氮原子与氢离子具有较强的配位能力。
(1)M中四种元素电负性由大到小的顺序为(用元素符号表示)
(2)M中N原子的杂化轨道类型为
(3)Q中存在配位键,其中提供空轨道的是
(4)在螯合树脂M处理含铜废水过程中,发现体系pH对Cu2+的吸附量有影响,实验结果如图所示。

①吸附去除Cu2+的过程中需保持体系处于适宜的pH,其中pH约为
②解释体系碱性过强时,吸附能力下降的原因
③从结构角度解释:体系酸性较强时,吸附能力下降的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式______________________ ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是_________________________ 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为______ ;在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键_______ 。

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为_______ ;该化合物的晶体熔点比干冰高得多,原因是_____ 。
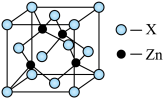
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是_______ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是_______ 。
(4)苯胺(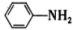 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
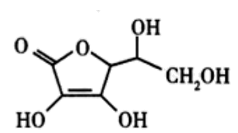
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:_______ (填“难溶于水”或“易溶于水”)。
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是
(4)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在极性分子中,正电荷重心与负电荷重心间的距离称为偶极长,通常用 表示。极性分子的极性强弱与偶极长和电荷量(
表示。极性分子的极性强弱与偶极长和电荷量(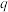 )有关,一般用偶极矩(
)有关,一般用偶极矩(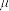 )来衡量。分子的偶极矩是偶极长和电荷量的乘积,即
)来衡量。分子的偶极矩是偶极长和电荷量的乘积,即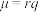 。在非极性分子中,其正、负电荷重心重合,故
。在非极性分子中,其正、负电荷重心重合,故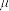 为0。试回答下列问题:
为0。试回答下列问题:
(1)HCl、CS2、H2S、SO2四种分子中 的有
的有______________________________ 。
(2)实验测得: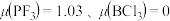
①由此可知,PF3分子的空间构型为____________________ ;
②BCl3分子的空间构型为____________________ ,中心原子的杂化方式为____________________ 。
(3)治癌药物 具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的
具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的 ,淡黄色化合物的
,淡黄色化合物的 。试写出两种同分异构体的结构简式:
。试写出两种同分异构体的结构简式:____________________ (棕黄色)、____________________ (淡黄色),在水中溶解度较大的是____________________ (填结构简式)。
 表示。极性分子的极性强弱与偶极长和电荷量(
表示。极性分子的极性强弱与偶极长和电荷量(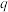 )有关,一般用偶极矩(
)有关,一般用偶极矩(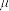 )来衡量。分子的偶极矩是偶极长和电荷量的乘积,即
)来衡量。分子的偶极矩是偶极长和电荷量的乘积,即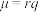 。在非极性分子中,其正、负电荷重心重合,故
。在非极性分子中,其正、负电荷重心重合,故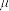 为0。试回答下列问题:
为0。试回答下列问题:(1)HCl、CS2、H2S、SO2四种分子中
 的有
的有(2)实验测得:
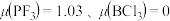
①由此可知,PF3分子的空间构型为
②BCl3分子的空间构型为
(3)治癌药物
 具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的
具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个顶点。已知该化合物有两种同分异构体,棕黄色化合物的 ,淡黄色化合物的
,淡黄色化合物的 。试写出两种同分异构体的结构简式:
。试写出两种同分异构体的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)写出元素m的基态一价离子的核外电子排布式:___________ 。
(2)对应元素氢化物沸点e高于j的原因:___________ 。
(3)元素q与h同族,化合物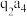 常用作火箭燃料,写出其电子式:
常用作火箭燃料,写出其电子式:___________ 。
(4)写出b的氢氧化物与f的氢氧化物反应的化学方程式___________ 。
(5)m和n比较:第一电离能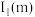
___________ 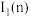 (填“大于”或“小于”),原因是
(填“大于”或“小于”),原因是___________ 。
(6)实验室制得元素k的单质中混有其氢化物,可用四氯化碳分离,其原理是:___________ 。

请回答下列问题:
(1)写出元素m的基态一价离子的核外电子排布式:
(2)对应元素氢化物沸点e高于j的原因:
(3)元素q与h同族,化合物
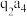 常用作火箭燃料,写出其电子式:
常用作火箭燃料,写出其电子式:(4)写出b的氢氧化物与f的氢氧化物反应的化学方程式
(5)m和n比较:第一电离能
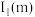
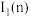 (填“大于”或“小于”),原因是
(填“大于”或“小于”),原因是(6)实验室制得元素k的单质中混有其氢化物,可用四氯化碳分离,其原理是:
您最近一年使用:0次



