螯合树脂吸附法处理废水具有吸附容量大、速度快以及选择性好等特点,已成为近年来的研究热点。螯合树脂M与Cu2+形成新的螯合物Q,从而达到去除Cu2+的效果,吸附机理如图所示。
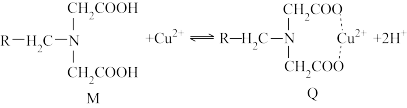
资料:
①吸附原理
螯合树脂M中的—COOH解离出H+,变成—COO-,而且树脂中含有N原子,在与Cu2+接触时,树脂中的—COO-、N原子与Cu2+形成配位键,形成新的螯合物Q,从而达到去除Cu2+的目的。
②在体系酸性较强情况下,氮原子与氢离子具有较强的配位能力。
(1)M中四种元素电负性由大到小的顺序为(用元素符号表示)____ 。
(2)M中N原子的杂化轨道类型为____ 。
(3)Q中存在配位键,其中提供空轨道的是____ 。
(4)在螯合树脂M处理含铜废水过程中,发现体系pH对Cu2+的吸附量有影响,实验结果如图所示。

①吸附去除Cu2+的过程中需保持体系处于适宜的pH,其中pH约为____ 时吸附效果最好。
②解释体系碱性过强时,吸附能力下降的原因____ 。
③从结构角度解释:体系酸性较强时,吸附能力下降的原因____ 。
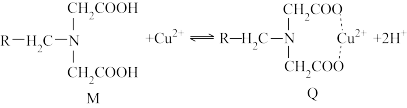
资料:
①吸附原理
螯合树脂M中的—COOH解离出H+,变成—COO-,而且树脂中含有N原子,在与Cu2+接触时,树脂中的—COO-、N原子与Cu2+形成配位键,形成新的螯合物Q,从而达到去除Cu2+的目的。
②在体系酸性较强情况下,氮原子与氢离子具有较强的配位能力。
(1)M中四种元素电负性由大到小的顺序为(用元素符号表示)
(2)M中N原子的杂化轨道类型为
(3)Q中存在配位键,其中提供空轨道的是
(4)在螯合树脂M处理含铜废水过程中,发现体系pH对Cu2+的吸附量有影响,实验结果如图所示。

①吸附去除Cu2+的过程中需保持体系处于适宜的pH,其中pH约为
②解释体系碱性过强时,吸附能力下降的原因
③从结构角度解释:体系酸性较强时,吸附能力下降的原因
2022·北京昌平·二模 查看更多[1]
更新时间:2022-05-06 21:50:55
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】材料是人类文明进步的阶梯,主族非金属元素是组成特殊材料的重要元素。请回答下列问题:
(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是_____ ,第一电离能从大到小的顺序是_____ 。
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是______ (填化学式);已知等电子体具有相同的空间构型,结合价电子对互斥理论可知N2O分子为______ 形。
(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是_____ (填符号);配合物T与[M(NH3)5(H2O)]Cl3组成所含微粒种类和数目相同,中心离子的配位数相同且T中也只有两种配体,若1molT溶于水,加入足量AgNO3溶液只生成2molAgCl,则T的配合物可表示为_____ 。
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为_____ 。

(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO
 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态 Ge 原子的简化电子排布式为_____ ,有_____ 个未成对电子,它在周期表的位置是_____ ,_____ 区。
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、叁键,但 Ge 原子之间难以形成双键或叁键。从 原子结构角度分析,原因是_____ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____ 。
(4)光催化还原 CO2 制备 CH4 反应中,带状纳米 Zn2GeO4 是该反应的良好催化剂。Zn、Ge、O 电负性由大至小的顺序是_______________ 。
(1)基态 Ge 原子的简化电子排布式为
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、叁键,但 Ge 原子之间难以形成双键或叁键。从 原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约 400 |
(4)光催化还原 CO2 制备 CH4 反应中,带状纳米 Zn2GeO4 是该反应的良好催化剂。Zn、Ge、O 电负性由大至小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】锰是国家紧缺战略矿产资源,广泛用于新能源、新材料等战略新兴产业,贵州地矿局研发的“气液喷溢沉积型锰矿”的找矿勘查关键技术体系,荣获贵州省2022年度十大科技创新成果。黔东地区集中分布的富锰矿床资源主体是菱锰矿( )。工业上可用菱锰矿生产锰的一种配合物
)。工业上可用菱锰矿生产锰的一种配合物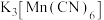 ,其主要应用于制药、电镀、造纸、钢铁生产。
,其主要应用于制药、电镀、造纸、钢铁生产。
(1)Mn元素在周期表中的位置为_____ ,基态Mn原子价电子排布式为_____ ,基态N原子核外电子空间运动状态有_____ 种。
(2)C、N、O三种元素中电负性最小的是_____ ,第一电离能最大的是_____ (填元素符号), 中的键角大小为
中的键角大小为_____ 。
(3)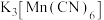 中Mn的化合价为+3价,则C的化合价为
中Mn的化合价为+3价,则C的化合价为_____ ,配体为_____ ,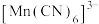 中
中 键与
键与 键的数目之比为
键的数目之比为_____ 。
 )。工业上可用菱锰矿生产锰的一种配合物
)。工业上可用菱锰矿生产锰的一种配合物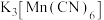 ,其主要应用于制药、电镀、造纸、钢铁生产。
,其主要应用于制药、电镀、造纸、钢铁生产。(1)Mn元素在周期表中的位置为
(2)C、N、O三种元素中电负性最小的是
 中的键角大小为
中的键角大小为(3)
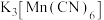 中Mn的化合价为+3价,则C的化合价为
中Mn的化合价为+3价,则C的化合价为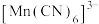 中
中 键与
键与 键的数目之比为
键的数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】黑火药是我国古代的四大发明之一,距今已有1000多年的历史,其成分是木炭(C)、硫粉(S)和硝酸钾(KNO3)。回答下列有关问题:
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为________________ 。
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕________ ,有____ 对成对电子。
(3)C、N、O、K的电负性由大到小的顺序是_________________ 。
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为_______________ 。
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是_________ ;KNO3可电离出NO3-,NO3-的空间构型是______________ 。
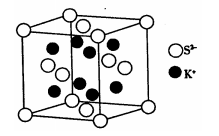
(6)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,若K2S晶体的密度为ρg·cm-3,则晶胞中距离最近的两个S2-核间距为_________ cm(用NA表示阿伏伽德罗常数的值)
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕
(3)C、N、O、K的电负性由大到小的顺序是
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是
(6)K2S的晶胞结构如图所示。其中K+的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式________ 。
(2)根据等电子原理,写出CO分子的结构式______ 。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是______________ ;甲醛分子中碳原子轨道的杂化类型为________ 。
②甲醛分子的空间构型是________ ;1 mol甲醛分子中σ键的数目为________ 。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式
(2)根据等电子原理,写出CO分子的结构式
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是
②甲醛分子的空间构型是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)Fe2+在基态时,核外电子排布式为_________ 。
(2)羟胺(NH2OH)中采用sp3杂化的原子有_________ ,羟胺熔沸点较高,是因为分子间存在较强的__________ 。
(3)Fe2+与邻啡罗啉形成的配合物(形成过程如图1)中,配位数为________ 。
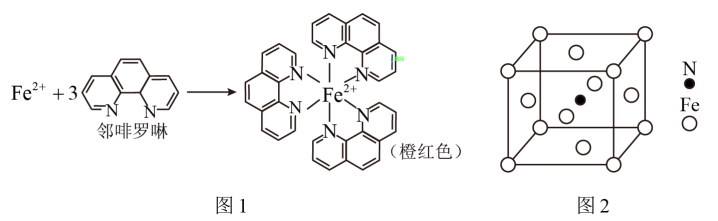
(4)根据价层互斥理论,ClO4-空间构形为___________ 。
(5)铁能与氮形成一种磁性材料,其晶胞结构如图2,该磁性材料的化学式为_______ 。
(2)羟胺(NH2OH)中采用sp3杂化的原子有
(3)Fe2+与邻啡罗啉形成的配合物(形成过程如图1)中,配位数为

(4)根据价层互斥理论,ClO4-空间构形为
(5)铁能与氮形成一种磁性材料,其晶胞结构如图2,该磁性材料的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)硫酸镍溶于过量的氨水可形成[Ni(NH3)6]SO4溶液。
①[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_____ ,中心原子(离子)是____ ;
②SO42-中,中心原子的轨道杂化类型为_______ ;
③写出一种与SO42-互为等电子体的分子的化学式______ ;
(2)NH3极易溶于水,除因为它们都是极性分子外,还因为__________ 。
(3)已知H—H键能为436kJ/mol,N≡N键的键能为945kJ/mol,根据化学方程式:N2+3H2 ==2NH3 ΔH=-92.4kJ/mol,则H—N键能为____ kJ/mol。
(4)下列分子既存在p-sp σ键,也存在p-p π键的是_____ 。
A.NH3 B.H2 C.CO2 D.C2H2
(5)根据已经掌握的共价键知识判断,键的极性N—H___ O—H(“>”,“=”或“<”)
①[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为
②SO42-中,中心原子的轨道杂化类型为
③写出一种与SO42-互为等电子体的分子的化学式
(2)NH3极易溶于水,除因为它们都是极性分子外,还因为
(3)已知H—H键能为436kJ/mol,N≡N键的键能为945kJ/mol,根据化学方程式:N2+3H2 ==2NH3 ΔH=-92.4kJ/mol,则H—N键能为
(4)下列分子既存在p-sp σ键,也存在p-p π键的是
A.NH3 B.H2 C.CO2 D.C2H2
(5)根据已经掌握的共价键知识判断,键的极性N—H
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】超分子化学在识别、催化、传输等功能方面已迅速渗透到各学科领域。如图是一种由两个相同分子(a)组装形成的分子盒(b)。请回答:
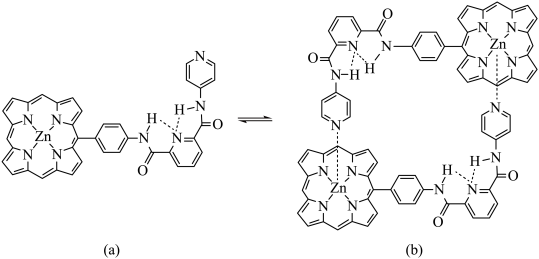
(1)两分子(a)通过______ 结合成(b)。
(2)(a)分子中C原子的杂化方式为______ ,基态Zn的价层电子轨道表示式为______ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为_____ 。

(1)两分子(a)通过
| A.离子键 | B.配位键 | C.氢键 | D.分子间作用力 |
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
您最近一年使用:0次



