锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态 Ge 原子的简化电子排布式为_____ ,有_____ 个未成对电子,它在周期表的位置是_____ ,_____ 区。
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、叁键,但 Ge 原子之间难以形成双键或叁键。从 原子结构角度分析,原因是_____ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____ 。
(4)光催化还原 CO2 制备 CH4 反应中,带状纳米 Zn2GeO4 是该反应的良好催化剂。Zn、Ge、O 电负性由大至小的顺序是_______________ 。
(1)基态 Ge 原子的简化电子排布式为
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、叁键,但 Ge 原子之间难以形成双键或叁键。从 原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约 400 |
(4)光催化还原 CO2 制备 CH4 反应中,带状纳米 Zn2GeO4 是该反应的良好催化剂。Zn、Ge、O 电负性由大至小的顺序是
更新时间:2018-04-24 11:20:48
|
相似题推荐
【推荐1】回答下列问题:
(1)2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。基态钛原子的px原子轨道上的电子数为___________ 。与钛同周期的第ⅡB族和第ⅢA族两种元素中第一电离能较大的是___________ (写元素符号)。
(2)互为同分异构体的两种有机物分子形成的氢键如图所示。

沸点:邻羟基苯甲醛___________ 对羟基苯甲醛(填“>”“=”或“<”),主要原因是___________ 。
(1)2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。基态钛原子的px原子轨道上的电子数为
(2)互为同分异构体的两种有机物分子形成的氢键如图所示。

沸点:邻羟基苯甲醛
您最近一年使用:0次
【推荐2】Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为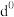 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
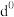 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.硒化锌是一种透明半导体,也可作为红外光学材料,熔点是1520℃。
(1)基态锌原子的价电子排布式是_____ 。
(2)根据元素周期律,电负性Se_____ S,Se位于周期表_____ 区。
(3)H2Se的分子构型是_____ ,其中硒原子的杂化轨道类型是_____ 。
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是_____ 。
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是_____ 。
(6)1molN2F2含有_____ molσ键。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是
(6)1molN2F2含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(2)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①发生反应的离子方程式为___________ 。
②为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为_________
③欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要___________ (选填字母)。
(3)纳米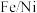 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:

①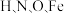 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是___________ 。
②反应ⅱ的离子方程式为___________ 。
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为___________ 。
(4)在 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。
已知:
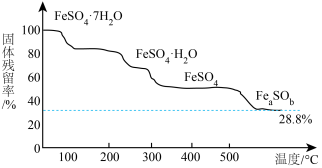
通过计算后,写出 受热分解的化学方程式
受热分解的化学方程式___________ 。
(1)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(2)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①发生反应的离子方程式为
②为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为③欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要(3)纳米
 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:
①
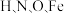 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是②反应ⅱ的离子方程式为
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为
(4)在
 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。已知:


通过计算后,写出
 受热分解的化学方程式
受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作用。
尿素 的合成揭开了人工合成有机物的序幕。其中各组成元素(氢除外,下同)电负性最弱的是
的合成揭开了人工合成有机物的序幕。其中各组成元素(氢除外,下同)电负性最弱的是_______ (填元素名称),第一电离能由小到大的顺序为_______ (填元素符号),氮原子的价层电子排布图为_______ 。
尿素
 的合成揭开了人工合成有机物的序幕。其中各组成元素(氢除外,下同)电负性最弱的是
的合成揭开了人工合成有机物的序幕。其中各组成元素(氢除外,下同)电负性最弱的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是_____________________ ,M2+的核外电子排布式为________________________ 。
(2)M2Z的熔点比M2W的_________ (填“高”或“低”) ,请解释原因___________ 。
(3)N3-和YZ2是等电子体,则N3-的结构式为_________________ 。
(4)WZ2分子中W原子价层电子对数是_____________ 对,WZ2的VSEPR 模型名称为______________________ ,WZ3气态为单分子,该分子中W原子的杂化轨道类型为__________________ ;WZ3的三聚体环状结构如图1所示,该结构中W原子的杂化轨道类型为__________ ;该结构中W-Z键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为___________ (填图2中字母) ,该分子中含有___ 个σ键。
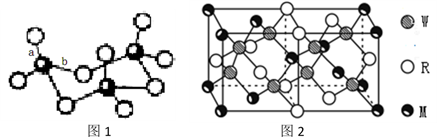
(5)MRW2的晶胞如图2所示,晶胞参数a=0.524nm、c=1.032nm;MRW2的晶胞中每个M原子与_______ 个W原子相连,晶体密度ρ=_______ g/cm3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA=6.02×1023mol-1)。
| 元素 | 相关信息 |
| Y | 原子核外有6个不同运动状态的电子 |
| Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
| W | 主族元素,与Z原子的价电子数相同 |
| R | 价层电子排布式为3d64s2 |
| M | IB族,其被称作“电器工业的主角” |
(1)Z、W元素相比,第一电离能较大的是
(2)M2Z的熔点比M2W的
(3)N3-和YZ2是等电子体,则N3-的结构式为
(4)WZ2分子中W原子价层电子对数是

(5)MRW2的晶胞如图2所示,晶胞参数a=0.524nm、c=1.032nm;MRW2的晶胞中每个M原子与
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题。
(1)OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O,原因是_______ 。
(2)硅、锗(Ge)及其化合物广泛应用于光电材料领域,晶体硅和碳化硅熔点较高的是_______ (填化学式)。
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(1)OF2的熔、沸点
(2)硅、锗(Ge)及其化合物广泛应用于光电材料领域,晶体硅和碳化硅熔点较高的是
(3)H2S、CH4、H2O的沸点由高到低顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知氯化铝的熔点为190℃(2.02×105 Pa),但它在180 ℃和常压下即开始升华。
(1)氯化铝是_______ 晶体(填“离子”或“分子”)。
(2)在500 ℃,1.01×105 Pa时,氯化铝的蒸气密度(换算成标准状况)为11.92 g·L-1,且已知它的结构中还含有配位键,氯化铝的结构式为_______ 。
(3)设计一个更可靠的实验,证明氯化铝是离子晶体还是分子晶体,你的实验是______ 。
(1)氯化铝是
(2)在500 ℃,1.01×105 Pa时,氯化铝的蒸气密度(换算成标准状况)为11.92 g·L-1,且已知它的结构中还含有配位键,氯化铝的结构式为
(3)设计一个更可靠的实验,证明氯化铝是离子晶体还是分子晶体,你的实验是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)已知氯乙酸的酸性强于醋酸,则酸性:
___________  (填:>、<或=)。
(填:>、<或=)。
(2)次磷酸( )与足量
)与足量 溶液反应生成
溶液反应生成 ,据此写出
,据此写出 的结构式
的结构式___________ 。
注:磷酸的结构式为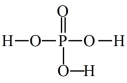
(3)常压下,苯和甲苯的熔、沸点如下表:
①苯的沸点比甲苯的沸点更低,主要原因是___________ 。
②苯晶体的熔点比甲苯的熔点更高,主要原因是___________ 。

 (填:>、<或=)。
(填:>、<或=)。(2)次磷酸(
 )与足量
)与足量 溶液反应生成
溶液反应生成 ,据此写出
,据此写出 的结构式
的结构式注:磷酸的结构式为

(3)常压下,苯和甲苯的熔、沸点如下表:
| 苯的模型 |  | 熔点: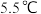 | 甲苯模型 |  | 熔点: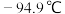 |
沸点: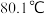 | 沸点: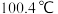 |
②苯晶体的熔点比甲苯的熔点更高,主要原因是
您最近一年使用:0次



