铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(2)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①发生反应的离子方程式为___________ 。
②为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为_________
③欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要___________ (选填字母)。
(3)纳米 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:

① 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是___________ 。
②反应ⅱ的离子方程式为___________ 。
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为___________ 。
(4)在 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。
已知:
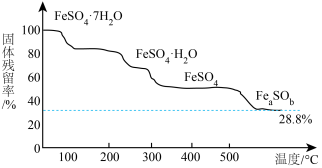
通过计算后,写出 受热分解的化学方程式
受热分解的化学方程式___________ 。
(1)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(2)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①发生反应的离子方程式为
②为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为③欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要(3)纳米
 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:
①
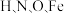 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是②反应ⅱ的离子方程式为
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为
(4)在
 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。已知:


通过计算后,写出
 受热分解的化学方程式
受热分解的化学方程式
更新时间:2023-09-17 17:46:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氨是一种重要的化工原料,氨的合成和应用是当前的研究热点。
(1)实验室制取氨气的化学原理是________ (用化学方程式表示),验满方法是________ 。
(2)已知:N2(g)+3H2(g) 2NH3(g) △H=-92kJ·mol-1,工业合成氨温度选择700K的原因是
2NH3(g) △H=-92kJ·mol-1,工业合成氨温度选择700K的原因是________ 。
(3)利用NH3处理硝酸工业尾气中的NOx,将其转化为无毒物质,该反应的化学方程式为________ 。
(4)水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图:

①利用平衡原理分析含氨氮水样中加入NaOH溶液的作用________ 。
②若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为3.9×10-4mol,则水样中氨氮(以氨气计)含量为________ mg·L-1。
(5)联氨(N2H4)为二元弱碱,在水中的电离方式与氨类似。25℃时,联氨的电离常数Kb1=3×10-6mol·L-1,Kb2=7.6×10-15mol·L-1。联氨和盐酸按物质的量之比1∶1反应的离子方程式是________ ,所得溶液呈________ 性(填“酸”、“中”或“碱”)。
(1)实验室制取氨气的化学原理是
(2)已知:N2(g)+3H2(g)
 2NH3(g) △H=-92kJ·mol-1,工业合成氨温度选择700K的原因是
2NH3(g) △H=-92kJ·mol-1,工业合成氨温度选择700K的原因是(3)利用NH3处理硝酸工业尾气中的NOx,将其转化为无毒物质,该反应的化学方程式为
(4)水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图:

①利用平衡原理分析含氨氮水样中加入NaOH溶液的作用
②若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为3.9×10-4mol,则水样中氨氮(以氨气计)含量为
(5)联氨(N2H4)为二元弱碱,在水中的电离方式与氨类似。25℃时,联氨的电离常数Kb1=3×10-6mol·L-1,Kb2=7.6×10-15mol·L-1。联氨和盐酸按物质的量之比1∶1反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】水体中的含氮化合物(以 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。
(1)酸性废水中的氨氮(主要是以 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。
①向该酸性废水中加入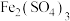 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为________ 价,除去氨氮的过程中生成 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为________ 。
②向该酸性废水中加入NaClO溶液可将 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为________ ;NaCl可以通过 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为________ 。
(2)使用NH3时也要注意防止污染环境。电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图:
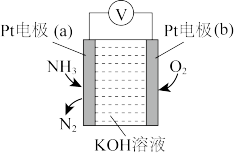
①Pt电极(a)为________ 极(填“正”或“负”);Pt电极(b)上的电极反应式为________ 。
②电池总反应的化学反应方程式为________ ,反应一段时间后,KOH溶液的浓度将________ (填“增大”“减小”或“不变”)。
 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。(1)酸性废水中的氨氮(主要是以
 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。①向该酸性废水中加入
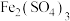 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为②向该酸性废水中加入NaClO溶液可将
 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为(2)使用NH3时也要注意防止污染环境。电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图:

①Pt电极(a)为
②电池总反应的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】《一种协同脱除VOCs和 的催化剂及其制备方法》是华电光大(宜昌)环保技术有限公司于2021年2月25日申请的专利,脱除
的催化剂及其制备方法》是华电光大(宜昌)环保技术有限公司于2021年2月25日申请的专利,脱除 是当前科学家研究的重要课题。
是当前科学家研究的重要课题。
(1) 对环境的一种危害是
对环境的一种危害是___________ 。
(2)碱性 氧化法可将
氧化法可将 进行脱除。
进行脱除。
① (NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整
(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整___________ 。
_____NO+_____ _____
_____
 ______
______ ____
____ ____
____
②下列叙述不正确的是___________ 填字时)。
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:
C.在不同酸碱性条件下, 发生氧化还原反应的产物可能不同
发生氧化还原反应的产物可能不同
③在实验室用 (NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为
(NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为 ,理论上需要
,理论上需要 的质量为
的质量为___________ g( 靡尔质量为158
靡尔质量为158 )。
)。
(3)用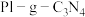 光催化氧化法脱除NO的过程如图所示。
光催化氧化法脱除NO的过程如图所示。

①该脱除过程中,太阳能转化为___________ 能。
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。 端的反应为
端的反应为
 ,P1端的反应为
,P1端的反应为___________ 。
 的催化剂及其制备方法》是华电光大(宜昌)环保技术有限公司于2021年2月25日申请的专利,脱除
的催化剂及其制备方法》是华电光大(宜昌)环保技术有限公司于2021年2月25日申请的专利,脱除 是当前科学家研究的重要课题。
是当前科学家研究的重要课题。(1)
 对环境的一种危害是
对环境的一种危害是(2)碱性
 氧化法可将
氧化法可将 进行脱除。
进行脱除。①
 (NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整
(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整_____NO+_____
 _____
_____
 ______
______ ____
____ ____
____
②下列叙述不正确的是
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:

C.在不同酸碱性条件下,
 发生氧化还原反应的产物可能不同
发生氧化还原反应的产物可能不同③在实验室用
 (NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为
(NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为 ,理论上需要
,理论上需要 的质量为
的质量为 靡尔质量为158
靡尔质量为158 )。
)。(3)用
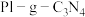 光催化氧化法脱除NO的过程如图所示。
光催化氧化法脱除NO的过程如图所示。
①该脱除过程中,太阳能转化为
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。
 端的反应为
端的反应为
 ,P1端的反应为
,P1端的反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某混合物A含有Al2(SO4)3、Al2O3和FeO,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是____________ .
(2)写出反应①、②、③、④四个反应的方程式(是离子反应的写离子方程式)
①_________ ;②_________ ;③_________ ;④___________ 。
(3)如果把步骤③中适量的盐酸改为过量的二氧化碳,则反应的离子方程式______________ 。
(4)在空气中将NaOH溶液滴入F溶液中,观察到的现象是______________ ,写出最终反应的化学方程式为_______________ 。

据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)写出反应①、②、③、④四个反应的方程式(是离子反应的写离子方程式)
①
(3)如果把步骤③中适量的盐酸改为过量的二氧化碳,则反应的离子方程式
(4)在空气中将NaOH溶液滴入F溶液中,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁、铝及其化合物的应用十分广泛,请回答:
(1)在实验室中,硝酸铝必须与可燃物分开存放,是因为硝酸铝具有____________ (填字母序号)。
A.可燃性 B.氧化性 C.还原性
(2)已知:当Al(NO3),溶液中pH>3时,铝元素有多种存在形态,如A13+、[Al(OH)]2+、[Al(OH)2]+等,各形态之间可相互转化,写出该溶液中[Al(OH)]2+转化为[Al(OH)2]+的离子方程式_________________ 。
(3)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为___________ ;从腐蚀废液中回收金属铜还需要的试剂是__________ 。
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),溶液中铁元素的存在形式为________ (填离子符号),检验该离子的实验操作、现象和结论是_________ ;参加反应的铁粉的质量为______________ 。
(1)在实验室中,硝酸铝必须与可燃物分开存放,是因为硝酸铝具有
A.可燃性 B.氧化性 C.还原性
(2)已知:当Al(NO3),溶液中pH>3时,铝元素有多种存在形态,如A13+、[Al(OH)]2+、[Al(OH)2]+等,各形态之间可相互转化,写出该溶液中[Al(OH)]2+转化为[Al(OH)2]+的离子方程式
(3)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),溶液中铁元素的存在形式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
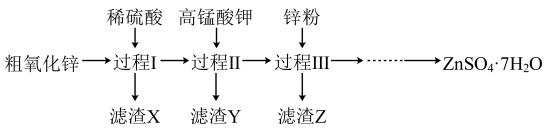
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是_______ 。
(2)过程Ⅰ,能与稀硫酸反应的物质有________ 。写出生成氢气的离子方程式:_______ ,因此过程Ⅰ需要持续强制通风,原因是生成的氢气具有______ 性。
(3)过程Ⅱ中,滤渣Y含有 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是_______ 。
(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为________ 。
 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是
(2)过程Ⅰ,能与稀硫酸反应的物质有
(3)过程Ⅱ中,滤渣Y含有
 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第_______ 周期第_______ 族,其基态原子的轨道表示式为_______ 。
(2)Cu的基态原子的电子排布式为_______ 。
(3)原子半径:Al_______ Si,电负性:N_______ O,第一电离能:C_______ N。(用“>”或“<”填空)
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
(1)Si位于元素周期表第
(2)Cu的基态原子的电子排布式为
(3)原子半径:Al
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
| A.是一种活泼的金属元素 | B.其电负性大于硅 |
| C.其单质可作为半导体材料 | D.其第一电离能小于硅 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】C、Si、S和N元素在化学中占有极其重要的地位。
(1)写出Si的基态原子价电子排布式______ 。从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为______ 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为______ ,微粒间存在的作用力是______ 。
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是______ 。
(4)SO2、NO2、H2S同属于______ 结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是______ 。
(1)写出Si的基态原子价电子排布式
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是
(4)SO2、NO2、H2S同属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)下列物质中:① ②金刚石 ③NaCl ④
②金刚石 ③NaCl ④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨Ne。只含离子键的是
⑨Ne。只含离子键的是_______ (填序号,下同 ),既含离子键又含共价键的是_______ ,不存在化学键的是_______ ,属于离子晶体的是_______ ,属于共价晶体的是_______ ,属于分子晶体的是_______ 。
(2)二氯化二硫 是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
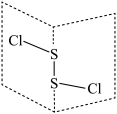
① 的化学键类型为
的化学键类型为_______ (填“极性键”、“非极性键”或“极性键和非极性键”),它是_______ (填“极性”或“非极性”)分子。
②电负性:S_______ (填“>”或“<”)Cl, 中硫元素的化合价为
中硫元素的化合价为_______ 。
③ 分子中每个S原子有
分子中每个S原子有_______ 个孤电子对。
(1)下列物质中:①
 ②金刚石 ③NaCl ④
②金刚石 ③NaCl ④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨Ne。只含离子键的是
⑨Ne。只含离子键的是(2)二氯化二硫
 是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
①
 的化学键类型为
的化学键类型为②电负性:S
 中硫元素的化合价为
中硫元素的化合价为③
 分子中每个S原子有
分子中每个S原子有
您最近一年使用:0次



