C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第_______ 周期第_______ 族,其基态原子的轨道表示式为_______ 。
(2)Cu的基态原子的电子排布式为_______ 。
(3)原子半径:Al_______ Si,电负性:N_______ O,第一电离能:C_______ N。(用“>”或“<”填空)
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
(1)Si位于元素周期表第
(2)Cu的基态原子的电子排布式为
(3)原子半径:Al
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
| A.是一种活泼的金属元素 | B.其电负性大于硅 |
| C.其单质可作为半导体材料 | D.其第一电离能小于硅 |
21-22高二上·山东济南·阶段练习 查看更多[2]
更新时间:2022-12-13 15:50:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是_______ (填元素符号),酸性最强的最高价氧化物对应水化物是______ (填化学式)。
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程___________ 。
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)非金属性①_____ ⑧(填“>”或“<”),请设计实验证明_________ (用化学方程式表示)。
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(6)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)最活泼的金属元素是
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)非金属性①
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(6)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素。
请用化学用语回答:
(1)推断B元素在元素周期表中的位置_______ ,写出C的单质的电子式____________ 。
(2)A与D形成的18电子的化合物与FD2化合生成一种强酸,其化学方程式为_________ 。
(3)E、F、G三种元素所形成的简单离子,其离子半径由大到小的顺序是______________ (用离子符号表示)。
(4)用电子式表示化合物E2F的形成过程____________________ 。
(5)下图为某新型发电装置示意图,其负极电极反应为_________ 。
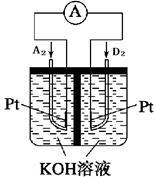
(6)在101 kPa、25℃下,16 g 液态C2A4在D2中完全燃烧生成气体C2,放出312 kJ热量,则C2A4和D2反应的热化学方程式为__________ 。
请用化学用语回答:
(1)推断B元素在元素周期表中的位置
(2)A与D形成的18电子的化合物与FD2化合生成一种强酸,其化学方程式为
(3)E、F、G三种元素所形成的简单离子,其离子半径由大到小的顺序是
(4)用电子式表示化合物E2F的形成过程
(5)下图为某新型发电装置示意图,其负极电极反应为

(6)在101 kPa、25℃下,16 g 液态C2A4在D2中完全燃烧生成气体C2,放出312 kJ热量,则C2A4和D2反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对①~⑩元素在表中的位置,回答下列问题:
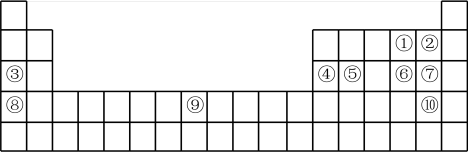
(1)⑨元素在元素周期表中的位置为___________ 。
(2)在①、②、③、④四种元素中,其离子半径按由大到小的顺序排列为___________ (用离子符号比较大小)。
(3)②、⑥、⑦元素所形成简单氢化物的稳定性由强到弱的顺序是___________ (用化学式比较强弱)。
(4)请写出⑥的最高价氧化物对应水化物和4的单质之间发生的化学方程式___________ 。
(5)写出⑩的单质与SO2水溶液反应的方程式:___________ 。
(6)写出工业制单质⑤的化学方程式___________ 。
(7)⑤的最高价氧化物与⑧的最高价氧化物对应的水化物反应的离子方程式___________ 。

(1)⑨元素在元素周期表中的位置为
(2)在①、②、③、④四种元素中,其离子半径按由大到小的顺序排列为
(3)②、⑥、⑦元素所形成简单氢化物的稳定性由强到弱的顺序是
(4)请写出⑥的最高价氧化物对应水化物和4的单质之间发生的化学方程式
(5)写出⑩的单质与SO2水溶液反应的方程式:
(6)写出工业制单质⑤的化学方程式
(7)⑤的最高价氧化物与⑧的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下图是元素周期表的一部分,所列的字母分别代表一种化学元素。试回答下列问题:
(1)基态n原子中,核外电子占据最高能层的符号是_______ ,占据该能层的电子云轮廓图形状为_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ 。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
①o元素价电子的轨道表示式为_______ 。
②比较两元素的 、
、 可知,气态
可知,气态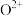 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为_______ (填元素符号)。
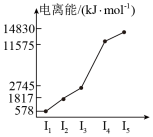
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式_______ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
| 元素 | o | p | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
②比较两元素的
 、
、 可知,气态
可知,气态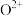 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,主要步骤如下:
Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C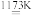 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C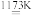 TiCl4+2CO
TiCl4+2CO
Ⅱ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg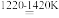 Ti+2MgCl2
Ti+2MgCl2
Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为___ 。
(2)与CO互为等电子体的离子为___ (填化学式)。
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有___ 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于___ (填“原子”“分子”或“离子”)晶体。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是___ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为___ 。
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为___ 。

Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C
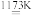 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6COTiO2+2Cl2+2C
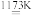 TiCl4+2CO
TiCl4+2COⅡ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg
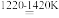 Ti+2MgCl2
Ti+2MgCl2Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为
(2)与CO互为等电子体的离子为
(3)在CH2Cl2、HCHO、CO2、C2H4中,碳原子采取sp2杂化的分子有
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种元素,其中A和B原子都有1个未成对电子,A+比B-少一个电子层。B原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子,其气态氢化物的水溶液的pH在同族氢化物中最大,D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D 40%,且其核内质子数等于中子数,据此判断:
(1)D是_______ 。(填元素名称)
(2)B-的电子排布式____ ,A+的结构示意图____ ,D原子的轨道表示式______ 。
(3)在A、B、D三种元素的简单离子中,其离子还原性最强的是________ 。(填离子符号)
(4)用电子式表示化合物AB的形成过程________________ 。
(1)D是
(2)B-的电子排布式
(3)在A、B、D三种元素的简单离子中,其离子还原性最强的是
(4)用电子式表示化合物AB的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用。回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:___________ ,其价电子轨道表示式为___________ 。
②比较键角大小:气态SeO3分子___________ Se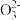 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是___________ 。
(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N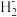 ,反应过程如图所示:
,反应过程如图所示:___________ 。
②与N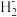 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

②比较键角大小:气态SeO3分子
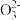 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为N
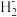 ,反应过程如图所示:
,反应过程如图所示: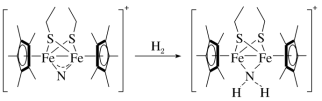
②与N
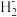 互为等电子体的一种分子为
互为等电子体的一种分子为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有下列几种晶体,按要求回答下列问题
A.SiO2 B.冰醋酸 C.白磷 D.金刚石 E.晶体氩 F.干冰
(1)干冰中C原子的杂化方式为:_______ ,其分子结构为:_______ 。
(2)SiO2中,Si的价电子排布图为:_______ 。
(3)属于分子晶体的是_______ (填字母,下同)。
(4)直接由原子构成的共价晶体是_______ 。
(5)受热融化时共价键不发生变化的晶体是_______ 。
(6)晶体中存在氢键的是_______ 。
A.SiO2 B.冰醋酸 C.白磷 D.金刚石 E.晶体氩 F.干冰
(1)干冰中C原子的杂化方式为:
(2)SiO2中,Si的价电子排布图为:
(3)属于分子晶体的是
(4)直接由原子构成的共价晶体是
(5)受热融化时共价键不发生变化的晶体是
(6)晶体中存在氢键的是
您最近一年使用:0次
【推荐1】回答下列问题
(1)写出基态As原子的核外电子排布式___________ 、基态碳原子的电子排布图___________ ,根据元素周期律,原子半径Ga___________ As,第一电离能Ga___________ As。(填“大于”或“小于”)
(2)镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ ;①C、N、O;②N、S、P;③C 、N、Si;④N、 O、F的第一电离能由大到小的顺序为___________ ;电负性:H、O、S电负性由大到小的顺序是___________ 。B和N相比,电负性较大的是___________ ;BN中B元素的化合价为___________ ;从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为___________ 。
(3)铬、铜、铁、锰等原子的基态电子排布式___________ ,氯元素的基态原子的价电子层排布式是___________ ,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号),第一电离能I1(C)、I1(N)、I1(O)由大到小的顺序为___________ 。
(4)基态Co原子核外电子排布式为___________ ,C、N、O三种元素的第一电离能由大到小的顺序为___________ (用具体元素符号表示)。
(5)基态Fe3+的M层电子排布式为___________ ,铝原子核外自旋方向相同的电子最多有___________ 个,与铝同族的第四周期元素原子的价电子排布式为___________ ,基态磷原子的核外电子运动状态共有___________ 种,其价电子排布式为___________ 。在硼、氧、氟、氮中第一电离能由大到小的顺序是___________ (用元素符号表示)。
(6)基态Ge原子的核外电子排布式为[Ar]___________ ,有___________ 个未成对电子。光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是___________ 。
(1)写出基态As原子的核外电子排布式
(2)镍元素基态原子的电子排布式为
(3)铬、铜、铁、锰等原子的基态电子排布式
(4)基态Co原子核外电子排布式为
(5)基态Fe3+的M层电子排布式为
(6)基态Ge原子的核外电子排布式为[Ar]
您最近一年使用:0次
【推荐2】已知OF2分子的极性比水分子的极性弱,其原因是______________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】常见晶体的结构分析
(1)金刚石晶体

①在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为_______ ,晶体中碳原子个数与C-C键数之比为_______ 。
②晶体中C-C-C夹角为_______ ,碳原子采取了_______ 杂化。
(2)二氧化硅晶体(如图):
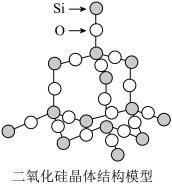
晶体中Si原子与O原子个数比为_______ ,1molSiO2晶体中含Si-O键数目为_______ (用NA表示阿伏加德罗常数)。
(3)Si原子与H原子结合时,Si呈正化合价,则电负性:Si_______ H(选填“<”或“>”)。锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有_______ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其气态氢化物的稳定性低于硅的气态氢化物
(4)A、B、C、D为四种晶体,依据下列晶体性质推断属于离子晶体的是_______。
(1)金刚石晶体

①在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为
②晶体中C-C-C夹角为
(2)二氧化硅晶体(如图):

晶体中Si原子与O原子个数比为
(3)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其气态氢化物的稳定性低于硅的气态氢化物
(4)A、B、C、D为四种晶体,依据下列晶体性质推断属于离子晶体的是_______。
| A.固态时能导电,能溶于盐酸 |
| B.固态时不导电,液态时能导电,可溶于水 |
| C.能溶于苯,不溶于水 |
| D.固态、液态时均不导电,熔点为3500℃ |
您最近一年使用:0次

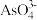 中和
中和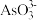 中
中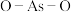 键角较大的是
键角较大的是 ,其空间构型为
,其空间构型为 可形成配离子
可形成配离子 ,该配离子中各元素的第一电离能由小到大的顺序为
,该配离子中各元素的第一电离能由小到大的顺序为

