针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是_______ (填元素符号),酸性最强的最高价氧化物对应水化物是______ (填化学式)。
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程___________ 。
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)非金属性①_____ ⑧(填“>”或“<”),请设计实验证明_________ (用化学方程式表示)。
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(6)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)最活泼的金属元素是
(2)用电子式表示⑤和⑨两种元素组成的化合物的形成过程
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)非金属性①
(5)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(6)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性; ⑨强于⑧
更新时间:2023-12-26 13:00:04
|
相似题推荐
【推荐1】按要求完成
(1)已知CO、 是N2的等电子体,写出CO、
是N2的等电子体,写出CO、 的电子式
的电子式___________ ,___________
(2)按键的极性强弱排序F—F、F—H、F—O___________
(3)键角比较:①CH 、CH
、CH
___________ ,②CO2、SO2、H2O___________ 。
(1)已知CO、
 是N2的等电子体,写出CO、
是N2的等电子体,写出CO、 的电子式
的电子式(2)按键的极性强弱排序F—F、F—H、F—O
(3)键角比较:①CH
 、CH
、CH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】科学工作者研发了一种 的系统,借助锂循环可持续合成氨,其原理如图所示:
的系统,借助锂循环可持续合成氨,其原理如图所示:
(1)过程Ⅰ得到Li3N的电子式为___________ 。
(2)过程Ⅱ生成W的化学反应方程式为____________ 。
(3)实验室制取氨气的化学反应方程式为___________ 。
 的系统,借助锂循环可持续合成氨,其原理如图所示:
的系统,借助锂循环可持续合成氨,其原理如图所示: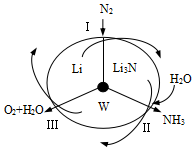
(1)过程Ⅰ得到Li3N的电子式为
(2)过程Ⅱ生成W的化学反应方程式为
(3)实验室制取氨气的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表为元素周期表的一部分,标出了A~K共十种元素所在位置。请用元素符号或化学式 回答下列问题。
(1)10种元素中,化学性质最不活泼的是______ ,最活泼的金属是_____ 。
(2)C、E、F三种元素形成的简单离子半径最小的是_______ 。
(3)化合物C2B2的电子式为__________________ ;该化合物和AB2反应的化学方程式为__________________________________________ 。
(4)E的最高价氧化物属于________________ 性氧化物,它与氢氧化钠溶液反应的离子方程式为____________________________________________ 。
(5)D的单质在A、B形成化合物中燃烧的化学方程式为________________________ 。
(6)用电子式表示H与B组成的H2B型化合物的形成过程_____________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | ||||||
| 3 | C | D | E | F | G | |||
| 4 | H | I | K |
(1)10种元素中,化学性质最不活泼的是
(2)C、E、F三种元素形成的简单离子半径最小的是
(3)化合物C2B2的电子式为
(4)E的最高价氧化物属于
(5)D的单质在A、B形成化合物中燃烧的化学方程式为
(6)用电子式表示H与B组成的H2B型化合物的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E元素形成的氧化物对应的水化物的化学式为______ 。
(2)元素B、C、D、E形成的简单离子半径大小关系是_________ 。(用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程:_________ 。
(4)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为_________ 。(化学式用具体的元素符号表示)。
(1)E元素形成的氧化物对应的水化物的化学式为
(2)元素B、C、D、E形成的简单离子半径大小关系是
(3)用电子式表示化合物D2C的形成过程:
(4)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,请用标出的元素回答有关问题:
⑴表中给出的化学性质最不活泼的元素,其原子结构示意图为__________________ 。
⑵表中能形成两性氢氧化物的元素是___________ (用元素符号表示),写出该元素形成的单质与⑨最高价氧化物对应的水化物反应的离子方程式:_______________________ 。
⑶用电子式表示④元素与⑦元素形成化合物的过程___________________________ 。
⑷写出②的最高价氧化物对应的水化物与其简单气态氢化物反应的生成物的化学式___________ 。
⑸③元素与⑩元素两者核电荷数之差是______________ 。
⑹为探究元素性质的递变规律,某化学兴趣小组将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由。______ ;_______________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
⑴表中给出的化学性质最不活泼的元素,其原子结构示意图为
⑵表中能形成两性氢氧化物的元素是
⑶用电子式表示④元素与⑦元素形成化合物的过程
⑷写出②的最高价氧化物对应的水化物与其简单气态氢化物反应的生成物的化学式
⑸③元素与⑩元素两者核电荷数之差是
⑹为探究元素性质的递变规律,某化学兴趣小组将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】比较下列离子半径大小
(1)r(Cl-)______ r(Cl),r(Fe)_______ r(Fe2+)________ r(Fe3+)
(2)r(O2-)________ r(F-)________ r(Na+)_______ r(Mg2+)________ r(Al3+)
(3)r(Li+)______ r(Na+)_______ r(K+)______ r(Rb+)______ r(Cs+),r(O2-)_______ r(S2-)________ r(Se2-)________ r(Te2-)
(4)r(K+)_______ r(Na+)________ r(Mg2+)
(5)总结离子半径大小判断的方法___________
(1)r(Cl-)
(2)r(O2-)
(3)r(Li+)
(4)r(K+)
(5)总结离子半径大小判断的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增。已知:B原子有3个能级且各能级电子数相等;D原子最外能层P能级上有2个未成对电子,E是同周期元素中第一电离能最小的元素;F是同周期元素中原子半径最小的元素;A是非金属元素,且A、C、F可形成离子化合物。请回答:
(1)A、D形成的三原子分子中心原子杂化类型是______ ,分子空间构型为_____ 。
(2)B、C、D的简单氢化物稳定性由强到弱的顺序为___________ (用化学用语回答,下同),B、C、F最高价含氧酸酸性由强到弱的顺序为_________ ,B、C、D、E第一电离能由小到大的顺序为___ ;
(3)元素A、D、E形成的化合物电子式为_________ ,其中含有的化学键类型有________ 。
(4)C的氢化物极易溶于D的常见氢化物,列出所有可能的原因_________________________
(1)A、D形成的三原子分子中心原子杂化类型是
(2)B、C、D的简单氢化物稳定性由强到弱的顺序为
(3)元素A、D、E形成的化合物电子式为
(4)C的氢化物极易溶于D的常见氢化物,列出所有可能的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有第ⅥA族和几种元素的位置。请回答下列问题:

(1)铁元素位于元素周期表中第四周期__________ 族。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是氢原子的最外层电子“饱和缺一”。请写出LiH的电子式_____________ ,而且Li+的离子半径比H-_______ (填“大”或“小”)。
(3)d的某化合物呈淡黄色,可与硫酸亚铁溶液反应生成红褐色沉淀和能使带火星的木条复燃的气体,d的该化合物中含有的化学键类型为__________________ 。
(4)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带______ (填“正”或“负”) 电荷。
(5)下列叙述正确的是______
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.氢化物的酸性:f弱于g

(1)铁元素位于元素周期表中第四周期
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,理由是氢原子的最外层电子“饱和缺一”。请写出LiH的电子式
(3)d的某化合物呈淡黄色,可与硫酸亚铁溶液反应生成红褐色沉淀和能使带火星的木条复燃的气体,d的该化合物中含有的化学键类型为
(4)b元素的氢化物与其最高价氧化物的水化物可生成一种盐,土壤中施用该盐做化肥时,其阴离子在水田中的利用率低,说明土壤胶体粒子带
(5)下列叙述正确的是
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>a
E.氢化物的酸性:f弱于g
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
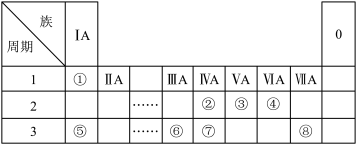
(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是___________ (填化学式),③的基态原子核外电子的运动状态有___________ 种。
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是___________ (填离子符号)。②③④三种元素中第一电离能最大的是___________ (填元素符号)
(3)单质④有两种同素异形体,其中沸点高的是___________ (填化学式),原因是___________ ;④和⑤的氢化物所属的晶体类型分别为___________ 和___________ 。

(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是
(3)单质④有两种同素异形体,其中沸点高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锶(Sr)位于元素周期表的第5周期IIA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是______ 。非金属性最强的是______ 。
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式______ ,该分子为______ (选填“极性”、“非极性”)分子。
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号______ 。写出锶原子的最外层电子排布式______ 。下列关于锶及其化合物的叙述中,错误的是______ 。
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因______ 。
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。
(5)常温下Al的金属性比Ba的金属性______ (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是______ 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO
 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。(5)常温下Al的金属性比Ba的金属性
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】含过渡金属元素的物质种类繁多,应用广泛。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。基态铁原子的简化电子排布式为
是一种常用的补铁剂。基态铁原子的简化电子排布式为___________ ,基态 核外电子的空间运动状态有
核外电子的空间运动状态有___________ 种。
(2) 电极材料被用于生产各种锂离子电池。
电极材料被用于生产各种锂离子电池。 中所含短周期非金属元素的原子半径由大到小的顺序是
中所含短周期非金属元素的原子半径由大到小的顺序是___________ ,下列Li原子轨道表示式表示的状态中,能量最低和最高的分别为___________ 、___________ (填字母)。
A.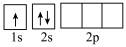 B.
B. C.
C. D.
D.
(3)铜、锌两种元素的第一电离能、第二电离能如表所示。元素1的元素符号为___________ ,元素2在周期表中位于第四周期第___________ 族。用 表示元素的第n电离能,则图中的a、b、c分别代表
表示元素的第n电离能,则图中的a、b、c分别代表___________ (填字母)。

A.a为 、b为
、b为 、c为
、c为 B.a为
B.a为 、b为
、b为 、c为
、c为
C.a为 、b为
、b为 、c为
、c为 D.a为
D.a为 、b为
、b为 、c为
、c为
(1)乳酸亚铁
 是一种常用的补铁剂。基态铁原子的简化电子排布式为
是一种常用的补铁剂。基态铁原子的简化电子排布式为 核外电子的空间运动状态有
核外电子的空间运动状态有(2)
 电极材料被用于生产各种锂离子电池。
电极材料被用于生产各种锂离子电池。 中所含短周期非金属元素的原子半径由大到小的顺序是
中所含短周期非金属元素的原子半径由大到小的顺序是A.
 B.
B. C.
C. D.
D.
(3)铜、锌两种元素的第一电离能、第二电离能如表所示。元素1的元素符号为
 表示元素的第n电离能,则图中的a、b、c分别代表
表示元素的第n电离能,则图中的a、b、c分别代表| 电离能/(kJ/mol) |  |  |
| 元素1 | 906 | 1733 |
| 元素2 | 746 | 1958 |

A.a为
 、b为
、b为 、c为
、c为 B.a为
B.a为 、b为
、b为 、c为
、c为
C.a为
 、b为
、b为 、c为
、c为 D.a为
D.a为 、b为
、b为 、c为
、c为
您最近一年使用:0次



