下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
2021高一·全国·专题练习 查看更多[4]
(已下线)专题4.2.1 元素性质的周期性变化规律(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题
更新时间:2021-12-06 14:23:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表短周期的一部分

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是___________ 。
(2)表中元素⑥的原子结构示意图为___________ 。
(3)④与⑤形成的化合物的化学键类型为_______ ,该化合物的电子式为____________ 。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式,下同);④所在主族的前四种元素的单质分别与氢气化合形成的气态氢化物的稳定性由强到弱的顺序是_________ 。
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为___________________ 。

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是
(2)表中元素⑥的原子结构示意图为
(3)④与⑤形成的化合物的化学键类型为
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
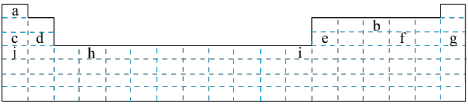
(2)f元素位于第
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
| A.比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e |
| B.比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j<c<d<e |
| C.比较四种元素形成的单质分别与非氧化性酸反应置换氢气的剧烈程度:c>j>d>e |
| D.将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
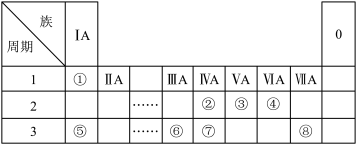
(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是___________ (填化学式),③的基态原子核外电子的运动状态有___________ 种。
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是___________ (填离子符号)。②③④三种元素中第一电离能最大的是___________ (填元素符号)
(3)单质④有两种同素异形体,其中沸点高的是___________ (填化学式),原因是___________ ;④和⑤的氢化物所属的晶体类型分别为___________ 和___________ 。

(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是
(3)单质④有两种同素异形体,其中沸点高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4)反应的产物,以其产物为原料制备氯气:室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。分析实验并回答相应问题。
(1)M的化学式是_____ ,组成草酸的三种元素中,非金属性最强的是_____ (填元素符号)。
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为_____ ,向滤液中加入盐酸时又产生无色无味气体,该反应的离子方程式为______ 。
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是_____ 。
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为_____ 。
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:______ 。
(1)M的化学式是
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是________ ,碱性最强的化合物的电子式是____________ ,其含有的化学键类型___________
(3)最高价氧化物是两性氧化物的元素是________ ;写出它的氧化物与盐酸反应的离子方程式_________________________________________
(4)写出元素③的氢化物的电子式______________
(5)写出④的单质与水反应的离子方程式________________________________________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)写出元素③的氢化物的电子式
(5)写出④的单质与水反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空:
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子__________ ;(用元素符号表示)
(2)写电子式:HClO:____ ;NH4+:_____ ;写结构式:CCl4:_____ ;CS2:_____ ;
(3)画出钙原子的原子结构示意图:____ ;画出溴离子的离子结构示意图:____ ;
(4)用电子式表示氯化钠的形成过程:_________________________
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;______________
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;______________
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子
(2)写电子式:HClO:
(3)画出钙原子的原子结构示意图:
(4)用电子式表示氯化钠的形成过程:
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】观察下列表格,回答相关问题:
(1)其中属于离子化合物的物质有___________ 。
(2)试比较F-、Cl-、Br-的离子半径大小___________ (用元素符号表示);推测离子半径与离子晶体熔点的关系___________ ;猜想KCl的熔点___________ (高于/低于)NaCl的熔点。
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为___________ g(保留2位小数)。
| 物质 | NaF | NaCl | NaBr | KCl | AlCl3 | CH4 | CCl4 |
| 熔点/℃ | 995 | 801 | 755 | 190 | -182.5 | -23 |
(2)试比较F-、Cl-、Br-的离子半径大小
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是______ 个;
O2—、Na+、Cl—中半径最小的是_____________ 。
(2)NaCN晶体中含有的化学键类型为_____________________________ 。
(3)第二段过程中,产物属于双原子分子的结构式是___________ ,该物质一般要比其他共价化合物如:NH3、H2S等都要稳定,其原因为:___________________ ;写出该物质的一种用途:____________________ 。
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是
O2—、Na+、Cl—中半径最小的是
(2)NaCN晶体中含有的化学键类型为
(3)第二段过程中,产物属于双原子分子的结构式是
您最近一年使用:0次



