结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
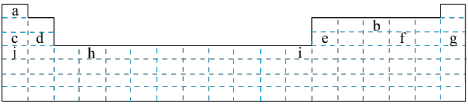
(2)f元素位于第
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
| A.比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e |
| B.比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j<c<d<e |
| C.比较四种元素形成的单质分别与非氧化性酸反应置换氢气的剧烈程度:c>j>d>e |
| D.将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e |
更新时间:2024-04-11 16:39:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】一氯化碘(ICl)是一种卤素互化物,与卤素单质性质相似,可用于制农药等。
(1)Cl在元素周期表中位于第三周期、第_______ 族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为_______ 价。
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,_______ ,得电子能力Cl强于I。
(4)下列推断中,正确的是_______ (填字母)。
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
(1)Cl在元素周期表中位于第三周期、第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,
(4)下列推断中,正确的是
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,根据表中的①~⑩种元素,按要求填写下列空白:
(1)在这些元素中,化学性质最不活泼元素的原子结构示意图为___________ 。
(2)①用于考古的一种核素符号为___________ 。①和⑦简单氢化物稳定性较差的是___________ (填化学式)。
(3)元素②和⑥对应的离子半径较小的是___________ (填离子符号)。⑤和⑧最高价氧化物对应水化物酸性较强的是___________ (填化学式)。④和⑥最高价氧化物对应水化物碱性较弱的是___________ (填化学式)。
(4)写出②与④形成原子个数为1:2的化合物的电子式___________ 。
(5)下列关于⑩元素硒(Se)说法推断正确的是___________(填标号)。
(6)④和⑥最高价氧化物对应水化物相互反应的离子方程式为___________ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ④ | ⑥ | ⑦ | ⑤ | ⑧ | ⑨ | ||
| 4 | ③ | ⑩ |
(2)①用于考古的一种核素符号为
(3)元素②和⑥对应的离子半径较小的是
(4)写出②与④形成原子个数为1:2的化合物的电子式
(5)下列关于⑩元素硒(Se)说法推断正确的是___________(填标号)。
A. 属于共价化合物,只具有还原性 属于共价化合物,只具有还原性 |
B.Se的最低负化合价是负2价;但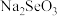 中Se化合价为+4 中Se化合价为+4 |
| C.Se元素非金属性比⑤强 |
| D.Se元素原子半径小于③ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85.根据材料完成下列问题:
(1)铷Rb37位于周期表的第___________ 周期,第___________ 族。
(2)关于铷的结构和性质判断正确的是________ 。
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤ C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是________ 。
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是_________ 。
A.Li B.Na C.K D.Cs
(1)铷Rb37位于周期表的第
(2)关于铷的结构和性质判断正确的是
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤ C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是
A.Li B.Na C.K D.Cs
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,根据A~H在元素周期表中的位置,用元素符号或化学式回答下列问题:
(1)上表中,元素金属性最强的是________ (填元素符号)。
(2)写出D的原子结构示意图:__________
(3)B与C的原子半径比较:B________ C (填“>”或“<”)。G与H的非金属性比较:G ________ H(填“>”或“<”)。
(4)A与H形成化合物的电子式:_______
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | F | H |
(1)上表中,元素金属性最强的是
(2)写出D的原子结构示意图:
(3)B与C的原子半径比较:B
(4)A与H形成化合物的电子式:
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)默写化学元素周期表前20号元素。___________
(2)默写金属金属活动性顺序。__________
(1)默写化学元素周期表前20号元素。
(2)默写金属金属活动性顺序。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为
(2)由A、W元素组成的18电子微粒的分子式为
(3)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式
(4)向含有Fe2+和淀粉KI的溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成。当消耗2mol I-时,共转移3mol电子,该反应的离子方程式是
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,A-具有与He相同的电子层结构,DA能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律是指导学生学好元素及其化合物知识的理论工具,回答下列问题。
(1)最活泼的非金属元素是_____ (填元素符号);短周期元素中共有____ 种金属元素。
(2)硫元素在元素周期表中的位置为________ 。
(3)用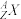 形式表示出中子数为10 的氧原子
形式表示出中子数为10 的氧原子________ 。
(4) 下表为元素周期表的一部分,请参照元素①~ ⑦在表中的位置,用化学用语回答下列问题:

则①、②、⑥的最高价氧化物对应的水化物的酸性由强到弱的顺序是______ (用化学式表示), ③形成的简单氢化物的结构式为_______ ,⑦的最高价氧化物的化学式_______ ,③与④形成的含有两种化学键物质的电子式为________ ,④、⑤两种元素的最高价氧化物对应水化物之间可发生反应,对应离子方程式为___________________ 。
(1)最活泼的非金属元素是
(2)硫元素在元素周期表中的位置为
(3)用
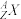 形式表示出中子数为10 的氧原子
形式表示出中子数为10 的氧原子(4) 下表为元素周期表的一部分,请参照元素①~ ⑦在表中的位置,用化学用语回答下列问题:

则①、②、⑥的最高价氧化物对应的水化物的酸性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,表中的每个编号代表一种短周期元素,回答下列问题:
(1)①和③两种元素形成化合物的电子式为___________ 。
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为___________ (用化学式表示)。
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为___________ 。
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为___________ 。
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和③两种元素形成化合物的电子式为
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ________ ;
(2)表中能形成两性氢氧化物的元素是________ (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式:_________ ;
(3)③⑦⑩三种元素的阴离子还原性顺序为:___________________ ;⑦的水溶液呈__________ 色;
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式) ;
(5)③元素与⑩元素两者核电荷数之差是____________ ;
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
| 周期 主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氢氧化物的元素是
(3)③⑦⑩三种元素的阴离子还原性顺序为:
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是
(5)③元素与⑩元素两者核电荷数之差是
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
| 实验步骤 | 实验现象与结论 |
| |
您最近一年使用:0次



