氮族元素是指元素周期表中VA族的所有元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)等元素,在农药、化肥等领域有广泛应用。回答下列问题:
(1)基态Bi的价电子排布图为_______ 。
(2)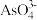 中和
中和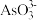 中
中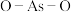 键角较大的是
键角较大的是_______ 。
(3)氮元素的常见含氧酸根为 ,其空间构型为
,其空间构型为_______ 。
(4) 和
和 可形成配离子
可形成配离子 ,该配离子中各元素的第一电离能由小到大的顺序为
,该配离子中各元素的第一电离能由小到大的顺序为_______ (用元素符号表示)。
(1)基态Bi的价电子排布图为
(2)
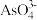 中和
中和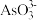 中
中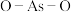 键角较大的是
键角较大的是(3)氮元素的常见含氧酸根为
 ,其空间构型为
,其空间构型为(4)
 和
和 可形成配离子
可形成配离子 ,该配离子中各元素的第一电离能由小到大的顺序为
,该配离子中各元素的第一电离能由小到大的顺序为
更新时间:2022-06-30 20:49:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)镁元素基态原子核外M层电子的自旋状态______ (填“相同”或“相反”)。
(2)基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(3)基态K原子中,核外电子占据最高能层的符号是______ ,占据该能层电子的电子云轮廓图形状为______ 。
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用______ 形象化描述。在基态 原子中,核外存在
原子中,核外存在______ 对自旋相反的电子。
(5)铝原子核外电子云有______ 种不同的伸展方向,有______ 种不同运动状态的电子。
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)基态K原子中,核外电子占据最高能层的符号是
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
 原子中,核外存在
原子中,核外存在(5)铝原子核外电子云有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为__________ ;Y元素原子最外层电子的电子排布图为__________ 。
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为__________ (填“共价键”或“离子键”)。
(3)该化合物的立体构型为__________ ,中心原子的杂化类型为__________ ,分子为__________ (填“极性分子”或“非极性分子”)。
(1)X元素的原子基态时电子排布式为
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为
(3)该化合物的立体构型为
您最近一年使用:0次
【推荐1】回答下列问题
(1)基态 的外围电子排布式是
的外围电子排布式是_______ 。
(2)三草酸合铁酸钾可用氯化铁与草酸钾混合直接合成: ;上述反应涉及的主族元素中,第一电离能最小的是
;上述反应涉及的主族元素中,第一电离能最小的是_______ (填元素符号)。
(3)1mol异氰酸苯酯分子中含有 键数目为
键数目为_______ 。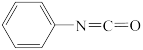 (异氰酸苯酯)
(异氰酸苯酯)
(4)写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_______ 。
(5)H2O与 可以任意比例互溶,主要因为
可以任意比例互溶,主要因为_______ 。
(1)基态
 的外围电子排布式是
的外围电子排布式是(2)三草酸合铁酸钾可用氯化铁与草酸钾混合直接合成:
 ;上述反应涉及的主族元素中,第一电离能最小的是
;上述反应涉及的主族元素中,第一电离能最小的是(3)1mol异氰酸苯酯分子中含有
 键数目为
键数目为 (异氰酸苯酯)
(异氰酸苯酯)(4)写出一种与
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(5)H2O与
 可以任意比例互溶,主要因为
可以任意比例互溶,主要因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某元素的激发态原子的电子排布式为1s22s22p63s23p34s1,则该元素基态原子的电子排布式为____________ ;元素符号为________ ;其最高价氧化物对应的水化物的化学式是________ 。
您最近一年使用:0次
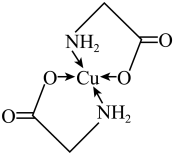
【推荐3】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:___________ 区。在第___________ 周期
(2)基态二价铜离子的电子排布式为___________ ,已知高温下 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释
(3)硼核外电子的运动状态的概率密度分布可用___________ 形象化描述。
(4) 的价电子排布图为
的价电子排布图为___________ 。
(5)N、O、Se三种元素中的第一电离能最大的为:___________ ,电负性最大的是___________ 。
(2)基态二价铜离子的电子排布式为
 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释(3)硼核外电子的运动状态的概率密度分布可用
(4)
 的价电子排布图为
的价电子排布图为(5)N、O、Se三种元素中的第一电离能最大的为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如何用杂化轨道理论解释 分子的空间结构
分子的空间结构_____ ?
 分子的空间结构
分子的空间结构
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氟及其化合物的用途十分广泛。回答下列问题:
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电。
①CuF的熔点比CuCl的高,原因是_______ 。
②已知Cu、Zn的第二电离能分别为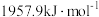 、
、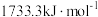 ,前者高于后者的原因是
,前者高于后者的原因是_______ 。
(2)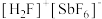 (氟锑酸,是一种超强酸),其中阳离子
(氟锑酸,是一种超强酸),其中阳离子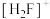 的空间构型为
的空间构型为_______ 。
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电。
①CuF的熔点比CuCl的高,原因是
②已知Cu、Zn的第二电离能分别为
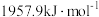 、
、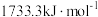 ,前者高于后者的原因是
,前者高于后者的原因是(2)
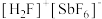 (氟锑酸,是一种超强酸),其中阳离子
(氟锑酸,是一种超强酸),其中阳离子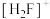 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】三氟化氮(NF3)是一种无色、无臭的气体。三氟化氮在一定条件下与水蒸气能发生氧化还原反应,反应产物中生成酸 X、酸 Y 和一种无色气体(遇空气变成红棕色),其中酸X 是一种弱酸,酸Y 为常见的含氧强酸。
(1)NF3的空间构型为__________ 。
(2)酸X是弱酸(难电离)的可能原因是______ 。
(3)工业上通过 NH3和氟气(F2)反应制备 NF3,请结合题给信息,判断NF3主要表现出来的化学性质是_______ 。
(4)NF3的一种下游产品三聚氟氰(分子式为:C3N3F3),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式________ 。
(1)NF3的空间构型为
(2)酸X是弱酸(难电离)的可能原因是
(3)工业上通过 NH3和氟气(F2)反应制备 NF3,请结合题给信息,判断NF3主要表现出来的化学性质是
(4)NF3的一种下游产品三聚氟氰(分子式为:C3N3F3),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
您最近一年使用:0次



