超分子化学在识别、催化、传输等功能方面已迅速渗透到各学科领域。如图是一种由两个相同分子(a)组装形成的分子盒(b)。请回答:
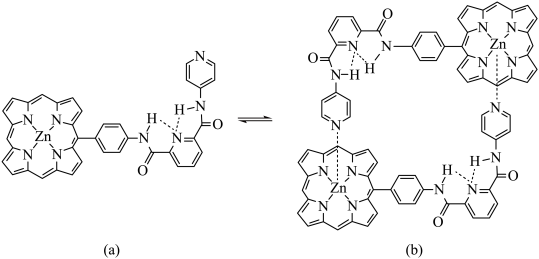
(1)两分子(a)通过______ 结合成(b)。
(2)(a)分子中C原子的杂化方式为______ ,基态Zn的价层电子轨道表示式为______ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为_____ 。

(1)两分子(a)通过
| A.离子键 | B.配位键 | C.氢键 | D.分子间作用力 |
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态O原子,其核外电子自旋磁量子数的代数和为
更新时间:2023-04-30 22:31:59
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小 的,其核外电子排布式为______ ,价电子构型为______ ,属________ 区元素。
(2)某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,最高正化合价为________ ,元素符号是________ 。
(3)原子序数为24的元素原子中有________ 个电子层,________ 个能级,________ 个未成对电子。
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)________________ 。
(2)某元素原子的价电子构型为4s24p1,它属于第
(3)原子序数为24的元素原子中有
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁粉可用于处理水中污染物。铁粉的氧化物层可以导电。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下600℃高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:___________ 。
(2)采朗NaBH4溶液还原铁盐,可以制备纳米级的铁粉,并生成H2。
①写出Cu2+的外围电子轨道表示式___________ 。
②NaBH4中 离子的空间构型为
离子的空间构型为___________ 。
③由Fe3+每生成1molFe,需要NaBH4物质的量是___________ mol。
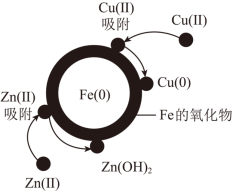
(3)利用纳米铁粉可以有效处理废水中的Cu2+和Zn2+去除机理如下图所示,纳米铁粉去除污水中Cu2+和Zn2+机理不同,请解释原因并简述两者的区别___________ 。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下600℃高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:
(2)采朗NaBH4溶液还原铁盐,可以制备纳米级的铁粉,并生成H2。
①写出Cu2+的外围电子轨道表示式
②NaBH4中
 离子的空间构型为
离子的空间构型为③由Fe3+每生成1molFe,需要NaBH4物质的量是
(3)利用纳米铁粉可以有效处理废水中的Cu2+和Zn2+去除机理如下图所示,纳米铁粉去除污水中Cu2+和Zn2+机理不同,请解释原因并简述两者的区别

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】法匹拉韦是治疗新冠肺炎的一种药物,结构简式如图。回答下列问题:

(1)该药物的组成元素中,电负性最大的是_____________ (填元素符号)。
(2)与羟基相连的碳原子采用的杂化轨道类型为_____________ 。
(3)分子内氮氢原子间形成_____________ 键(填“极性”或“非极性”)。
(4)组成该药物的元素所形成的最简单氢化物中,分子立体构型为V形的是_____________ (填化学式),沸点最低的是_____________ (填化学式)。

(1)该药物的组成元素中,电负性最大的是
(2)与羟基相连的碳原子采用的杂化轨道类型为
(3)分子内氮氢原子间形成
(4)组成该药物的元素所形成的最简单氢化物中,分子立体构型为V形的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)在BF3分子中,F−B−F的键角是________ ,B原子的杂化轨道类型为________ ,BF3和过量NaF作用可生成NaBF4, 的立体构型为
的立体构型为________ 。
(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体分子__________ ,三角锥形分子__________ ,V型分子__________ 。
(3)已知白磷(P4)的结构为 ,可知每个磷原子以
,可知每个磷原子以___ 个共价键与另外的___ 磷原子结合成正四面体结构,它应该是________ 分子(填“极性”或“非极性”),在CS2中______ (填“能”或“不能”)溶解,P原子的杂化方式为______________ 。
(1)在BF3分子中,F−B−F的键角是
 的立体构型为
的立体构型为(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体分子
(3)已知白磷(P4)的结构为
 ,可知每个磷原子以
,可知每个磷原子以
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】查阅有关氯化铝的一些资料,得到如下一些信息:①将氯化铝加热,在180℃时开始升华;②在2.02×105Pa条件下,氯化铝的熔点为190℃;③在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g/L;④氯化铝的结构中含有配位键。
请回答下列问题:
(1)请你就氯化铝是“离子化合物”还是“共价化合物”提出一种猜想,并写出一条猜想的理由。你的猜想是_______ ,理由是_______ 。
(2)通过计算确定氯化铝的化学式为_______ ,结构式为_______ 。
(3)用无水氯化铝进行实验时,发现它在潮湿空气中强烈地“发烟”。进一步查阅资表明,其原因是氯化铝与空气中的水发生了复分解反应。请写出反应的化学方程式_______ 。
(4)请你设计一实验方案,证明氯化铝是“离子化合物”还是“共价化合物”。写出实验内容、现象和结论_______ 。
请回答下列问题:
(1)请你就氯化铝是“离子化合物”还是“共价化合物”提出一种猜想,并写出一条猜想的理由。你的猜想是
(2)通过计算确定氯化铝的化学式为
(3)用无水氯化铝进行实验时,发现它在潮湿空气中强烈地“发烟”。进一步查阅资表明,其原因是氯化铝与空气中的水发生了复分解反应。请写出反应的化学方程式
(4)请你设计一实验方案,证明氯化铝是“离子化合物”还是“共价化合物”。写出实验内容、现象和结论
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)四种晶体的熔点数据如表:
互为同分异构体的硝基化合物与氨基酸,前者熔点低于后者的主要原因是____ 。
(2)用质谱仪检测氯化铝时,谱图中出现质荷比(相对分子质量)为267的峰,原因是____ 。
(1)四种晶体的熔点数据如表:
| 物质 | CH3CH2NO2 | CH3CH2CH2NO2 | H2NCH2COOH | H2NCH(CH3)COOH |
| 熔点/℃ | -90 | -108 | 240 | 314 |
互为同分异构体的硝基化合物与氨基酸,前者熔点低于后者的主要原因是
(2)用质谱仪检测氯化铝时,谱图中出现质荷比(相对分子质量)为267的峰,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
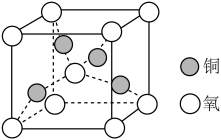
【推荐3】铜是人类最早使用的金属之一,最近科学家发现Cu元素有很强的杀菌作用,还可代替Al布线在硅芯片上。用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下: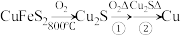
回答下列问题:
(1)基态Cu原子的价层电子排布式为_______ 。Cu2O的熔点 ________ Cu2S的熔点(填写“<”、“>”或“=”)。
(2)反应①、②中生成的气体SO2,分子的空间结构为_______ 。
(3)Cu2+能与NH3形成配位数为4的配合物,向CuSO4溶液中加入氨水,最终形成配合物[Cu(NH3)4]SO4。请判断:[Cu(NH3)4]SO4。中存在的化学键的类型有_________ (填序号)。
a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为__________ ,每个O原子周围与它最近且等距离的Cu原子有________ 个,每个Cu原子周围与它最近且等距离的O原子有_______ 个。
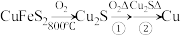
回答下列问题:
(1)基态Cu原子的价层电子排布式为
(2)反应①、②中生成的气体SO2,分子的空间结构为
(3)Cu2+能与NH3形成配位数为4的配合物,向CuSO4溶液中加入氨水,最终形成配合物[Cu(NH3)4]SO4。请判断:[Cu(NH3)4]SO4。中存在的化学键的类型有
a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为
您最近一年使用:0次

 外围电子的轨道表示式
外围电子的轨道表示式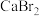 电子式
电子式 分子中所有原子均满足8电子构型,则其结构式为
分子中所有原子均满足8电子构型,则其结构式为 分子的空间结构为
分子的空间结构为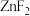 的晶体类型为
的晶体类型为 微粒间的作用力为
微粒间的作用力为