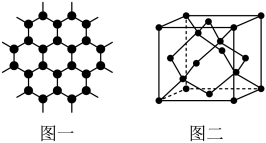
法匹拉韦是治疗新冠肺炎的一种药物,结构简式如图。回答下列问题:

(1)该药物的组成元素中,电负性最大的是_____________ (填元素符号)。
(2)与羟基相连的碳原子采用的杂化轨道类型为_____________ 。
(3)分子内氮氢原子间形成_____________ 键(填“极性”或“非极性”)。
(4)组成该药物的元素所形成的最简单氢化物中,分子立体构型为V形的是_____________ (填化学式),沸点最低的是_____________ (填化学式)。

(1)该药物的组成元素中,电负性最大的是
(2)与羟基相连的碳原子采用的杂化轨道类型为
(3)分子内氮氢原子间形成
(4)组成该药物的元素所形成的最简单氢化物中,分子立体构型为V形的是
更新时间:2023-01-10 14:52:26
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请查阅化合物HCl、NO、MgO、KCl中元素的电负性数值,判断_______ 是离子化合物,_______ 是共价化合物。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据下列表格,回答有关问题:

(1)上表中,第一电离能最小的元素是____ (填元素名称,下同),电负性最大的元素是___
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是_____ (填化学式,下同),碱性最强的是_____ 。
(3)某元素最高价氧化物对应的水化物呈两性,则该元素是_____ (填对应的字母),该元素与c元素形成的化合物能否与NaOH溶液反应(若能,写出相应的离子方程式;若不能,则填“否”)________ 。
(4)在e~k元素的原子中,原子半径最小的是_____ (填元素符号),其价电子排布式为______ ;未成对电子数最多的是____ (填元素符号),其最高价氧化物对应水化物的化学式为_____ ;有两个未成对电子的元素是________ (填元素符号);M层有两个空轨道的是____ (填元素符号),其阳离子结构示意图为____ 。

(1)上表中,第一电离能最小的元素是
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(3)某元素最高价氧化物对应的水化物呈两性,则该元素是
(4)在e~k元素的原子中,原子半径最小的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)写出铜原子价电子排布式:______ 。与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有________ (填元素符号)。
(2)第三周期第一电离能处于Al和P之间的元素有______ 种。
(3)某种原子的结构示意图为 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为______ 。
(4)Cr在周期表中位于_____ 周期___ 族,属于___ 区,价电子排布图为______
(5)ClO4-互为等电子体的分子或离子为____ 。
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_____ 。
(2)第三周期第一电离能处于Al和P之间的元素有
(3)某种原子的结构示意图为
 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为(4)Cr在周期表中位于
(5)ClO4-互为等电子体的分子或离子为
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】N、P、As及其化合物在生产生活方面都有重要的用途。回答下列问题:
(1)As原子的基态核外电子排布式为___________ 。
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是___________ 。顺铂在水中溶解度较大,反铂在水中溶解度小,顺铂在水中溶解度较大的原因是___________ 。
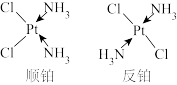
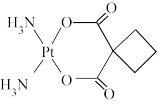
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为___________ 。
(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为___________ (用文字描述),该反应的化学方程式为___________ 。

(1)As原子的基态核外电子排布式为
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是
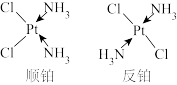
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为

(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】水是自然界中普遍存在的一种重要物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为____________ 。
(2)已知2H2O H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是____________ ,中心原子的杂化类型是___________ 。
(3)下列关于水的说法正确的是__________ (选填序号)。
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:___________________ 沸点:___________________
(1)氧原子基态时价层电子的电子排布图为
(2)已知2H2O
 H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是(3)下列关于水的说法正确的是
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为________ 。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因________________ 。
(3)H2Se分子的键角_______ H2O分子的键角(选填“>”、“=”或“<”)。写出与SeO3互为等电子体的一种阴离子_____________ (写化学式)。
(4) AsF3分子的立体构型为__________ ;AsF3是极性分子,理由是_________________ 。
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有__________________ 。
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:
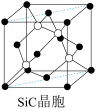
金刚砂中硅原子的杂化轨道类型为_______ ,沿晶胞图中虚线方向的切面图为__________ (填标号)。

(1)基态Ga原子的电子排布式为
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因
(3)H2Se分子的键角
(4) AsF3分子的立体构型为
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:

金刚砂中硅原子的杂化轨道类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图:

(1)A分子中采取sp2杂化的碳原子数目是___ 。
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___ 。
①分子中不同化学环境的氢原子个数比是2:2:2:1。
②苯环上有4个取代基,且有两种含氧官能团。

(1)A分子中采取sp2杂化的碳原子数目是
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①分子中不同化学环境的氢原子个数比是2:2:2:1。
②苯环上有4个取代基,且有两种含氧官能团。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯吡苯脲是一种常用的膨大剂,其结构简式为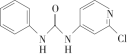 ,它是经国家批准使用的植物生长调节剂。请回答下列问题:
,它是经国家批准使用的植物生长调节剂。请回答下列问题:
(1)基态氯原子核外未成对电子数为_______ 。
(2)氯吡苯脲分子中,氮原子的杂化类型为_______ ,碳原子的杂化类型为_______ ,该分子_______ (填“是”或“不是”)手性分子。
(3)查阅文献知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
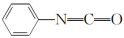 +
+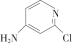 ―→
―→
反应过程中,每生成1mol氯吡苯脲,断裂_______ 个σ键、_______ 个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O比NH3稳定的原因:_______ 。
②CO2的水溶液中含有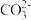 ,则该阴离子的VSEPR模型名称为
,则该阴离子的VSEPR模型名称为_______ ,中心原子的杂化类型为_______ 。
 ,它是经国家批准使用的植物生长调节剂。请回答下列问题:
,它是经国家批准使用的植物生长调节剂。请回答下列问题:(1)基态氯原子核外未成对电子数为
(2)氯吡苯脲分子中,氮原子的杂化类型为
(3)查阅文献知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
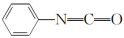 +
+ ―→
―→
反应过程中,每生成1mol氯吡苯脲,断裂
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O比NH3稳定的原因:
②CO2的水溶液中含有
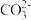 ,则该阴离子的VSEPR模型名称为
,则该阴离子的VSEPR模型名称为
您最近一年使用:0次

 =1.732)
=1.732)