(1)写出铜原子价电子排布式:______ 。与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有________ (填元素符号)。
(2)第三周期第一电离能处于Al和P之间的元素有______ 种。
(3)某种原子的结构示意图为 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为______ 。
(4)Cr在周期表中位于_____ 周期___ 族,属于___ 区,价电子排布图为______
(5)ClO4-互为等电子体的分子或离子为____ 。
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_____ 。
(2)第三周期第一电离能处于Al和P之间的元素有
(3)某种原子的结构示意图为
 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为(4)Cr在周期表中位于
(5)ClO4-互为等电子体的分子或离子为
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为
更新时间:2019-05-24 10:35:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)简化的氯离子的电子排布式:___________ ,P原子的价层电子轨道表示式:___________ ,基态Cu原子的电子排布式为:___________
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ 。
(3)PO 离子的空间构型为
离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
(1)简化的氯离子的电子排布式:
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)PO
 离子的空间构型为
离子的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷是生物体内不可或缺的元素之一,自然界主要以磷酸盐的形式存在。磷酸盐可用于制备白磷(P4),白磷在加热条件下,能转化为红磷(P),白磷还能与足量热的浓碱发生如下反应:P4+3KOH+3H2O PH3↑+3KH2PO2。
PH3↑+3KH2PO2。
(1)磷原子的最外层核外电子排布式为______ 。
(2)PH3的电子式为______ 。热稳定性:NH3______ PH3(选填“>”或“<”)。
(3)P4的分子构型为正四面体,P4为______ 分子(选填“极性”或“非极性”)。
(4)白磷和红磷互为______ 。
(5)利用磷酸钙矿混以石英砂(SiO2)和炭粉在电炉中加热可以制备白磷。
______Ca3(PO4)2+______SiO2+______C ______CaSiO3+______P4+______CO↑
______CaSiO3+______P4+______CO↑
配平上述化学方程式______ 。
(6)次磷酸(H3PO2)是______ 弱酸(选填“一元”、“二元”或“三元”)。KH2PO2稀溶液中存在:c(K+)=______ 。
 PH3↑+3KH2PO2。
PH3↑+3KH2PO2。(1)磷原子的最外层核外电子排布式为
(2)PH3的电子式为
(3)P4的分子构型为正四面体,P4为
(4)白磷和红磷互为
(5)利用磷酸钙矿混以石英砂(SiO2)和炭粉在电炉中加热可以制备白磷。
______Ca3(PO4)2+______SiO2+______C
 ______CaSiO3+______P4+______CO↑
______CaSiO3+______P4+______CO↑配平上述化学方程式
(6)次磷酸(H3PO2)是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳、氮、氧、氟、硫是中学常见的非金属元素,铁离子可与由这几种元素组成的SCN-、CN-、F-等形成很多配合物。
(1)基态Fe原子中,电子占据的最高电子层符号为__ ,该电子层具有的原子轨道数为__ 。
(2)已知(CN)2是直线形分子,并有对称性,则(CN)2中π键和σ键的个数比为__ ;在配合物[Fe(SCN)]2+中,提供空轨道接受孤对电子的微粒是__ 。
(3)配合物K4[Fe(CN)6]中不存在的作用力是__ (填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
(4)写出一种与SCN-互为等电子体的分子__ (用化学式表示),该分子的空间构型为__ 。
(5)已知乙烯酮(CH2=C=O)是一种重要的有机中间体,可由CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子的杂化轨道类型是__ 。1mol(C2H5O)3P=O分子中含有的σ键的物质的量为__ 。
(1)基态Fe原子中,电子占据的最高电子层符号为
(2)已知(CN)2是直线形分子,并有对称性,则(CN)2中π键和σ键的个数比为
(3)配合物K4[Fe(CN)6]中不存在的作用力是
A.极性键 B.离子键 C.非极性键 D.配位键
(4)写出一种与SCN-互为等电子体的分子
(5)已知乙烯酮(CH2=C=O)是一种重要的有机中间体,可由CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子的杂化轨道类型是
您最近一年使用:0次
【推荐1】火药的爆炸反应原理为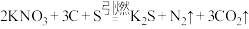 。请回答下列问题:
。请回答下列问题:
(1)基态 原子核外有
原子核外有___________ 种空间运动状态的电子。
(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为_______ 。
(3)基态钾离子的电子占据的最高能层符号是___________ ; 与
与 具有相同的核外电子排布,
具有相同的核外电子排布,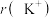 小于
小于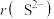 ,原因是
,原因是___________ 。
(4)元素的气态基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能( )。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
)。MgO的Born-Haber循环(原理为盖斯定律)如图所示。

由图可知,Mg原子的第二电离能为___________ kJ/mol;O=O键的键能为___________ kJ/mol;氧原子的第一电子亲和能为___________ kJ/mol(取正值)。
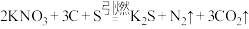 。请回答下列问题:
。请回答下列问题:(1)基态
 原子核外有
原子核外有(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为(3)基态钾离子的电子占据的最高能层符号是
 与
与 具有相同的核外电子排布,
具有相同的核外电子排布,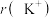 小于
小于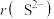 ,原因是
,原因是(4)元素的气态基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(
 )。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
)。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
由图可知,Mg原子的第二电离能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】乙炔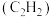 和丙烯腈
和丙烯腈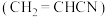 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。
(1) 的基态核外电子排布式为
的基态核外电子排布式为_______ 。 元素在周期表中的位置为
元素在周期表中的位置为_______ 。
(2)基态N原子第一电离能比基态O原子_______ (填“高”,“低”或“相等”)
(3) 的分子构型为
的分子构型为_______ 。
(4)每个丙烯腈分子中碳原子的杂化轨道类型有_______ 。
(5) 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为_______  。
。
(6)丙烯腈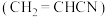 分子中共面的原子数目最多为
分子中共面的原子数目最多为_______ 。
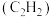 和丙烯腈
和丙烯腈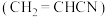 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。(1)
 的基态核外电子排布式为
的基态核外电子排布式为 元素在周期表中的位置为
元素在周期表中的位置为(2)基态N原子第一电离能比基态O原子
(3)
 的分子构型为
的分子构型为(4)每个丙烯腈分子中碳原子的杂化轨道类型有
(5)
 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为 。
。(6)丙烯腈
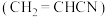 分子中共面的原子数目最多为
分子中共面的原子数目最多为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素在有机化学中有很重要的地位。请回答下列问题:
(1)基态氮原子的价层电子排布图为___________ 。
(2)2022年11月发射搭载神舟十五号载人飞船的长征二号火箭燃料为偏二甲肼 ,其中所含元素电负性从大到小的顺序为
,其中所含元素电负性从大到小的顺序为___________ 。
(3)N-甲基咪唑( )用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是
)用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是___________ 。
(4)吡啶( )在水中的溶解度远大于苯,可能原因是①
)在水中的溶解度远大于苯,可能原因是①___________ ;②___________ 。
(5)有机物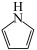 常用作医药原料、有机合成等,分子中
常用作医药原料、有机合成等,分子中 键与
键与 键之比为
键之比为___________ 。
(1)基态氮原子的价层电子排布图为
(2)2022年11月发射搭载神舟十五号载人飞船的长征二号火箭燃料为偏二甲肼
 ,其中所含元素电负性从大到小的顺序为
,其中所含元素电负性从大到小的顺序为(3)N-甲基咪唑(
 )用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是
)用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是(4)吡啶(
 )在水中的溶解度远大于苯,可能原因是①
)在水中的溶解度远大于苯,可能原因是①(5)有机物
 常用作医药原料、有机合成等,分子中
常用作医药原料、有机合成等,分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)中国古代四大发明之一--黑火药,它的爆炸反应为 (已配平)
(已配平)
①除S外,上列元素的电负性从大到小依次为__________ 。
②生成物A的晶体类型为__________ ,含极性共价键的分子的中心原子轨道杂化类型为_______ 。
③已知CN-与N2结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为____________ 。
(2)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_________ 。
(3)下列有关说法正确的是______________ 。
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.铬的堆积方式与钾相同,则其堆积方式如图

D.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强
(4)含有Cu2+ 的溶液中加入过量氨水,发现生成深蓝色溶液,试写出反应的离子方程式:_______ 。
(5)氮化硼形成立方晶体,晶体结构类似金刚石,如图所示。
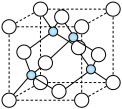
已知:该晶体密度为ρg·㎝-3,NA代表阿伏加 德罗常数的值。
①该晶体的化学式为______________ 。
②在该晶体中,B与N形成共价键的键长(d)为________________________ pm(列式即可)。
 (已配平)
(已配平)①除S外,上列元素的电负性从大到小依次为
②生成物A的晶体类型为
③已知CN-与N2结构相似,推算HCN分子中
 键与
键与 键数目之比为
键数目之比为(2)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是
(3)下列有关说法正确的是
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.铬的堆积方式与钾相同,则其堆积方式如图

D.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强
(4)含有Cu2+ 的溶液中加入过量氨水,发现生成深蓝色溶液,试写出反应的离子方程式:
(5)氮化硼形成立方晶体,晶体结构类似金刚石,如图所示。

已知:该晶体密度为ρg·㎝-3,NA代表阿伏加 德罗常数的值。
①该晶体的化学式为
②在该晶体中,B与N形成共价键的键长(d)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据元素周期表和周期律相关知识,回答下列问题:
(1)C、N、O三种元素电负性由大到小排序_______ ,第一电离能由小到大排序_______ ;
(2)①O2-,②Al3+,③Cl-,④Ca2+的半径由大到小排列为:_______ (用序号表示);
(3)元素非金属性Cl_______ S(填“>”或“<”),请举例证明:_______ (可用方程式或客观事实回答);
(4)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:_______ 。
(1)C、N、O三种元素电负性由大到小排序
(2)①O2-,②Al3+,③Cl-,④Ca2+的半径由大到小排列为:
(3)元素非金属性Cl
(4)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
您最近一年使用:0次



