磷是生物体内不可或缺的元素之一,自然界主要以磷酸盐的形式存在。磷酸盐可用于制备白磷(P4),白磷在加热条件下,能转化为红磷(P),白磷还能与足量热的浓碱发生如下反应:P4+3KOH+3H2O PH3↑+3KH2PO2。
PH3↑+3KH2PO2。
(1)磷原子的最外层核外电子排布式为______ 。
(2)PH3的电子式为______ 。热稳定性:NH3______ PH3(选填“>”或“<”)。
(3)P4的分子构型为正四面体,P4为______ 分子(选填“极性”或“非极性”)。
(4)白磷和红磷互为______ 。
(5)利用磷酸钙矿混以石英砂(SiO2)和炭粉在电炉中加热可以制备白磷。
______Ca3(PO4)2+______SiO2+______C ______CaSiO3+______P4+______CO↑
______CaSiO3+______P4+______CO↑
配平上述化学方程式______ 。
(6)次磷酸(H3PO2)是______ 弱酸(选填“一元”、“二元”或“三元”)。KH2PO2稀溶液中存在:c(K+)=______ 。
 PH3↑+3KH2PO2。
PH3↑+3KH2PO2。(1)磷原子的最外层核外电子排布式为
(2)PH3的电子式为
(3)P4的分子构型为正四面体,P4为
(4)白磷和红磷互为
(5)利用磷酸钙矿混以石英砂(SiO2)和炭粉在电炉中加热可以制备白磷。
______Ca3(PO4)2+______SiO2+______C
 ______CaSiO3+______P4+______CO↑
______CaSiO3+______P4+______CO↑配平上述化学方程式
(6)次磷酸(H3PO2)是
2023·上海徐汇·一模 查看更多[2]
更新时间:2023-03-09 21:21:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为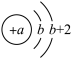 。请回答下列问题:
。请回答下列问题:
(1)Z元素在元素周期表中的位置是___ 。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为___ (元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为___ (用化学式表示)。
(4)用电子式表示WY2的形成过程___ 。
(5)写出W单质与浓硫酸反应的化学方程式___ 。
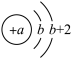 。请回答下列问题:
。请回答下列问题:| W | X | Y |
| Z |
(2)X、Y、Z三种元素的原子半径由大到小的顺序为
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)用电子式表示WY2的形成过程
(5)写出W单质与浓硫酸反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)用一个化学反应方程式表示C的非金属性比Si强___________ 。
(2)羟胺(H2NOH)是NH3的衍生物,各原子均满足稳定结构,H2NOH的电子式是___________ 。
(3)乙醇的沸点大于乙醛,主要原因是___________ 。
(2)羟胺(H2NOH)是NH3的衍生物,各原子均满足稳定结构,H2NOH的电子式是
(3)乙醇的沸点大于乙醛,主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.有①CH3COOH、②HCl、③H2SO4三种酸。
(1)0.1 mol·L-1的三种酸溶液,c(H+)由大到小的排列顺序是_______ (填序号)。
(2)体积相同、c(H+)相同的三种酸溶液分别与相同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_______ (填序号)。
(3)将c(H+)相同的三种酸溶液均加水稀释至原来的10倍,则稀释后三种酸溶液的pH由大到小的顺序为_______ (填序号)。
II.痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
①HUr(尿酸,aq) Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6) ,
Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6) ,
②NaUr(s) Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)
(4)37 ℃时,1.0L水中最多可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的Ksp为_______ 。
(5)关节炎发作多在脚趾和手指的关节处,这说明温度降低时,尿酸钠的Ksp_______ (填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是_______ (填“放热”或“吸热”)反应。
(6)37 ℃时,某尿酸结石病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol·L-1,其中尿酸分子的浓度为5.0×10-4mol·L-1,该病人尿液的c(H+)为_______ ,pH_______ 7(填“>”、“<”或“=”)。
(1)0.1 mol·L-1的三种酸溶液,c(H+)由大到小的排列顺序是
(2)体积相同、c(H+)相同的三种酸溶液分别与相同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是
(3)将c(H+)相同的三种酸溶液均加水稀释至原来的10倍,则稀释后三种酸溶液的pH由大到小的顺序为
II.痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
①HUr(尿酸,aq)
 Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6) ,
Ur-(尿酸根,aq)+H+(aq)(37 ℃时,Ka=4.0×10-6) ,②NaUr(s)
 Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)(4)37 ℃时,1.0L水中最多可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的Ksp为
(5)关节炎发作多在脚趾和手指的关节处,这说明温度降低时,尿酸钠的Ksp
(6)37 ℃时,某尿酸结石病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol·L-1,其中尿酸分子的浓度为5.0×10-4mol·L-1,该病人尿液的c(H+)为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列五种溶液:盐酸、NH3·H2O、NH4HSO4、NaOH、CH3COOH。回答下列问题:
(1)将1LpH=2的HCl溶液分别与0.01mol·L-1的NH3· H2O溶液x L、0.01 mol·L-1的NaOH溶液yL充分反应至中性,x、y大小关系为:y___ x(填“>”“<”或“=”)。
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是____ (填写序号)。
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
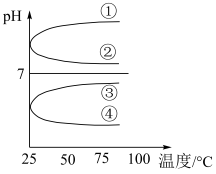
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的____ 曲线(填写序号)。
(4)室温下,向0.01mol·L-1NH4HSO4溶液中滴加0.01mol·L-1NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)___ 2c(SO42- )(填“>”“=”或“<”);用NH4HSO4与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH___ 7(填“>”“=”或“<”)
(5)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是____ (用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___ (填“正向”“不”或“逆向”)移动。
(1)将1LpH=2的HCl溶液分别与0.01mol·L-1的NH3· H2O溶液x L、0.01 mol·L-1的NaOH溶液yL充分反应至中性,x、y大小关系为:y
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的

(4)室温下,向0.01mol·L-1NH4HSO4溶液中滴加0.01mol·L-1NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)
(5)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1) 25℃时,电离平衡常数:
回答下列问题:
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是_______ (用化学式表示,下同)。
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是_______ 。
③在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO- + H+△H>0,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是_______ 。
a.加入少量0.10mol/L的稀盐酸 b.加热c.加水稀释至0.010mol/L d.加入少量冰醋酸 e.加入少量氯化钠固体
④常温下,0.1mol/L的CH3COOH液加水稀释过程中,下列表达式的数据一定变小的是_______ 。
a.c(H+) b. c.c(H+)c(OH-) d.
c.c(H+)c(OH-) d.
⑤体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图。溶液稀释后,HX溶液中水电离出来的c(H+)____ 醋酸溶液水电离出来c(H+)(填“大于”、“等于”或“小于”)。

(2)已知纯水中存在如下平衡:H2O ⇌ H++OH-。现欲使平衡逆向移动,且所得溶液显酸性,可选择的方法是_______ (填字母序号)。
a.向水中加入NaOH固体 b.向水中加入NaHSO4固体c.加热至100℃ d.向水中通入CO2气体
(3)常温下,将pH=11 的NaOH 溶液与pH=4 的硫酸混合,所得溶液的PH=9,则酸、碱溶液的体积比是_______ 。
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 4.0×10-8 |
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
③在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO- + H+△H>0,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是
a.加入少量0.10mol/L的稀盐酸 b.加热c.加水稀释至0.010mol/L d.加入少量冰醋酸 e.加入少量氯化钠固体
④常温下,0.1mol/L的CH3COOH液加水稀释过程中,下列表达式的数据一定变小的是
a.c(H+) b.
 c.c(H+)c(OH-) d.
c.c(H+)c(OH-) d.
⑤体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图。溶液稀释后,HX溶液中水电离出来的c(H+)

(2)已知纯水中存在如下平衡:H2O ⇌ H++OH-。现欲使平衡逆向移动,且所得溶液显酸性,可选择的方法是
a.向水中加入NaOH固体 b.向水中加入NaHSO4固体c.加热至100℃ d.向水中通入CO2气体
(3)常温下,将pH=11 的NaOH 溶液与pH=4 的硫酸混合,所得溶液的PH=9,则酸、碱溶液的体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】砷化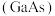 是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。
是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。
回答下列问题:
(1)写出基态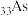 原子的核外电子排布式
原子的核外电子排布式___________ 。
(2)原子半径Ga___________ As,第一电离能Ga___________ As。
(3) 熔点为
熔点为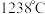 ,晶胞结构如图所示,则一个晶胞含
,晶胞结构如图所示,则一个晶胞含
___________ 个,含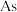
___________ 个。
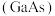 是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。
是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。回答下列问题:
(1)写出基态
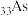 原子的核外电子排布式
原子的核外电子排布式(2)原子半径Ga
(3)
 熔点为
熔点为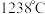 ,晶胞结构如图所示,则一个晶胞含
,晶胞结构如图所示,则一个晶胞含
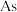

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】FeO和Fe2O3中较稳定的是___________ ,从原子结构角度分析,其理由是___________ 。
您最近一年使用:0次
【推荐3】回答下列问题
(1)元素 基态原子的核外电子排布式为
基态原子的核外电子排布式为____________ ;属于____________ 区
(2)基态 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为____________ ,该能层具有的原子轨道数为____________ .
(3)21号元素为:____________ (填元素符号),属于____________ 族.
(4) 原子序数为
原子序数为____________ ,其核外M层电子的排布式为____________ .
(5)某元素原子的 能级上有一个未成对电子,该元素为
能级上有一个未成对电子,该元素为____________ (填元素符号).
(6)第二周期中第一电离能在B和N之间的元素有____________ 种.
(7) 的价电子排布图为
的价电子排布图为____________ .
(1)元素
 基态原子的核外电子排布式为
基态原子的核外电子排布式为(2)基态
 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为(3)21号元素为:
(4)
 原子序数为
原子序数为(5)某元素原子的
 能级上有一个未成对电子,该元素为
能级上有一个未成对电子,该元素为(6)第二周期中第一电离能在B和N之间的元素有
(7)
 的价电子排布图为
的价电子排布图为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】数十亿年来,地球上的物质不断的变化,大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分,用下表涉及的分子回答下列问题。
(1)含有非极性共价键的分子是______ (填化学式)
(2)含有极性共价键的非极性分子是______ (填化学式)
(3)H2O中心原子的杂化方式及分子构型为______
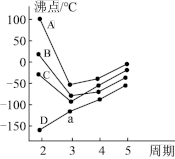
(4)图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物。其中代表CH4的是______ (填字母序号)
(5)根据NH3•H2O⇌NH4++OH-,用氢键表示式写出氨分子和水分子之间最主要存在的氢键形式______
| 原始大气的主要成分 | CH4、NH3、CO、CO2等 |
| 目前空气的主要成分 | N2、O2、CO2、水蒸气、稀有气体(He、Ne等) |
(1)含有非极性共价键的分子是
(2)含有极性共价键的非极性分子是
(3)H2O中心原子的杂化方式及分子构型为
(4)图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物。其中代表CH4的是

(5)根据NH3•H2O⇌NH4++OH-,用氢键表示式写出氨分子和水分子之间最主要存在的氢键形式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨基乙酸铜被广泛应用于染料、涂料、塑料和电池等领域,其化学式为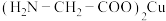 ,结构如图所示。
,结构如图所示。 原子的电子排布式为
原子的电子排布式为_______ , 位于元素周期表中
位于元素周期表中_______ 区元素(填“s、p、d、ds和f”其中一个)。
(2)氨基乙酸铜中碳原子的杂化方式有_______ 、_______ ,该分子中有_______ 个 键。
键。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态
表示,称为电子的自旋磁量子数。对于基态 原子,其价电子自旋磁量子数的代数和为
原子,其价电子自旋磁量子数的代数和为_______ 。
(4) 原子的第一电离能比
原子的第一电离能比 原子的
原子的_______ (填“大”或“小”),其原因是_______ 。
(5)氨基乙酸铜可由碳酸铜、氯乙酸、乙二胺等制得,碳酸铜中 的VSEPR模型名称为
的VSEPR模型名称为_______ ,氯乙酸的酸性大于乙酸的原因是_______ 。
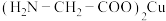 ,结构如图所示。
,结构如图所示。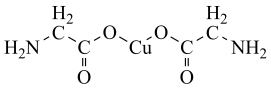
 原子的电子排布式为
原子的电子排布式为 位于元素周期表中
位于元素周期表中(2)氨基乙酸铜中碳原子的杂化方式有
 键。
键。(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态
表示,称为电子的自旋磁量子数。对于基态 原子,其价电子自旋磁量子数的代数和为
原子,其价电子自旋磁量子数的代数和为(4)
 原子的第一电离能比
原子的第一电离能比 原子的
原子的(5)氨基乙酸铜可由碳酸铜、氯乙酸、乙二胺等制得,碳酸铜中
 的VSEPR模型名称为
的VSEPR模型名称为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碳元素能形成多种单质如金刚石、石墨等,24g 金刚石中含有_______ 个碳碳单键。碳元素也能形成多种化合物,在形成化合物时,其所成化学键以共价键为主,原因是 _______ 。
(1)工业制镁时,电解 MgCl2 而不电解 MgO 的原因是_______ 。
(2)BeCl2 熔点较低,易升华,能溶于有机溶剂。由此可推测 BeCl2 晶体为_______ 晶体(填晶体类型),其分子为_______ 分子(填“极性”或“非极性”),分子构型为_______ ,BeCl2 熔点_______ (选填“低于”或“高于”)BeBr2。
(1)工业制镁时,电解 MgCl2 而不电解 MgO 的原因是
(2)BeCl2 熔点较低,易升华,能溶于有机溶剂。由此可推测 BeCl2 晶体为
您最近一年使用:0次



