完成下列小题
(1)写出“纯碱”的化学式___________ 。
(2)写出AlCl3在水中的电离方程式___________ 。
(3)写出NH3的电子式___________ 。
(4)将氯气通入冷的石灰乳中的化学反应方程式___________ 。
(1)写出“纯碱”的化学式
(2)写出AlCl3在水中的电离方程式
(3)写出NH3的电子式
(4)将氯气通入冷的石灰乳中的化学反应方程式
更新时间:2023-05-06 22:43:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氯化镁;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有_______ ,属于非电解质的有_______ 。
(2)④的电子式为_______ 。
(3)用电子式表示⑥的形成过程_______ 。
(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
(6) ②、③、⑦的气态氢化物中最不稳定的是___________ (填化学式);
(7)用电子式表示H2O的形成过程___________________ 。
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)写出③和⑥两种元素的元素符号:③
(2)②和④两种元素形成的共价化合物的电子式是
(3)元素②的气态氢化物的分子式为
元素⑨最高价氧化物对应水化物的分子式为
(4)④、⑤、⑧的原子半径由大到小的顺序为
(5) ②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(6) ②、③、⑦的气态氢化物中最不稳定的是
(7)用电子式表示H2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答下列问题:
(1)写出CO2的结构式___________ ;CCl4的电子式___________ 。
(2)写出NaHSO4在水中的电离方程式___________ 。
(3)写出CO2通入饱和Na2CO3溶液反应的离子方程式___________ 。
(4)用电子式表示K2O的形成过程___________ 。
(1)写出CO2的结构式
(2)写出NaHSO4在水中的电离方程式
(3)写出CO2通入饱和Na2CO3溶液反应的离子方程式
(4)用电子式表示K2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】以食盐为钠源制备纯碱的一种工艺流程如图。
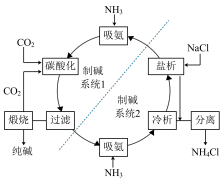
(1)熔融氯化钠可以导电是因为___________ (用化学用语解释)。
(2)电解熔融NaCl可制得单质钠,钠与水反应的化学方程式为___________ 。
(3)需要100mL0.1mol/L的NaCl溶液,配制时需用托盘天平称取NaCl固体___________ g。
(4)制碱系统1中,饱和食盐水吸氨后通入过量CO2碳酸化,过滤。
①滤渣的成分是___________ (填化学式),煅烧滤渣制取纯碱的化学方程式为___________ 。
②滤渣成分可作膨松剂,制馒头时与食醋(CH3COOH)共用效果更佳,相关的离子方程式为______ 。
(5)该流程中,可以循环利用的物质有CO2和___________ 。

(1)熔融氯化钠可以导电是因为
(2)电解熔融NaCl可制得单质钠,钠与水反应的化学方程式为
(3)需要100mL0.1mol/L的NaCl溶液,配制时需用托盘天平称取NaCl固体
(4)制碱系统1中,饱和食盐水吸氨后通入过量CO2碳酸化,过滤。
①滤渣的成分是
②滤渣成分可作膨松剂,制馒头时与食醋(CH3COOH)共用效果更佳,相关的离子方程式为
(5)该流程中,可以循环利用的物质有CO2和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】25°C时,在20 mL 0.1 mol·L-1HCOOH溶液中滴加0.1 mol·L-1 NaOH溶液,溶液中lg[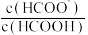 ]与pH的关系如图所示。已知Y点坐标为(0,3.75)。
]与pH的关系如图所示。已知Y点坐标为(0,3.75)。
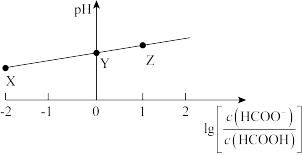
(1)HCOOH的电离方程式为___________________________________ 。
(2)25°C时,HCOOH 的电离平衡常数是_______________________ 。
(3)Y点溶液中各种离子浓度大小关系是____________________________ 。
(4)该滴定操作选择的最佳指示剂是____________ (填 “石蕊”“甲基橙”或“酚酞” )。滴定终点在Z点的_____ 方 (填“左下”或“右上”)。
(5)滴定终点观察到的现象是______________________________________________ 。 若滴定终了时发现滴定管尖嘴处有气泡,则记录NaOH溶液终点体积的读数______________ (填 “偏大”“偏小”或“无影响”)。
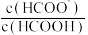 ]与pH的关系如图所示。已知Y点坐标为(0,3.75)。
]与pH的关系如图所示。已知Y点坐标为(0,3.75)。
(1)HCOOH的电离方程式为
(2)25°C时,HCOOH 的电离平衡常数是
(3)Y点溶液中各种离子浓度大小关系是
(4)该滴定操作选择的最佳指示剂是
(5)滴定终点观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:___ 。
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:_____________ 。
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是_______ 。
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。
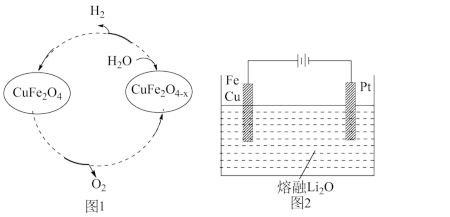
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_________ 。
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明 具有还原性的是实验
具有还原性的是实验_______ (填序号)。
(2)84消毒液的有效成分为 。
。
①NaClO中Cl元素的化合价是_______ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为_______ 。
(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式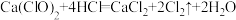 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:_______ 。
②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)_______ (填“能”或“不能”)同时使用,其原因是_______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①NaClO中Cl元素的化合价是
②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式
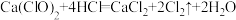 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】含氯消毒剂在生产生活中有着广泛的用途。完成下列填空:
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为_________ 。
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是_______________________________ ;“84消毒液”不能对钢铁制品进行消毒,原因是____________ 。
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是__________ ;处理从氯化塔中逸出气体的方法是_____ 。
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为_________ 。
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________________________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为
您最近一年使用:0次



