科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为________ 。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因________________ 。
(3)H2Se分子的键角_______ H2O分子的键角(选填“>”、“=”或“<”)。写出与SeO3互为等电子体的一种阴离子_____________ (写化学式)。
(4) AsF3分子的立体构型为__________ ;AsF3是极性分子,理由是_________________ 。
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有__________________ 。
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:
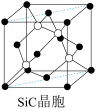
金刚砂中硅原子的杂化轨道类型为_______ ,沿晶胞图中虚线方向的切面图为__________ (填标号)。

(1)基态Ga原子的电子排布式为
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因
(3)H2Se分子的键角
(4) AsF3分子的立体构型为
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:

金刚砂中硅原子的杂化轨道类型为

更新时间:2019-07-10 10:35:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_____ Ⅰ1(Cu)(填“大于”或“小于”)。原因是_____________________________ 。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________ ,C原子的杂化形式为________________ ,SO42-、CS2、CO32-键角由大到小的顺序是______________________
(4)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫也可以发生类似水的自身电离2SO2 SO2++SO32-,S和O两种元素中电负性较强的是
SO2++SO32-,S和O两种元素中电负性较强的是______________ ,与SO2+互为等电子体的单质分子是________ (填化学式),SO2+中σ键和Π键数目比为___________ 。
(5)分析并比较物质A: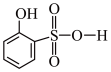 与B:
与B: 的沸点高低及其原因:
的沸点高低及其原因:__
(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫也可以发生类似水的自身电离2SO2
 SO2++SO32-,S和O两种元素中电负性较强的是
SO2++SO32-,S和O两种元素中电负性较强的是(5)分析并比较物质A:
 与B:
与B: 的沸点高低及其原因:
的沸点高低及其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)基态Cl原子中,电子占据的最高电子层符号为_______ ,该电子层具有的原子轨道数为_______ 。
(2)基态原子的N层有1个未成对电子,M层未成对电子最多的元素是_______ ,其价电子排布式为_______ 。
(3)最外层电子数是次外层电子数3倍的元素是_______ ,其电子排布图为_______ 。
(4)下列表示的为一激发态原子的是_______ 。
A.1s12s1 B.1s22s22p1 C.1s22p53s1 D.1s22s22p63s2
(2)基态原子的N层有1个未成对电子,M层未成对电子最多的元素是
(3)最外层电子数是次外层电子数3倍的元素是
(4)下列表示的为一激发态原子的是
A.1s12s1 B.1s22s22p1 C.1s22p53s1 D.1s22s22p63s2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】GaN是制造芯片的新型半导体材料。回答下列问题:
(1)镓为第四周期的元素,基态Ga原子的核外电子排布式为___________ 。
(2)N、Si、P的电负性由强到弱顺序为___________ (元素符号表示,下同);C、N、O的第一电离能由大到小顺序为___________ ; 的空间构型为
的空间构型为___________ 。
(3)芯片制造中用到光刻胶,可由不饱和物质甲基丙烯酸甲酯(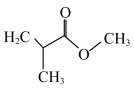 )、马来酸酐(
)、马来酸酐( )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为___________ ,马来酸酐分子中,σ键和π键个数比为___________ 。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①图甲中,Ga原子的配位数为___________ ,若GaAs晶体密度为ρg·cm3,相对分子质量为M, 表示阿伏伽德罗常数的数值,则晶胞中距离最近的两个Ga原子间距离为
表示阿伏伽德罗常数的数值,则晶胞中距离最近的两个Ga原子间距离为___________ nm。
②图乙中a、b的坐标分别为 (0,0,0)和(1,1,0),则c点Mn的原子坐标为___________ 。掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为___________ 。
(1)镓为第四周期的元素,基态Ga原子的核外电子排布式为
(2)N、Si、P的电负性由强到弱顺序为
 的空间构型为
的空间构型为(3)芯片制造中用到光刻胶,可由不饱和物质甲基丙烯酸甲酯(
 )、马来酸酐(
)、马来酸酐( )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①图甲中,Ga原子的配位数为
 表示阿伏伽德罗常数的数值,则晶胞中距离最近的两个Ga原子间距离为
表示阿伏伽德罗常数的数值,则晶胞中距离最近的两个Ga原子间距离为②图乙中a、b的坐标分别为 (0,0,0)和(1,1,0),则c点Mn的原子坐标为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】三价铬离子( )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
(1)Cr的价层电子排布式为_______ 。
(2)O、N、S的原子半径由大到小的顺序为_______ 。
(3) 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为_______ ,其中心原子的杂化方式为_______ 。
(4)化学式为 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为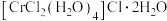 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为_______ ,配位数为_______ 。
(5) 分子可以与
分子可以与 结合生成
结合生成 ,这个过程发生改变的是
,这个过程发生改变的是_______ (填序号)。
a.微粒的空间结构 b.N原子的杂化类型 c.H-N-H键角 d.微粒的电子数
 )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、HO、N、S、Cr等。回答下列问题:(1)Cr的价层电子排布式为
(2)O、N、S的原子半径由大到小的顺序为
(3)
 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为(4)化学式为
 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为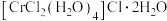 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为(5)
 分子可以与
分子可以与 结合生成
结合生成 ,这个过程发生改变的是
,这个过程发生改变的是a.微粒的空间结构 b.N原子的杂化类型 c.H-N-H键角 d.微粒的电子数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
回答下列问题:
(1)D的简单气态氢化物分子的立体构型为___________ 。
(2)第一电离能H___________ X(填“>”、“<”或“=”)。
(3)DA3的沸点比D2E的沸点高,其原因是___________ 。
(4)YE 的立体构型为
的立体构型为___________ ,YE 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是___________ 。
| A | R | ||||||||||||||||
| B | D | E | M | T | |||||||||||||
| G | H | X | J | Y | L | ||||||||||||
| N |
(1)D的简单气态氢化物分子的立体构型为
(2)第一电离能H
(3)DA3的沸点比D2E的沸点高,其原因是
(4)YE
 的立体构型为
的立体构型为 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.用“>”或“<”填空:
(1)键长:N-N_____ N=N (2)键能:2E(C-C)_____ E(C=C)
(3)键角:CO2_____ SO2; (4)键的极性:C-H_____ N-H。
II.指出下列原子的杂化轨道类型及分子的空间构型。
(1) CO2中的C________ 杂化,空间构型________ ;
(2) SiF4中的Si________ 杂化,空间构型________ ;
(3) PH3中的P________ 杂化,空间构型________ ;
(4) NO2ˉ中的N________ 杂化,空间构型________ 。
(1)键长:N-N
(3)键角:CO2
II.指出下列原子的杂化轨道类型及分子的空间构型。
(1) CO2中的C
(2) SiF4中的Si
(3) PH3中的P
(4) NO2ˉ中的N
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】分子空间构型
(1)孤电子对数=0的分子空间构型
(2)孤电子对、成键电子对之间斥力大小的顺序为:
___________ 之间的斥力>___________ 之间的斥力>___________ 之间的斥力。
(3)填写下表:
(1)孤电子对数=0的分子空间构型
| 价电子对数 | 价电子对的几何构型 | 分子的空间构型 | 实例 |
 | 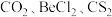 | ||
 | 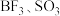 | ||
 | 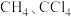 |
(3)填写下表:
| 分子 | 价电子对数 | 成键电子对数 | 孤电子对数 | 分子的空间构型 | 键角 | 同类型分子 |
| CH4 | 109.5° | |||||
| NH3 | 107.3° | |||||
| H2O | 104.5° |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氟及其化合物用途非常广泛。回答下列问题:
(1)基态F原子的价层电子的轨道表达式为____ 。
(2)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为_____ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_____ 和_____ (各举一例)。
(3)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是
中中心原子的杂化类型是_____ ;氟化铵中存在的化学键是_____ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
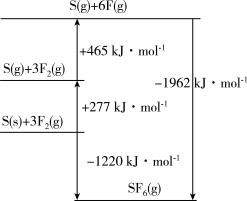
(4)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为____ kJ·mol-1,S-F键的键能为____ kJ·mol-1。
(1)基态F原子的价层电子的轨道表达式为
(2)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(3)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
 中中心原子的杂化类型是
中中心原子的杂化类型是A.离子键 B.σ键 C.π键 D.氢键
(4)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下(H2O)2•BF3可发生如图的转化:_______ ,属于_____ 分子(选填“极性”或“非极性”)。
(2) 中B原子采用杂化形式为
中B原子采用杂化形式为_______ 杂化。
(3)F-B-F键角大小:BF3_______  (选填>、=或<)。
(选填>、=或<)。
(4)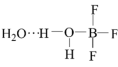 中不存在的微粒间相互作用是
中不存在的微粒间相互作用是_______ 。
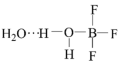


(2)
 中B原子采用杂化形式为
中B原子采用杂化形式为(3)F-B-F键角大小:BF3
 (选填>、=或<)。
(选填>、=或<)。(4)
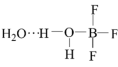 中不存在的微粒间相互作用是
中不存在的微粒间相互作用是| A.配位键 | B.氢键 | C.极性键 | D.非极性键 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】超临界状态是一种特殊的流体,用超临界CO2/CH3CN及水作电解质,使用碳作载体的铜基催化剂可高效将CO2还原为HCOOH。回答下列问题:
(1)CO2电子式为___________ 。
(2)碳元素位于元素周期表的___________ 区,基态碳原子核外电子有___________ 种空间运动状态。第二周期中基态原子与基态碳原子具有相同未成对电子数的元素是___________ (填元素符号)。
(3)基态Cu和Cu2+未成对电子数之比为___________ 。
(4)CO2和HCOOH分子中C原子的杂化形式分别为___________ 和___________ 。
(5)HCOOH通常以二聚体(含八元环)形式存在(如图),该二聚体中含有的微粒间作用力有___________ 。
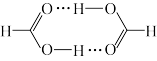
(1)CO2电子式为
(2)碳元素位于元素周期表的
(3)基态Cu和Cu2+未成对电子数之比为
(4)CO2和HCOOH分子中C原子的杂化形式分别为
(5)HCOOH通常以二聚体(含八元环)形式存在(如图),该二聚体中含有的微粒间作用力有
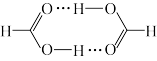
您最近一年使用:0次


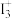 离子。
离子。

