根据下列表格,回答有关问题:

(1)上表中,第一电离能最小的元素是____ (填元素名称,下同),电负性最大的元素是___
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是_____ (填化学式,下同),碱性最强的是_____ 。
(3)某元素最高价氧化物对应的水化物呈两性,则该元素是_____ (填对应的字母),该元素与c元素形成的化合物能否与NaOH溶液反应(若能,写出相应的离子方程式;若不能,则填“否”)________ 。
(4)在e~k元素的原子中,原子半径最小的是_____ (填元素符号),其价电子排布式为______ ;未成对电子数最多的是____ (填元素符号),其最高价氧化物对应水化物的化学式为_____ ;有两个未成对电子的元素是________ (填元素符号);M层有两个空轨道的是____ (填元素符号),其阳离子结构示意图为____ 。

(1)上表中,第一电离能最小的元素是
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(3)某元素最高价氧化物对应的水化物呈两性,则该元素是
(4)在e~k元素的原子中,原子半径最小的是
更新时间:2019-04-20 22:41:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答下列各小题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,Fe成为阳离子时首先失去___________ 轨道电子。
(2)基态S原子电子占据最高能级的电子云轮廓图为___________ 形,Sm的价层电子排布式为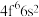 ,
, 的价层电子排布式为
的价层电子排布式为___________ 。
(3)28号镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)基态S原子电子占据最高能级的电子云轮廓图为
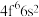 ,
, 的价层电子排布式为
的价层电子排布式为(3)28号镍元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究氮原子的结构及其化合物具有重要意义
(1)氮原子的基态电子排布式为_______ 。
(2)NH3的电子式_______ 。
(3)实验室制备NH3化学方程式是_______ 。
(4)①工业合成的NH3化学方程式是_______ 。
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于_______ kJ。
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①_______ 。②_______ 。③_______ 。
(1)氮原子的基态电子排布式为
(2)NH3的电子式
(3)实验室制备NH3化学方程式是
(4)①工业合成的NH3化学方程式是
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。

请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象。____________________
(2)由图分析可知,同一主族元素原子的第一电离能I1变化规律是____________________ 。
(3)图中5号元素在周期表中的位置是________ 周期________ 族。
(4)图中出现的元素中最活泼的金属元素位于元素周期表的________ 周期________ 族。
(5)写出图中6号元素的价电子排布式:________ 。
(6)分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围________ <Al<________ (填元素符号)。

请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象。
(2)由图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)图中5号元素在周期表中的位置是
(4)图中出现的元素中最活泼的金属元素位于元素周期表的
(5)写出图中6号元素的价电子排布式:
(6)分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】向硫酸铜水溶液中逐滴滴加氨水,先生成蓝色沉淀,继续滴加氨水得到深蓝色溶液,再向溶液中加入乙醇,有深蓝色晶体[Cu(NH3)4]SO4·H2O析出。
(1)铜元素位于元素周期表中____ 区,高温超导体钇钡铜氧材料中铜元素有+2和+3两种价态,基态Cu3+的电子排布式为____ 。
(2)非金属元素N、O、S的第一电离能由大到小的顺序是____ (用元素符号表示)。
(3)上述深蓝色晶体中含有的元素的电负性最小的是____ (用元素符号表示)。
(4)H2O的中心原子轨道杂化类型为____ 杂化;SO42-离子的立体构型是____ ,写出与SO42-互为等电子体的一种离子____ 。
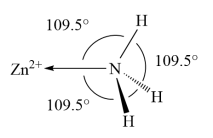
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因____ 。
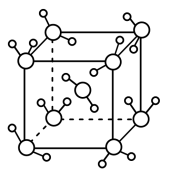
(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为____ g.cm-3(只列式,不计算)。
(1)铜元素位于元素周期表中
(2)非金属元素N、O、S的第一电离能由大到小的顺序是
(3)上述深蓝色晶体中含有的元素的电负性最小的是
(4)H2O的中心原子轨道杂化类型为
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因

(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.硒化锌是一种透明半导体,也可作为红外光学材料,熔点是1520℃。
(1)基态锌原子的价电子排布式是_____ 。
(2)根据元素周期律,电负性Se_____ S,Se位于周期表_____ 区。
(3)H2Se的分子构型是_____ ,其中硒原子的杂化轨道类型是_____ 。
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是_____ 。
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是_____ 。
(6)1molN2F2含有_____ molσ键。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是
(6)1molN2F2含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】生成氢气:在恒温恒容的反应器中,将水蒸气通过红热的炭即产生水煤气: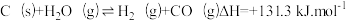 。
。
(1)以上涉及到的元素中,电负性最大的元素为_______。
(2)H2O的价层电子对空间结构为_______ (需过程)
(3)写出该反应的平衡常数表达式_______ 。
(4)下列能作为反应达到平衡的判据是_______。
(5)有利于提高H2平衡产率的条件是_______。
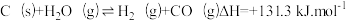 。
。(1)以上涉及到的元素中,电负性最大的元素为_______。
| A.碳 | B.氢 | C.氧 |
(3)写出该反应的平衡常数表达式
(4)下列能作为反应达到平衡的判据是_______。
| A.容器内气体的压强不变 |
| B.K值不变 |
| C.H2O和H2的物质的量之比不变 |
| D.CO和H2的物质的量之比不变 |
| A.低温低压 | B.低温高压 |
| C.高温低压 | D.高温高压 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
元素M化合态常见化合价是___________ 价,其基态原子电子排布式为____________ 。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是______________ 。
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为________________ 。
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为___________ 。NF3不易与Cu2 +形成化学键,其原因是________________________ 。
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]S04溶液,该溶液可用于溶解纤维素。
①[Cu (NH3) 4 ] S04中阴离子的立体构型是
②除硫元素外,[Cu( NH3) 4 ] S04中所含元素的电负性由小到大的顺序为
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铝及其化合物在制造、化工等领域都有广泛应用。回答下列问题:
(1)基态铝原子的核外电子排布式为_______ ,占据最高能级的电子云轮廓图形状为_______ 。基态铝原子比基态镁原子的第一电离能小,其原因是_______ 。
(2)通常情况下, 可由六氟铝酸铵[
可由六氟铝酸铵[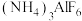 ]受热分解制得,反应的化学方程式为
]受热分解制得,反应的化学方程式为_______ 。
(3) 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于_______ (填晶体类型)晶体。 在178℃时升华,
在178℃时升华, 、
、 的晶体类型不同的原因是
的晶体类型不同的原因是_______ 。
(4) 在水溶液中实际上是以
在水溶液中实际上是以 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为_______ ,该阴离子中存在的化学键有_______ (填标号)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(1)基态铝原子的核外电子排布式为
(2)通常情况下,
 可由六氟铝酸铵[
可由六氟铝酸铵[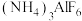 ]受热分解制得,反应的化学方程式为
]受热分解制得,反应的化学方程式为(3)
 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于 在178℃时升华,
在178℃时升华, 、
、 的晶体类型不同的原因是
的晶体类型不同的原因是(4)
 在水溶液中实际上是以
在水溶液中实际上是以 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
您最近一年使用:0次



