(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小 的,其核外电子排布式为______ ,价电子构型为______ ,属________ 区元素。
(2)某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,最高正化合价为________ ,元素符号是________ 。
(3)原子序数为24的元素原子中有________ 个电子层,________ 个能级,________ 个未成对电子。
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)________________ 。
(2)某元素原子的价电子构型为4s24p1,它属于第
(3)原子序数为24的元素原子中有
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)
更新时间:2017-04-12 08:05:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识回答问题:
(1)写出表示含有8个质子,10个中子的原子的结构示意图:___________ 。
(2)最外层电子数为次外层电子数 的原子
的原子___________ 或___________ ;(填元素符号)
(3)根据下列微粒回答问题: 、
、 、
、 、
、 、
、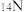 、
、 、
、 、
、 。
。
①以上8种微粒共有___________ 种核素,共___________ 种元素。
②互为同位素的是___________ 。
③中子数相等的是___________ 。
(4)相同物质的量的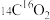 与
与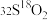 的质量之比为
的质量之比为___________ ;电子数之比为___________ 。
(1)写出表示含有8个质子,10个中子的原子的结构示意图:
(2)最外层电子数为次外层电子数
 的原子
的原子(3)根据下列微粒回答问题:
 、
、 、
、 、
、 、
、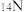 、
、 、
、 、
、 。
。①以上8种微粒共有
②互为同位素的是
③中子数相等的是
(4)相同物质的量的
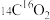 与
与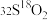 的质量之比为
的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
Ⅰ.用“>”或“<”填空:
(1)键长:N-N___________ N=N
(2)键能:2E(C-C)___________ E(C=C)
(3)键角:CO2___________ SO2;
(4)键的极性:C-H___________ N-H。
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO 中的N
中的N___________ 杂化,空间构型___________ ;
(2)BCl3中的B___________ 杂化,空间构型___________ ;
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含___________ 种元素,___ 种核素,___________ 种相对分子质量。
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是___________ 电子,原子轨道呈现___________ 形,它的氢化物的电子式是___________
Ⅰ.用“>”或“<”填空:
(1)键长:N-N
(2)键能:2E(C-C)
(3)键角:CO2
(4)键的极性:C-H
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO
 中的N
中的N(2)BCl3中的B
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮族元素包括氮、磷、砷、锑、铋等元素,其单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有____ 种能量不同的电子。
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为____ ,其水解会生成两种酸,写出水解的化学方程式____ 。
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是____ (填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为____ ,最高能级的电子云形状为____ ,As元素在元素周期表中的位置为____ 。
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式____ 。
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位于第ⅦA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。R基态原子的电子排布式是___ 。
(2)基态Ni原子的电子排布式为____ ,该元素位于元素周期表中的第____ 族。
(3) Cr3+基态核外电子排布式为___ 。
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用________ 形象化描述。在基态14C原子中,核外存在____ 对自旋相反的电子。
(2)基态Ni原子的电子排布式为
(3) Cr3+基态核外电子排布式为
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(一)铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表中第___ 族,其基态原子中未成对电子的个数为_________ 。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为_________ ,其中尿素分子中σ键与π键的数目之比为___ ,所含非金属元素的电负性由大到小的顺序是_______ 。
(二)已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_____________ 。
(2)砷与氢元素。可形成化合物砷化氢,该化合物的空间构型为_____ ,其中 砷原子的杂化方式为__________ 。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式__________ 。
(1)钴位于元素周期表中第
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为
(二)已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为
(2)砷与氢元素。可形成化合物砷化氢,该化合物的空间构型为
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】填写下列有关铁元素的信息
| 表示方法 | 写法 |
| 原子符号 | |
| 电子排布式 | |
| 简化电子排布式 | |
| 价电子排布式 | |
| M层电子排布式 | |
| 原子结构示意图 | |
| Fe2+的电子排布式 | |
| Fe3+的电子排布式 | |
| 电子排布图(轨道表示式) | |
| 价电子排布图 | |
| 最外层电子数 | |
| 价电子总数 |
您最近一年使用:0次
【推荐2】回答下列问题:
(1)下列原子或离子的电子排布式或轨道表示式正确的是___________ (填序号)
①K+: ②F:
②F: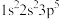
③P: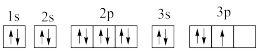
④Cu: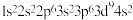
⑤Fe2+: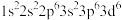
⑥Mg:
⑦O: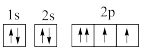
(2)基态原子的核外电子填充在6个轨道中的元素有___________ 种;
(3)C、N、O第一电离能从大到小的顺序为:___________ ;
(4)第四周期元素中,未成对电子数最多的元素是:___________ (写元素符号)。
(1)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:
 ②F:
②F: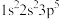
③P:
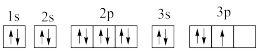
④Cu:
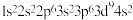
⑤Fe2+:
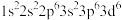
⑥Mg:

⑦O:
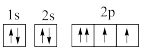
(2)基态原子的核外电子填充在6个轨道中的元素有
(3)C、N、O第一电离能从大到小的顺序为:
(4)第四周期元素中,未成对电子数最多的元素是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阿散酸(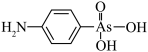 )是一种饲料添加剂,能溶于NaOH溶液中,常含有
)是一种饲料添加剂,能溶于NaOH溶液中,常含有 、NaCl等杂质。回答下列问题(用元表符号或化学式表示):
、NaCl等杂质。回答下列问题(用元表符号或化学式表示):
 原子核外电子占据的最高能级为
原子核外电子占据的最高能级为(2)As元素的第一电离能
(3)
 的中心原子的杂化方式为
的中心原子的杂化方式为 的空间构型为
的空间构型为(4)太阳电池材料中的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
(5)阿散酸分子中C和N的杂化类型分别是
您最近一年使用:0次



