合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
更新时间:2022-03-15 21:55:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据所学知识,回答下列问题:
(1)写出C元素在元素周期表中的位置:___________ ;
(2)写出C与浓硫酸反应的化学方程式:___________ ;
(3)将胆矾晶体投入浓硫酸中,可观察到___________ ,体现了浓硫酸的___________ 性;
(4)除下列气体中的杂质所需要的试剂,括号内为杂质: (HCl)
(HCl)___________ ;NO( )
)___________
(1)写出C元素在元素周期表中的位置:
(2)写出C与浓硫酸反应的化学方程式:
(3)将胆矾晶体投入浓硫酸中,可观察到
(4)除下列气体中的杂质所需要的试剂,括号内为杂质:
 (HCl)
(HCl) )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表中阿拉伯数字(1、2……)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:_______ 。
(2)I元素在周期表中的位置是第_______ 周期、第_______ 族。
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。
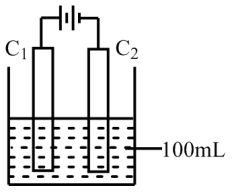
①写出电极C1上发生反应的电极反应式_______ 。
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=_______ 。(Kw=1.0×10-14)
纵行 横行 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:
(2)I元素在周期表中的位置是第
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。

①写出电极C1上发生反应的电极反应式
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图中的曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质):
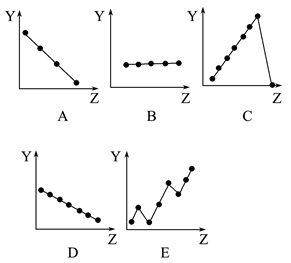
把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数___________ ;
(2)第三周期元素的最高正化合价___________ ;
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径___________ ;
(4)第二周期元素的原子半径(不包括稀有气体)___________ ;
(5)第二周期元素的第一电离能___________ 。

把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数
(2)第三周期元素的最高正化合价
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径
(4)第二周期元素的原子半径(不包括稀有气体)
(5)第二周期元素的第一电离能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表列出了A-R九种元素在元素周期表中的位置,试用元素符号或化学式回答下列问题:
(1)B的离子结构示意图为___________ ,AD两最高价氧化物对应的的水化物反应的离子方程式是___________ 。
(2)在AC、D、F这些元素形成的最简单离子中,离子半径由大到小的顺序是___________ (填离子符号),AC、D最高价氧化物对应水化物的碱性由强到弱为___________ 。
(3)由元素AF形成的一种杀菌消毒剂中存在的化学键有___________ 。
(4)由元素E和G形成的某种化合物可表示为 (其中各原子均满足8电子稳定结构),写出
(其中各原子均满足8电子稳定结构),写出 的电子式:
的电子式:___________ 。
(5)已知常温下氯酸钾与浓盐酸反应放出气体 ,现按如图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是___________。
,现按如图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是___________。
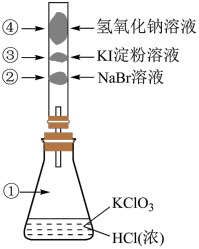
(6)G元素和H元素两者核电荷数之差是___________ 。
周期 主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | F | |||||||
| 3 | A | C | D | E | G | R | ||
| 4 | B | H |
(1)B的离子结构示意图为
(2)在AC、D、F这些元素形成的最简单离子中,离子半径由大到小的顺序是
(3)由元素AF形成的一种杀菌消毒剂中存在的化学键有
(4)由元素E和G形成的某种化合物可表示为
 (其中各原子均满足8电子稳定结构),写出
(其中各原子均满足8电子稳定结构),写出 的电子式:
的电子式:(5)已知常温下氯酸钾与浓盐酸反应放出气体
 ,现按如图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是___________。
,现按如图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是___________。
| ① | ② | ③ | ④ | |
| A | 黄绿色 | 橙色 | 蓝色 | 无色 |
| B | 无色 | 橙色 | 紫色 | 白色 |
| C | 黄绿色 | 橙色 | 蓝色 | 白色 |
| D | 黄绿色 | 无色 | 紫色 | 白色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】针对下面10种元素,完成以下各小题
(1)地壳中含量最多的元素是___________ (填名称)。
(2)化学性质最不活泼的元素是___________ (填元素符号)。
(3)Al的原子结构示意图为___________________ 。
(4)C与N相比,原子半径较小的是___________ 。
(5)最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________ 。
(7)S和Cl相比,元素非金属性较强的是___________ 。
(1)地壳中含量最多的元素是
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Al | Si | S | Cl | Ne |
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业烟气可用氯酸氧化法脱硫,涉及反应:_______ _______
_______ _______
_______ =_______
=_______ (未配平)。完成下列填空:
(未配平)。完成下列填空:
(1)写出N原子核外电子排布的轨道表示式_______ 。
(2)用含字母a、b的代数式配平上述化学方程式_______ ,标出电子转移的方向和数目_______ 。该化学方程式配平系数不唯一,请说明理由_______ 。
(3)氯酸是一元强酸,可由氯酸钡溶液和稀硫酸反应得到。写出该反应的化学方程式_______ 。
(4)工业烟气中的 也可用
也可用 和
和 的混合液脱除。
的混合液脱除。
① 脱除
脱除 的离子方程式为
的离子方程式为_______ ;
② 溶液呈碱性的原因是
溶液呈碱性的原因是_______ 。
 _______
_______ _______
_______ =_______
=_______ (未配平)。完成下列填空:
(未配平)。完成下列填空:(1)写出N原子核外电子排布的轨道表示式
(2)用含字母a、b的代数式配平上述化学方程式
(3)氯酸是一元强酸,可由氯酸钡溶液和稀硫酸反应得到。写出该反应的化学方程式
(4)工业烟气中的
 也可用
也可用 和
和 的混合液脱除。
的混合液脱除。①
 脱除
脱除 的离子方程式为
的离子方程式为②
 溶液呈碱性的原因是
溶液呈碱性的原因是
您最近一年使用:0次
【推荐2】①、②、③、④是原子序数依次增大的四种短周期元素,①周期表中原子半径最小的元素,②的最外层电子数比次外层多1,③的第一电离能比左右相邻两元素的都要大,④是周期表中电负性最大的元素。元素①和③可形成一种三角锥形的分子A,元素②和④可形成一种平面三角形的分子B。
(1)元素②的基态原子的电子排布式为___________ 。
(2)元素③的价电子的轨道表示式为___________ 。
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:___________ (用元素符号表示)。
(4)分子A的电子式为___________ ,分子B的中心原子杂化方式为___________ ;A与B之间能否形成配位键?若能,用化学用语表示出两者之间的配位键;若不能,说明理由:___________ 。
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:___________ 。
(1)元素②的基态原子的电子排布式为
(2)元素③的价电子的轨道表示式为
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:
(4)分子A的电子式为
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下列关于碳和碳的化合物的结构和性质中
(1)和碳同一主族的硅原子中能量最高的电子处在______ 电子层上(填写电子层符号),最外层有___ 种运动状态不同的电子,碳原子核外有______ 种能量不同的电子,有______ 种不同形状的电子云.
(2)1个C原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6.以下各对分子间不存在类似关系的是_________
A.NH3与N2H4 B.H2O与H2O2 C.SF6与S2F10 D.SCl4与S2Cl2
(3)金刚石的熔点低于石墨,原因可能是________
A.石墨中还有范德华力
B.石墨熔化也要破坏共价键,且键长更短
C.石墨热稳定性更好
(4)已知常温下,H2CO3:Ki1=4.3x10﹣7、Ki2=5.6x10﹣11.结合H+的能力Na2CO3溶液______ (填”>”、”<”或“=”)NaHCO3溶液,设计简单实验证明:______ .
(5)在1L 0.3mol/L的NaOH溶液中,通入4.48LCO2(标准状况),反应后所得溶液中离子的浓度之间有一些等量关系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外对此溶液中存在的离子按浓度由大到小排序为______ .
(1)和碳同一主族的硅原子中能量最高的电子处在
(2)1个C原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6.以下各对分子间不存在类似关系的是
A.NH3与N2H4 B.H2O与H2O2 C.SF6与S2F10 D.SCl4与S2Cl2
(3)金刚石的熔点低于石墨,原因可能是
A.石墨中还有范德华力
B.石墨熔化也要破坏共价键,且键长更短
C.石墨热稳定性更好
(4)已知常温下,H2CO3:Ki1=4.3x10﹣7、Ki2=5.6x10﹣11.结合H+的能力Na2CO3溶液
(5)在1L 0.3mol/L的NaOH溶液中,通入4.48LCO2(标准状况),反应后所得溶液中离子的浓度之间有一些等量关系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外对此溶液中存在的离子按浓度由大到小排序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)  及其周期表中相邻元素的第一电离能(
及其周期表中相邻元素的第一电离能( )如表所示。
)如表所示。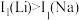 ,原因是
,原因是_____ 。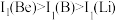 ,原因是
,原因是___________ 。
(2)黄铜是人类最早使用的合金之一,主要由 和
和 组成。第一电离能
组成。第一电离能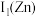
___________  (填“大于”或“小于”)。原因是
(填“大于”或“小于”)。原因是___________ 。
(3)元素 与O中,第一电离能较大的是
与O中,第一电离能较大的是___________ ,基态原子核外未成对电子数较多的是___________ 。
 及其周期表中相邻元素的第一电离能(
及其周期表中相邻元素的第一电离能( )如表所示。
)如表所示。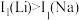 ,原因是
,原因是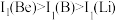 ,原因是
,原因是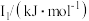 | ||
 520 |  900 | B 801 |
 496 |  738 |  578 |
(2)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。第一电离能
组成。第一电离能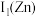
 (填“大于”或“小于”)。原因是
(填“大于”或“小于”)。原因是(3)元素
 与O中,第一电离能较大的是
与O中,第一电离能较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)Q+核外价电子排布式为___ 。
(2)ZW3- 离子的立体构型是___ 。
(3)Y、R的最高价氧化物,其中一种沸点较高,原因是___ 。
(4)W在元素周期表中的位置为___ 。
(1)Q+核外价电子排布式为
(2)ZW3- 离子的立体构型是
(3)Y、R的最高价氧化物,其中一种沸点较高,原因是
(4)W在元素周期表中的位置为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁的化合物在日常生产、生活中应用非常广泛。某含 化合物的制备需氮气、丙酮和乙醇参与。
化合物的制备需氮气、丙酮和乙醇参与。
(1)CO、NO均能够与血红蛋白(Hb)中 形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
已知: 进入血液后有如下平衡:
进入血液后有如下平衡:
①基态 中未成对电子数为
中未成对电子数为_______ 。
②C、N、O三种元素,第一电离能由大到小的顺序为_______ 。
③在 、
、 结构中,C、N、O原子均含有孤电子对,与
结构中,C、N、O原子均含有孤电子对,与 配位时,配位原子均不是
配位时,配位原子均不是 原子,理由是
原子,理由是_______ 。
(2)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是_______ 。
(3)合成氨催化剂前驱体(主要成分为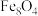 )使用前
)使用前 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为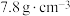 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,阿伏加德罗常数的值为 )。
)。
 化合物的制备需氮气、丙酮和乙醇参与。
化合物的制备需氮气、丙酮和乙醇参与。(1)CO、NO均能够与血红蛋白(Hb)中
 形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。已知:
 进入血液后有如下平衡:
进入血液后有如下平衡:
①基态
 中未成对电子数为
中未成对电子数为②C、N、O三种元素,第一电离能由大到小的顺序为
③在
 、
、 结构中,C、N、O原子均含有孤电子对,与
结构中,C、N、O原子均含有孤电子对,与 配位时,配位原子均不是
配位时,配位原子均不是 原子,理由是
原子,理由是(2)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是
(3)合成氨催化剂前驱体(主要成分为
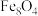 )使用前
)使用前 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为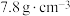 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。
您最近一年使用:0次



