根据所学知识,回答下列问题:
(1)写出C元素在元素周期表中的位置:___________ ;
(2)写出C与浓硫酸反应的化学方程式:___________ ;
(3)将胆矾晶体投入浓硫酸中,可观察到___________ ,体现了浓硫酸的___________ 性;
(4)除下列气体中的杂质所需要的试剂,括号内为杂质: (HCl)
(HCl)___________ ;NO( )
)___________
(1)写出C元素在元素周期表中的位置:
(2)写出C与浓硫酸反应的化学方程式:
(3)将胆矾晶体投入浓硫酸中,可观察到
(4)除下列气体中的杂质所需要的试剂,括号内为杂质:
 (HCl)
(HCl) )
)
更新时间:2023-04-11 21:59:58
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学是一门实用性很强的科学。根据题意填空:
(1)反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
①保持体积不变,充入N2使体系压强增大,其正反应速率____ ,逆反应速率____ 。
②保持压强不变,充入N2使容器的体积增大,其正反应速率____ ,逆反应速率____ 。
(2)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是____ (填“生石灰”或“盐酸”)。
(3)盛有浓硫酸的烧杯敞口放置一段时间,质量增加,则浓硫酸表现出_____ (填“吸水性”或“脱水性”)。
(4)浓硫酸与碳共热时发生反应2H2SO4(浓)+C CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出
CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出____ ,氧化产物是____ 。
(5)足量的Fe和稀硝酸反应的离子方程式为____ 。
(1)反应3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:①保持体积不变,充入N2使体系压强增大,其正反应速率
②保持压强不变,充入N2使容器的体积增大,其正反应速率
(2)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是
(3)盛有浓硫酸的烧杯敞口放置一段时间,质量增加,则浓硫酸表现出
(4)浓硫酸与碳共热时发生反应2H2SO4(浓)+C
 CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出
CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出(5)足量的Fe和稀硝酸反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】补齐物质及其用途的连线如A-b。_______
| 物质 | 用途。 |
| A.乙醇 | a.食品膨松剂 |
| B.浓硫酸 | b.燃料 |
| C.碳酸氢钠 | c.吸水剂 |
| D.蛋白质 | d.基本营养物质 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)写出正丁烷的结构简式:_______ ;
(2)胆矾晶体遇浓硫酸变白,体现了浓硫酸的_______ 性;
(3)写出铁和氯化铁溶液反应的离子方程式_______ ;
(4)根据所学的知识,试解释 比
比 热稳定性强的原因
热稳定性强的原因_______ 。
(1)写出正丁烷的结构简式:
(2)胆矾晶体遇浓硫酸变白,体现了浓硫酸的
(3)写出铁和氯化铁溶液反应的离子方程式
(4)根据所学的知识,试解释
 比
比 热稳定性强的原因
热稳定性强的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某小组同学设计实验实现几种价态硫元素的转化。
任务Ⅰ:从以下试剂中选择合适的试剂实现S(+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红溶液
(1)写出实现转化的化学方程式:___________ 。
任务Ⅱ:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2 Na2SO3溶液
Na2SO3溶液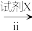 Na2S2O3溶液
Na2S2O3溶液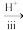 产生淡黄色沉淀和刺激性气味的气体
产生淡黄色沉淀和刺激性气味的气体
(2)过程ⅰ中加入的物质可以是___________ (任填一种化学式),该转化利用的是SO2具有___________ 的性质。
(3)过程ⅱ中试剂X为___________ (填“氧化剂”或“还原剂”)。
(4)写出过程ⅲ反应的离子方程式:___________ 。
任务Ⅰ:从以下试剂中选择合适的试剂实现S(+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红溶液
(1)写出实现转化的化学方程式:
任务Ⅱ:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2
 Na2SO3溶液
Na2SO3溶液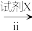 Na2S2O3溶液
Na2S2O3溶液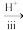 产生淡黄色沉淀和刺激性气味的气体
产生淡黄色沉淀和刺激性气味的气体(2)过程ⅰ中加入的物质可以是
(3)过程ⅱ中试剂X为
(4)写出过程ⅲ反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出BaSO4的名称:____ ,写出乙烷的结构简式:____ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:____ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是______________
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式______________________________ 。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是_________ ,反应中所消耗的硝酸的物质的量可能为______________
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为_____________________ 。
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,用相关化学用语回答下列问题:
(1)写出H、I两种元素的名称_____________ 、_____________ 。
(2)这些元素的气态氢化物中最稳定的是________________ ,元素A的最高价氧化物的分子式为____________ ,属于______________ 化合物(填离子或共价);
其电子式为_______________ ;其结构式为_______________ 。
(3)从E到K的元素中,______ 原子半径最小。元素E和J形成的化合物属于_______ 化合物(填离子或共价)
(4)试用实验证明E和F的金属性的强弱(简述实验内容和结论)_____________________________________________________________________________________________ 。
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H | I | J | K | L |
(1)写出H、I两种元素的名称
(2)这些元素的气态氢化物中最稳定的是
其电子式为
(3)从E到K的元素中,
(4)试用实验证明E和F的金属性的强弱(简述实验内容和结论)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,物质类别为横坐标的二维平面图象。如图为氯元素的价类二维图。

(1)氯元素在周期表中的位置___________ ,写出③的化学式___________ ,①中含有的化学键类型为___________ ,请用电子式表示物质⑤的形成过程___________ 。
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式___________ ,在该反应中浓盐酸体现了___________ 性。若制备标准状况下5.6L的物质②,则被氧化的HCl的质量为___________ 克。
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为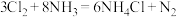 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目___________ 。

(1)氯元素在周期表中的位置
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为
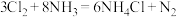 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素周期表的种类相当多,如大象式、回路式、能级式、亚历山大式等,教材上所附的长式周期表是目前使用最普遍的周期表。请回答下列问题:
(1)长式周期表中氢元素的位置争议最大,原因是_______
(2)有一种非常有趣的商业周期表如图所示。

①3:00时“时针”所指元素单质比11: 00时“时针”所指元素单质的还原性_______ (填“强”或“弱”)。
②8:00时“时针”和“分针”所指的两种元素形成的化合物所含化学键类型为_______ ,其与强酸溶液反应的离子方程式为 _______
(3)“亚历山大式周期表”的元素排列像一座连体三栋大楼(如图所示)。

下列有关其优点的说法中你不认可 的是_______ 。
A.较好地解决了氢元素所在族的问题
B.该周期表保留了长式周期表的优点,明确地表达周期律中族和周期的概念
C.携带和使用均比长才周期表方便
D.较好地处理了镧系和锕系元素,使周期表具有更好的连续性
(1)长式周期表中氢元素的位置争议最大,原因是
(2)有一种非常有趣的商业周期表如图所示。

①3:00时“时针”所指元素单质比11: 00时“时针”所指元素单质的还原性
②8:00时“时针”和“分针”所指的两种元素形成的化合物所含化学键类型为
(3)“亚历山大式周期表”的元素排列像一座连体三栋大楼(如图所示)。

下列有关其优点的说法中你
A.较好地解决了氢元素所在族的问题
B.该周期表保留了长式周期表的优点,明确地表达周期律中族和周期的概念
C.携带和使用均比长才周期表方便
D.较好地处理了镧系和锕系元素,使周期表具有更好的连续性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将下列分离各物质方法的代表字母填在横线上:
A.过滤;B.结晶;C.分液; D.萃取分液; E.蒸馏;F.升华
(1)除去食盐水中的泥沙_________ (2)除去植物油中的水_________
(3)将溶液中的硝酸钾与氯化钠分离_____ (4)将自来水制为纯净水________
A.过滤;B.结晶;C.分液; D.萃取分液; E.蒸馏;F.升华
(1)除去食盐水中的泥沙
(3)将溶液中的硝酸钾与氯化钠分离
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】选择合适的试剂(适量)对下列待提纯的物质进行除杂(括号内为杂质),并写出相应的化学方程式。
| 待提纯的物质 | 选用的试剂 | 相应化学方程式 |
| (1) N2 (CO2) | ||
| (2) C(CuO) | ||
| (3) NaNO3溶液(Na2SO4) |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】除杂:
①NaCl溶液中有少量的NaHCO3
方法____________________ 方程式为 ____________________
②小苏打溶液中有少量的苏打
方法____________________ 方程式为 ____________________
③碳酸钠溶液中有少量的碳酸氢钠
方法____________________ 方程式为 ____________________
④碳酸氢钠固体中有少量碳酸钠固体
方法____________________ 方程式为____________________
①NaCl溶液中有少量的NaHCO3
方法
②小苏打溶液中有少量的苏打
方法
③碳酸钠溶液中有少量的碳酸氢钠
方法
④碳酸氢钠固体中有少量碳酸钠固体
方法
您最近一年使用:0次

 主族
主族

