(1)写出BaSO4的名称:____ ,写出乙烷的结构简式:____ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:____ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:
更新时间:2020-06-02 11:39:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】有以下几种物质①熔融氯化钠 ②浓硫酸 ③Cu ④蔗糖 ⑤CH3COOH ⑥酒精 ⑦液溴,填空回答:(填序号)
(1)以上物质中属于强电解质的是______ ;属于非电解质的是_______ ;
(2)写出⑤在水中的电离方程式:_________________________ ;
(3)写出②与③共热时的化学反应方程式:_______________________ 。
(1)以上物质中属于强电解质的是
(2)写出⑤在水中的电离方程式:
(3)写出②与③共热时的化学反应方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】浓硫酸在下列用途和现象中所表现的性质是①沸点高、难挥发②酸性③吸水性④脱水性⑤强氧化性
| 用途或现象 | 体现浓硫酸的性质 |
| (1)浓硫酸使蓝矾变成白色 | |
| (2)浓硫酸使木条变黑 | |
| (3)浓硫酸制HCl | |
| (4)浓硫酸与铜片共热 | |
| (5)浓硫酸的木炭共热产生气体 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:
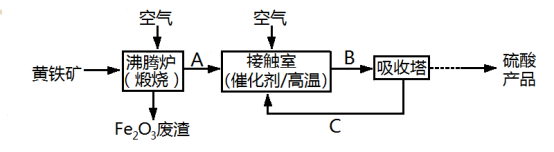
回答下列问题:
(1)在接触室中发生的反应是2SO2+O2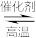 2SO3,该反应属于
2SO3,该反应属于_______ (填字母)
a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式_______ 。
(3)写出沸腾炉中发生反应的化学方程式:_______
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是_______ 。
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:_______ 。

回答下列问题:
(1)在接触室中发生的反应是2SO2+O2
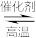 2SO3,该反应属于
2SO3,该反应属于a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式
(3)写出沸腾炉中发生反应的化学方程式:
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:_________________________________ 。
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式______________________________ 。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面____________ ,则发生了钝化;若铁棒表面________________ ,则未发生反应。
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):______________________________ 。
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:____________________________ 。
(6)制取硫酸铜有两种方法:方法一:2Cu+O2 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,
方法二:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:_____________________________________________ (答任一点)。
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:
(6)制取硫酸铜有两种方法:方法一:2Cu+O2
 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,方法二:Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚硫酸钠是工业上常用的还原剂,容易被空气氧化成硫酸钠。检验亚硫酸钠样品中是否含有硫酸钠的方法是:取少量亚硫酸钠样品溶于水,然后_______________________________________ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2价、0价、+4价、+6价四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式___ 。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现___ (选填“氧化性”、“还原性”)
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是___ 。
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫___ (性质)。
(5)硫酸盐的种类很多且应用广泛,医疗上采用___ 作X射线透视肠胃的内服药剂。
(1)写出硫与铁反应的化学方程式
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫
(5)硫酸盐的种类很多且应用广泛,医疗上采用
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】乙烯在化工生产领域应用广泛。
(1)乙烯能合成很多有实用价值的有机物。___________ (写化学式)。
②反应I的反应类型是___________ 。
(2)以原油为起始原料合成聚乙烯的路线如下图所示。
原油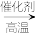 C4H10
C4H10 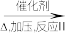 CH2=CH2
CH2=CH2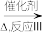 聚乙烯
聚乙烯
①反应Ⅱ的化学方程式是___________ 。
②写出分子式符合C4H10的有机物的结构简式:___________ 。
(1)乙烯能合成很多有实用价值的有机物。
CH3CH2Cl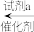 CH2=CH2
CH2=CH2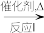

②反应I的反应类型是
(2)以原油为起始原料合成聚乙烯的路线如下图所示。
原油
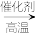 C4H10
C4H10 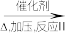 CH2=CH2
CH2=CH2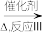 聚乙烯
聚乙烯①反应Ⅱ的化学方程式是
②写出分子式符合C4H10的有机物的结构简式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ、如图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都与氢原子结合。
(1)图中属于烷烃的是______ (填字母)。
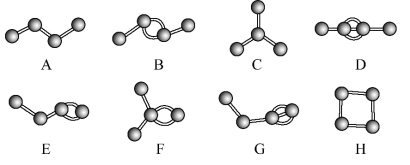
(2) 上图中互为同分异构体的是A与____ ;B与_____ ;D与____ (填字母)。
Ⅱ、等物质的量的乙烯与甲烷,所含分子数之比_____ ,碳原子个数之比为_____ ,若充分燃烧,消耗O2的体积比为______ ;0.1 mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6 mol,则该烃的分子式为______ 。
(1)图中属于烷烃的是

(2) 上图中互为同分异构体的是A与
Ⅱ、等物质的量的乙烯与甲烷,所含分子数之比
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】近年来随着机动车经济的飞速发展,机动车的生产和使用量急剧增长,机动车排放的尾气对环境的污染日趋严重,机动车排气污染对环境和人们身体健康的危害已相当严重。汽车尾气的主要成分包括一氧化碳、二氧化碳、二氧化硫、一氧化氮、氮气以及铅和碳氢化合物等。回答下列问题:
(1)CO、CO2、SO2、NO几种气体中属于酸性氧化物的是____ (填化学式),CO2的结构式为____ 。
(2)Pb2+的离子结构示意图如图所示,由此可知铅在元素周期表中的位置为____ 。

(3)汽车尾气中的一种碳氢化合物其化学式为C8H18,写出该碳氢化合物分子含有6个甲基的结构简式____ ,该结构的二氯代物有____ 种。
(4)为了测定尾气中SO2的含量,某同学将汽车尾气缓慢通入盛有500mL0.1mol·L-1酸性KMnO4溶液的容器中,若通入尾气的气速为16L·min-1,经过5min溶液恰好完全褪色,假定尾气中的SO2被充分吸收且尾气中其他物质不与酸性KMnO4溶液反应,则SO2与酸性KMnO4溶液反应的离子方程式为____ ,该尾气中SO2的含量为____ g·L-1。
(1)CO、CO2、SO2、NO几种气体中属于酸性氧化物的是
(2)Pb2+的离子结构示意图如图所示,由此可知铅在元素周期表中的位置为

(3)汽车尾气中的一种碳氢化合物其化学式为C8H18,写出该碳氢化合物分子含有6个甲基的结构简式
(4)为了测定尾气中SO2的含量,某同学将汽车尾气缓慢通入盛有500mL0.1mol·L-1酸性KMnO4溶液的容器中,若通入尾气的气速为16L·min-1,经过5min溶液恰好完全褪色,假定尾气中的SO2被充分吸收且尾气中其他物质不与酸性KMnO4溶液反应,则SO2与酸性KMnO4溶液反应的离子方程式为
您最近半年使用:0次



