浓硫酸在下列用途和现象中所表现的性质是①沸点高、难挥发②酸性③吸水性④脱水性⑤强氧化性
| 用途或现象 | 体现浓硫酸的性质 |
| (1)浓硫酸使蓝矾变成白色 | |
| (2)浓硫酸使木条变黑 | |
| (3)浓硫酸制HCl | |
| (4)浓硫酸与铜片共热 | |
| (5)浓硫酸的木炭共热产生气体 |
更新时间:2019-04-22 09:46:00
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸在下列用途或反应中各表现的性质主要是(用字母填在横线上)
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性
(1)浓硫酸滴在白纸上,过一会儿,白纸变黑。_______
(2)长期敞口放置浓硫酸时,质量增加。_______
(3)氧化铁粉末投入稀硫酸中,溶液呈黄色。_______
(4)把铜片放入浓硫酸里加热,有气体产生。_______
(5)利用浓硫酸和食盐固体反应可制HCl气体。_______
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性
(1)浓硫酸滴在白纸上,过一会儿,白纸变黑。
(2)长期敞口放置浓硫酸时,质量增加。
(3)氧化铁粉末投入稀硫酸中,溶液呈黄色。
(4)把铜片放入浓硫酸里加热,有气体产生。
(5)利用浓硫酸和食盐固体反应可制HCl气体。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】实验室制取下列气体时,应选用下列哪种酸:
A.浓盐酸B.稀盐酸 C.稀硫酸D.浓硫酸
用大理石和___________ 制 CO2;用食盐和___________ 制HCl。
A.浓盐酸B.稀盐酸 C.稀硫酸D.浓硫酸
用大理石和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组利用如图装置探究足量Zn与一定量浓硫酸反应后的气体产物成分(水蒸气除外).

(1)A中发生反应的化学方程式为_______________ 。
(2)按气流方向,仪器的连接顺序为(a)→( ) ( ) →( ) ( ) →( ) ( ) →( ) ( ) →尾气处理(填仪器接口字母编号)。
(3)盛放浓硫酸的仪器名称为________ ;该仪器在使用前应洗净并______________ 。
(4)试剂X为_________________ 。
(5)装置E的作用为____________________ 。
(6)装置C的作用为________ ;证明该装置中反应可逆性的实验操作及现象为_____________ 。
(7)实验时,应使A装置中物质先反应一段时间,再点燃B处酒精灯,原因为___________ 。

(1)A中发生反应的化学方程式为
(2)按气流方向,仪器的连接顺序为(a)→
(3)盛放浓硫酸的仪器名称为
(4)试剂X为
(5)装置E的作用为
(6)装置C的作用为
(7)实验时,应使A装置中物质先反应一段时间,再点燃B处酒精灯,原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫酸是中学化学实验室的常见药品,其性质有①酸性 ②吸水性 ③脱水性 ④强氧化性,请将序号填在相应的横线上:
(1)锌和稀H2SO4制H2________ ;
(2)浓硫酸作干燥剂________ ;
(3)浓硫酸使蔗糖炭化并产生刺激性气味气体________ ;
(4)浓硫酸与铜的反应________ ;(5)浓硫酸使硫酸铜晶体变白________ ;
(6)浓硫酸使湿润的蓝色石蕊试纸先变红,后来又变黑________ 。
(1)锌和稀H2SO4制H2
(2)浓硫酸作干燥剂
(3)浓硫酸使蔗糖炭化并产生刺激性气味气体
(4)浓硫酸与铜的反应
(6)浓硫酸使湿润的蓝色石蕊试纸先变红,后来又变黑
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】浓硫酸溶液具有①酸性;②强氧化性;③吸水性;④脱水性等性质,根据题意填空(填序号):
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有_______ ;
(2)浓H2SO4与Cu反应,体现了浓H2SO4的_______ 。
(3)将浓硫酸滴到胆矾上,胆矾变白,是因为浓硫酸具有_______ ;
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有
(2)浓H2SO4与Cu反应,体现了浓H2SO4的
(3)将浓硫酸滴到胆矾上,胆矾变白,是因为浓硫酸具有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有____________ 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有______________ 性。
用玻璃棒蘸取浓硝酸滴在pH试纸上,试纸逐渐变白,这种漂白现象说明浓硝酸具有_______ 性。
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是__________ (填序号)。
①Cu + HNO3(浓)→ Cu(NO3)2
②Cu + HNO3(稀)→ Cu(NO3)2
③Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
(3)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_____________ 。
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况) (不考虑N2O4),则所耗HNO3的物质的量____________ mol.
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为____________________________________________ 。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
用玻璃棒蘸取浓硝酸滴在pH试纸上,试纸逐渐变白,这种漂白现象说明浓硝酸具有
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是
①Cu + HNO3(浓)→ Cu(NO3)2
②Cu + HNO3(稀)→ Cu(NO3)2
③Cu
 CuO
CuO Cu(NO3)2
Cu(NO3)2(3)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况) (不考虑N2O4),则所耗HNO3的物质的量
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】将下列性质的选项,填入各小题后面对应的括号中:A.脱水性;B.强酸性;C.二元酸;D.氧化性;E.吸水性
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色。( )
(2)NaOH与H2SO4反应,可生成Na2SO4和NaHSO4这两种盐。( )
(3)在冷浓HNO3中放入铝片没明显现象。( )
(4)浓H2SO4敞口久置会增重。( )
(5)用稀硫酸清洗金属表面的氧化物( )
(6)在烧杯中放入蔗糖,滴入浓H2SO4变黑,并产生大量气体。( )
(7)在稀HNO3中放入铜片产生NO。( )
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色。
(2)NaOH与H2SO4反应,可生成Na2SO4和NaHSO4这两种盐。
(3)在冷浓HNO3中放入铝片没明显现象。
(4)浓H2SO4敞口久置会增重。
(5)用稀硫酸清洗金属表面的氧化物
(6)在烧杯中放入蔗糖,滴入浓H2SO4变黑,并产生大量气体。
(7)在稀HNO3中放入铜片产生NO。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体___________ 。
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸___________ 。
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体___________ 。
(4)常温下可以用铁或铝的容器贮存浓硫酸___________ 。
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末___________ 。
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体___________ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体
(4)常温下可以用铁或铝的容器贮存浓硫酸
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的__________ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种___________ (填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的化学方程式:_____________ 。
II.氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)在空气质量报告的各项指标中,有SO2和NO2的指数,SO2是一种无色有毒气体,NO2是一种_________ (填“无色”或“红棕色”)有毒气体;
(2)氨气极易溶于水,其水溶液显__________ (填“酸”、“碱”或“中”)性;
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
III.乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为__________ ;
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸_____ 碳酸(填“>”或“<”);
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH + CH3CH2OH CH3COOCH2CH3+
CH3COOCH2CH3+________ 。
(1)钠在空气中燃烧生成淡黄色的
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的化学方程式:
II.氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)在空气质量报告的各项指标中,有SO2和NO2的指数,SO2是一种无色有毒气体,NO2是一种
(2)氨气极易溶于水,其水溶液显
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出III.乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH + CH3CH2OH
 CH3COOCH2CH3+
CH3COOCH2CH3+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在一定体积的 的浓硫酸中加入过量铜片,加热使之充分反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积
的浓硫酸中加入过量铜片,加热使之充分反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积_______ (填“大于”“等于”或“小于”)180mL。
(2)将 投入到150mL某浓度的稀硫酸中,再投入7g铁粉,充分反应后,共收集到
投入到150mL某浓度的稀硫酸中,再投入7g铁粉,充分反应后,共收集到 (标准状况下),同时,Fe和
(标准状况下),同时,Fe和 均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗
均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗 的NaOH溶液150mL。则原硫酸溶液的物质的量浓度为
的NaOH溶液150mL。则原硫酸溶液的物质的量浓度为_______ 。
 的浓硫酸中加入过量铜片,加热使之充分反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积
的浓硫酸中加入过量铜片,加热使之充分反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积(2)将
 投入到150mL某浓度的稀硫酸中,再投入7g铁粉,充分反应后,共收集到
投入到150mL某浓度的稀硫酸中,再投入7g铁粉,充分反应后,共收集到 (标准状况下),同时,Fe和
(标准状况下),同时,Fe和 均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗
均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗 的NaOH溶液150mL。则原硫酸溶液的物质的量浓度为
的NaOH溶液150mL。则原硫酸溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题。
I.以下是生产、生活中常见的物质。①冰醋酸;② ;③
;③ ;④干冰;⑤
;④干冰;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧浓硫酸;⑨蔗糖。
;⑦石墨;⑧浓硫酸;⑨蔗糖。
(1)属于强电解质的有___________ ,属于非电解质的有___________ 。(用序号填空)
(2)写出⑥的电离方程式:___________ 。
(3)将⑧与⑨混合,观察到混合物变黑,体积迅速膨胀,产生刺激性气味,该过程中体现的物质⑧的性质有___________ 。
(4)常温下, 均为
均为 的①溶液和⑥溶液,加水稀释100倍,pH较大的是
的①溶液和⑥溶液,加水稀释100倍,pH较大的是___________ 。(用序号填空)
Ⅱ.常温下几种酸的电离平衡常数如表:
(5)常温下,0.1mol/L的HCN溶液中, 约为
约为___________ 。
(6)根据电离平衡常数判断,以下反应不能进行的是___________。
I.以下是生产、生活中常见的物质。①冰醋酸;②
 ;③
;③ ;④干冰;⑤
;④干冰;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧浓硫酸;⑨蔗糖。
;⑦石墨;⑧浓硫酸;⑨蔗糖。(1)属于强电解质的有
(2)写出⑥的电离方程式:
(3)将⑧与⑨混合,观察到混合物变黑,体积迅速膨胀,产生刺激性气味,该过程中体现的物质⑧的性质有
(4)常温下,
 均为
均为 的①溶液和⑥溶液,加水稀释100倍,pH较大的是
的①溶液和⑥溶液,加水稀释100倍,pH较大的是Ⅱ.常温下几种酸的电离平衡常数如表:
| 酸 | HCOOH | HCN |  |
 |  | 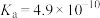 |  , , |
 约为
约为(6)根据电离平衡常数判断,以下反应不能进行的是___________。
A. | B.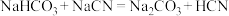 |
C. | D. |
您最近一年使用:0次



