工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:
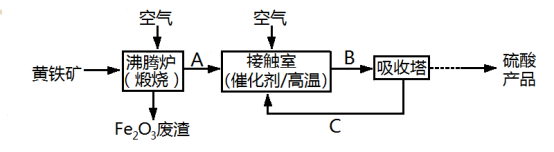
回答下列问题:
(1)在接触室中发生的反应是2SO2+O2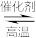 2SO3,该反应属于
2SO3,该反应属于_______ (填字母)
a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式_______ 。
(3)写出沸腾炉中发生反应的化学方程式:_______
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是_______ 。
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:_______ 。

回答下列问题:
(1)在接触室中发生的反应是2SO2+O2
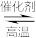 2SO3,该反应属于
2SO3,该反应属于a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式
(3)写出沸腾炉中发生反应的化学方程式:
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
更新时间:2021-04-02 07:45:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】配平下列氧化还原反应方程式:
(1)Mn2++O2+OH-→MnO(OH)2↓___
(2)MnO(OH)2+I-+H+→Mn2++I2+H2O___
(1)Mn2++O2+OH-→MnO(OH)2↓
(2)MnO(OH)2+I-+H+→Mn2++I2+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二氧化氯是黄绿色的气体,可用于水体消毒与废水处理.一种制备方法为:
完成下列填空:
(1)配平上述反应方程式,该反应的还原产物是______ .
(2)该反应每产生0.2mol ClO2,需要消耗草酸晶体(H2C2O4•2H2O)_____ g.
(3)上述反应物中属于第三周期的元素的原子半径大小顺序是______ ,其中原子半径最大的元素最外层电子云形状为______ .
(4)二氧化氯具有强氧化性,能漂白有色物质,其漂白原理与_______ 相同.(写一种)
(5)二氧化氯能净化有毒废水中的氰化钠(NaCN),生成NaCl、CO2和N2,请写出此反应的离子方程式:__________ .
(6)上述反应产物NaCl中含有______ 键,工业上用电解熔融的氯化钠制备金属钠,氯气在_____ (写电极名称)产生.
完成下列填空:
(1)配平上述反应方程式,该反应的还原产物是
(2)该反应每产生0.2mol ClO2,需要消耗草酸晶体(H2C2O4•2H2O)
(3)上述反应物中属于第三周期的元素的原子半径大小顺序是
(4)二氧化氯具有强氧化性,能漂白有色物质,其漂白原理与
(5)二氧化氯能净化有毒废水中的氰化钠(NaCN),生成NaCl、CO2和N2,请写出此反应的离子方程式:
(6)上述反应产物NaCl中含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硫的氧化物、氮的氧化物是常见的大气污染物。
(1)酸雨是降水呈酸性(pH小于5.6)统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107kg。NO2溶于水发生反应的化学方程式为:___________ 。
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中氮的氧化物用______ 吸收,写出NO2与之反应的离子方程式_____ 。
(2)某化学兴趣小组选用如图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
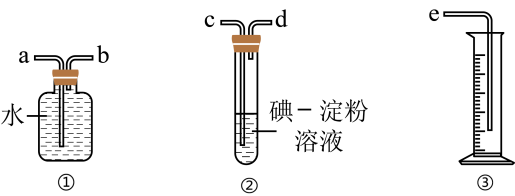
①若原料气从左向右流时,上述装置连接的顺序是______ (填字母)。
②装置②中发生反应的离子方程式为:______ ;当装置②中出现_______ 现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是__________ 。
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(1)酸雨是降水呈酸性(pH小于5.6)统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107kg。NO2溶于水发生反应的化学方程式为:
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中氮的氧化物用
(2)某化学兴趣小组选用如图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。

①若原料气从左向右流时,上述装置连接的顺序是
②装置②中发生反应的离子方程式为:
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图是几种烃的球棍模型和空间填充模型,试回答下列问题:_______ 。
(2)若将D通入溴的四氯化碳溶液中,反应的化学方程式为_______ 。
(3)在一定条件下,D能与水反应生成的有机物的结构简式是_______ ,其反应类型是_______ 。
(4)用 取代D中一个氢原子后得到物质F,F在催化剂条件下发生加聚反应生成一种高分子材料,该高分子材料主要用于家用电器、塑料管材、高透材料等方面。写出F发生加聚反应的化学方程式
取代D中一个氢原子后得到物质F,F在催化剂条件下发生加聚反应生成一种高分子材料,该高分子材料主要用于家用电器、塑料管材、高透材料等方面。写出F发生加聚反应的化学方程式_______ 。
(5)等物质的量的下列烃完全燃烧,消耗氧气的物质的量最多的是_______ (填序号)。
① ②
②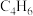 ③
③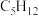 ④
④
(6)下列化学反应原理相同的是_______ (填序号)。
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
② 使溴水和酸性高锰酸钾溶液褪色
使溴水和酸性高锰酸钾溶液褪色
③ 使品红溶液和滴有酚酞的NaOH溶液褪色
使品红溶液和滴有酚酞的NaOH溶液褪色
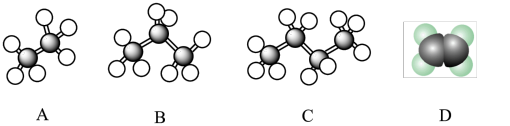
(2)若将D通入溴的四氯化碳溶液中,反应的化学方程式为
(3)在一定条件下,D能与水反应生成的有机物的结构简式是
(4)用
 取代D中一个氢原子后得到物质F,F在催化剂条件下发生加聚反应生成一种高分子材料,该高分子材料主要用于家用电器、塑料管材、高透材料等方面。写出F发生加聚反应的化学方程式
取代D中一个氢原子后得到物质F,F在催化剂条件下发生加聚反应生成一种高分子材料,该高分子材料主要用于家用电器、塑料管材、高透材料等方面。写出F发生加聚反应的化学方程式(5)等物质的量的下列烃完全燃烧,消耗氧气的物质的量最多的是
①
 ②
②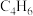 ③
③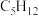 ④
④
(6)下列化学反应原理相同的是
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②
 使溴水和酸性高锰酸钾溶液褪色
使溴水和酸性高锰酸钾溶液褪色③
 使品红溶液和滴有酚酞的NaOH溶液褪色
使品红溶液和滴有酚酞的NaOH溶液褪色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知铜和浓硫酸可以在加热条件下发生反应(已配平): 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题
(1)此反应中,硫酸体现了___________ 性和___________ 性。
(2)A物质可以导致酸雨的形成。A应该属于___________ 。(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)___________ 失去电子,氧化剂是___________ 。
 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题(1)此反应中,硫酸体现了
(2)A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硫酸或硝酸在下列用途或反应中各表现的性质是:
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末__________ ;
(2)用铝槽车装运浓硫酸或浓硝酸__________ ;
(3)蔗糖中加入浓硫酸,形成“黑色发糕”__________ ;
(4)浓硝酸久置会变黄____________________ ;
(5)浓硝酸与不活泼金属铜单质反应_____ ;
(6)98%以上的浓硝酸俗称“发烟硝酸”________ 。
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末
(2)用铝槽车装运浓硫酸或浓硝酸
(3)蔗糖中加入浓硫酸,形成“黑色发糕”
(4)浓硝酸久置会变黄
(5)浓硝酸与不活泼金属铜单质反应
(6)98%以上的浓硝酸俗称“发烟硝酸”
您最近一年使用:0次

 +
+ +
+

