盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是______________
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式______________________________ 。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是_________ ,反应中所消耗的硝酸的物质的量可能为______________
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为_____________________ 。
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为
10-11高三上·浙江杭州·期中 查看更多[1]
(已下线)2011届浙江省杭州市七校高三上学期期中考试化学卷
更新时间:2010-11-22 09:02:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③ 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
上述状态下的物质中,能导电的有___________ (填序号,下同),属于电解质的有___________ 。
(2)已知H3PO2是一元弱酸,NaH2PO2属于___________ (填:酸式盐、正盐或者碱式盐)。写出H3PO2与足量NaOH溶液反应的离子方程式:___________
(3)某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: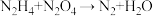 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
①配平该方程式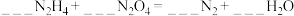 。
。___________
②该反应中,氧化产物与还原产物的质量之比为___________ 。
(4)补全并配平下列方程式
①_______ _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
___________
②______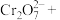 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________ ___________
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③
 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。上述状态下的物质中,能导电的有
(2)已知H3PO2是一元弱酸,NaH2PO2属于
(3)某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: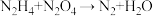 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。①配平该方程式
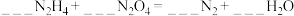 。
。②该反应中,氧化产物与还原产物的质量之比为
(4)补全并配平下列方程式
①_______
 _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
②______
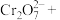 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】过渡元素现代社会得到广泛应用。请回答下列问题:
(1)稀土金属包括______ 、钇和钪,在合金中加入稀土金属,能大大改善合金的性能,稀土金属被称为“冶金工业的维生素”。
(2)钼系催化剂:(NH4)2O·4MoO3·2H2O主要用于石油炼制和化学工业中。高温用H2还原(NH4)2O·4MoO3·2H2O得金属钼,氧化剂与还原剂物质的量之比为______ 。
(3)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:______ 。
(4)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:______ 。(高锰酸根离子的还原产物为Mn2+)
(5)V2O5是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为______ 。
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:______ 。
(1)稀土金属包括
(2)钼系催化剂:(NH4)2O·4MoO3·2H2O主要用于石油炼制和化学工业中。高温用H2还原(NH4)2O·4MoO3·2H2O得金属钼,氧化剂与还原剂物质的量之比为
(3)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了
 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(4)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:
(5)V2O5是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在浓硝酸中放入铜片:
(1)开始反应的离子方程式为___________ ,实验现象为___________ 。
(2)若铜有剩余,则反应将要结束时的离子方程式为___________ 。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是______________________ 。
(4)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标准状况下),则所消耗硝酸的物质的量是___________ 。
(1)开始反应的离子方程式为
(2)若铜有剩余,则反应将要结束时的离子方程式为
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是
(4)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标准状况下),则所消耗硝酸的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列各题内容:
(1)写出下列物质的电子式:
①过氧化钠:_______
②氢氧化钠:_____
③二氧化碳:_______
④水:_____
(2)写出下列符合要求的离子方程式 :
①稀硝酸与铜反应:_____
②稀硝酸与硫酸亚铁溶液反应:_____
(3)写出下列符合要求的化学反应方程式:
③碳与浓硝酸反应:_____
④氯化铵与消石灰制氨气:_____
(1)写出下列物质的电子式:
①过氧化钠:
②氢氧化钠:
③二氧化碳:
④水:
(2)写出下列符合要求的
①稀硝酸与铜反应:
②稀硝酸与硫酸亚铁溶液反应:
(3)写出下列符合要求的化学反应方程式:
③碳与浓硝酸反应:
④氯化铵与消石灰制氨气:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:_________________________________ 。
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式______________________________ 。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面____________ ,则发生了钝化;若铁棒表面________________ ,则未发生反应。
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):______________________________ 。
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:____________________________ 。
(6)制取硫酸铜有两种方法:方法一:2Cu+O2 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,
方法二:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:_____________________________________________ (答任一点)。
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:
(6)制取硫酸铜有两种方法:方法一:2Cu+O2
 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,方法二:Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用如图可以从不同角度研究含硫物质的性质及其转化关系。
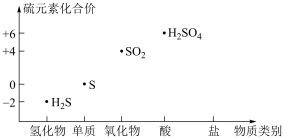
回答下列问题:
(1)H2S与SO2反应的化学方程式为____ ,反应中H2S体现____ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____ ,下列试剂不能用于验证生成物中含有SO2的是____ (填标号)。
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<____ 的雨水,其中NOx的排放也会导致酸雨的形成,写出NO2与水反应的化学方程式____ 。
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式____ 。

回答下列问题:
(1)H2S与SO2反应的化学方程式为
(2)加热时,浓硫酸与木炭反应的化学方程式为
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.地壳中的硅元素在现代高科技产品中占有重要位置,足见化学对现代文明的重要作用。例如:
(1)计算机芯片的主要成分是___________ 。
(2)工业上制取粗硅的化学方程式为___________ ;光导纤维遇到强碱易被腐蚀,请写出该物质与氢氧化钠溶液反应的化学方程式___________ 。
(3)下列物质的主要成份不属于硅酸盐的是___________(填字母)。
Ⅱ.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(4)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出___________ 性。
(5)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是___________ 。
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI
(6)在加热条件下,浓硫酸能与Cu反应,表现___________ 。请写出这个化学反应的化学方程式___________ 。
(1)计算机芯片的主要成分是
(2)工业上制取粗硅的化学方程式为
(3)下列物质的主要成份不属于硅酸盐的是___________(填字母)。
| A.陶瓷 | B.玻璃 | C.水泥 | D.碳化硅陶瓷 |
Ⅱ.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(4)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出
(5)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI
(6)在加热条件下,浓硫酸能与Cu反应,表现
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3=3Cu(NO3)2+2NO ↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目__________
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是___________ mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________ 。
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是
(3)被还原的硝酸占参加反应硝酸的比例为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在盛有一定量浓硝酸的试管中加入6.4 g铜片发生反应。请回答:
(1)开始阶段,观察到的现象为________________ ,反应的化学方程式是_____________ 。
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是__________________ 。
(3)若6.4 g铜片消耗完时,共产生气体2.8 L(标准状况)。则整个反应过程中所消耗的硝酸的物质的量是_____________ 。
(4)实验室中硝酸通常保存在棕色试剂瓶中,原因是_____________ (用化学方程式表示)。
(5)工业上通常用氨催化氧化法制硝酸,写出氨催化氧化的化学方程式:_______________ 。
(1)开始阶段,观察到的现象为
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是
(3)若6.4 g铜片消耗完时,共产生气体2.8 L(标准状况)。则整个反应过程中所消耗的硝酸的物质的量是
(4)实验室中硝酸通常保存在棕色试剂瓶中,原因是
(5)工业上通常用氨催化氧化法制硝酸,写出氨催化氧化的化学方程式:
您最近一年使用:0次



