价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,物质类别为横坐标的二维平面图象。如图为氯元素的价类二维图。

(1)氯元素在周期表中的位置___________ ,写出③的化学式___________ ,①中含有的化学键类型为___________ ,请用电子式表示物质⑤的形成过程___________ 。
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式___________ ,在该反应中浓盐酸体现了___________ 性。若制备标准状况下5.6L的物质②,则被氧化的HCl的质量为___________ 克。
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为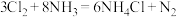 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目___________ 。

(1)氯元素在周期表中的位置
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为
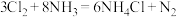 ,请用单线桥法表示出该反应转移电子的方向和数目
,请用单线桥法表示出该反应转移电子的方向和数目
更新时间:2022-03-26 19:04:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E、G六种元素,原子序数依次增大。A的简单气态氢化物能与其最高价含氧酸反应生成盐:B原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;C是短周期中原子半径最大的主族元素;D元素3p能级有两个空轨道;E是所在周期电负性最大的元素:G是第四周期未成对电子数最多的元素
(1)G在元素周期表中第四周期、________ 族、______ 区;第二电离能: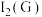
______ 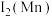 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
(2)B、C、D、E四种元素形成的简单离子半径由小到大的顺序为___________ (填离子符号)。
(3)A与E形成的化合物的电子式为___________ 。
(4)写出D的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式___________ 。
(5)写出A的最高价氧化物对应水化物的稀溶液与过量Fe反应的离子方程式___________ 。
(1)G在元素周期表中第四周期、
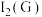
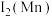 (填“>”或“<”),原因是
(填“>”或“<”),原因是(2)B、C、D、E四种元素形成的简单离子半径由小到大的顺序为
(3)A与E形成的化合物的电子式为
(4)写出D的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式
(5)写出A的最高价氧化物对应水化物的稀溶液与过量Fe反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】消毒剂在生产生活中有极重要的作用,广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)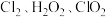 (还原产物为
(还原产物为 )、
)、 (1 mol
(1 mol  转化为1 mol
转化为1 mol  和1 mol
和1 mol  )等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。
)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。
(2) 有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:
有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现: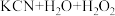 =
=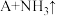 ,则生成物A的化学式为
,则生成物A的化学式为_______ , 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是_______ , 的结构式是
的结构式是_______ 。
(3)漂白剂亚氯酸钠( )在常温、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。该反应中,有1 mol
(未配平)。该反应中,有1 mol  生成转移的电子数约为
生成转移的电子数约为_______ 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______ (用离子方程式表示)。利用氯碱工业的产物可生产“84”消毒液,写出有关反应的化学方程式:_______ 。
(1)
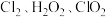 (还原产物为
(还原产物为 )、
)、 (1 mol
(1 mol  转化为1 mol
转化为1 mol  和1 mol
和1 mol  )等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。
)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。A. | B. | C. | D. |
 有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:
有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现: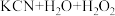 =
=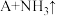 ,则生成物A的化学式为
,则生成物A的化学式为 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是 的结构式是
的结构式是(3)漂白剂亚氯酸钠(
 )在常温、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。该反应中,有1 mol
(未配平)。该反应中,有1 mol  生成转移的电子数约为
生成转移的电子数约为(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
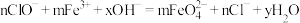 ,回答下列问题:
,回答下列问题:
(1)上述反应中的
___________ ,
___________ 。
(2)上述反应中还原产物为___________ ,氧化性强弱:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)请用双线桥法表示以下反应中电子的转移情况:___________ 。
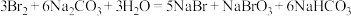
 )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: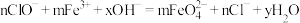 ,回答下列问题:
,回答下列问题:(1)上述反应中的


(2)上述反应中还原产物为

 (填“>”或“<”)。
(填“>”或“<”)。(3)请用双线桥法表示以下反应中电子的转移情况:
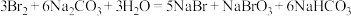
您最近一年使用:0次
【推荐2】I.完成下列氧化还原反应相关问题。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出___________ (填“氧化性”或“还原性”)。
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为___________ (填化学式)。
(4)浓盐酸在该反应中显示出来的性质是___________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为___________ 。还原性:
___________ Cl−(填“>”“<”或“=”)。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为
(4)浓盐酸在该反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO
 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为
您最近一年使用:0次
【推荐3】高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是_______ ,氧化产物是_______ 。
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:_____ 。
_______Fe(OH)3+_______ClO−+_______OH−=_______ +_______Cl−+_______H2O。
+_______Cl−+_______H2O。
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4_______ (填“>”或“<”)Cl2。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:
_______Fe(OH)3+_______ClO−+_______OH−=_______
 +_______Cl−+_______H2O。
+_______Cl−+_______H2O。(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知溶液中还原性: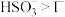 ,氧化性:
,氧化性: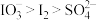
(1)在 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______ 。
_______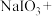 _______
_______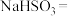 _______
_______ _______
_______ _______
_______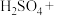 _______
_______
该反应中还原剂是_______ (填化学式),被还原的元素是_______ (填名称)。
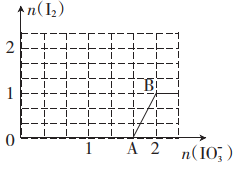
(2)在含5mol 的溶液中逐滴加入
的溶液中逐滴加入 溶液。加入
溶液。加入 的物质的量和析出
的物质的量和析出 单质的物质的量的关系曲线如图所示。写出反应过程中OA段、AB段曲线分别对应的离子方程式:
单质的物质的量的关系曲线如图所示。写出反应过程中OA段、AB段曲线分别对应的离子方程式:_______ 、_______ 。
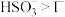 ,氧化性:
,氧化性: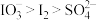
(1)在
 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______
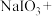 _______
_______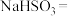 _______
_______ _______
_______ _______
_______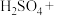 _______
_______
该反应中还原剂是
(2)在含5mol
 的溶液中逐滴加入
的溶液中逐滴加入 溶液。加入
溶液。加入 的物质的量和析出
的物质的量和析出 单质的物质的量的关系曲线如图所示。写出反应过程中OA段、AB段曲线分别对应的离子方程式:
单质的物质的量的关系曲线如图所示。写出反应过程中OA段、AB段曲线分别对应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在。由于金红石熔点高,为金属Ti的直接制备带来了困难。在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法。金红石转化成TiCl4的反应方程式如下:TiO2+2C+2Cl2=TiCl4+2CO。
(1)指出发生还原反应的是___________ ,氧化产物是_____ 。
(2)用双线桥法标出电子转移_____ 。
(3)当有6mol电子转移,则有___________ molC被氧化。
(1)指出发生还原反应的是
(2)用双线桥法标出电子转移
(3)当有6mol电子转移,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界_______ 。

(2)表中所列元素,属于短周期主族元素有_______ ;g元素在周期表的位置_______ ;26号元素周期表的位置_______ 。
(3)元素e的原子结构示意图_______ ,最高价氧化物的水化物的名称_______ ,请在方框中按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量_______ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界

(2)表中所列元素,属于短周期主族元素有
(3)元素e的原子结构示意图

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
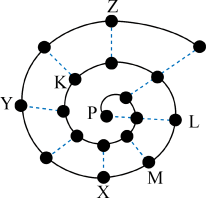
(1)X元素符号为__________________ 。
(2)M与Z两种元素形成的化合物含有的化学键为________________ 。
(3)下列说法正确的是__________________ 。
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键

(1)X元素符号为
(2)M与Z两种元素形成的化合物含有的化学键为
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次

 MnCl2 + Cl2↑+ 2H2O,回答下列问题:
MnCl2 + Cl2↑+ 2H2O,回答下列问题:

