I.完成下列氧化还原反应相关问题。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出___________ (填“氧化性”或“还原性”)。
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为___________ (填化学式)。
(4)浓盐酸在该反应中显示出来的性质是___________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为___________ 。还原性:
___________ Cl−(填“>”“<”或“=”)。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为
(4)浓盐酸在该反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO
 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为
更新时间:2023-12-31 21:07:46
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成球。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
(1)请完成上述火法炼锌反应的化学方程式:ZnCO3+ _______ _______ + _______ CO↑
_______ + _______ CO↑
_______
(2)在该反应中,还原剂是_______ (填化学式,下同),被还原的是_______ 。
(1)请完成上述火法炼锌反应的化学方程式:ZnCO3+ _______
 _______ + _______ CO↑
_______ + _______ CO↑(2)在该反应中,还原剂是
您最近一年使用:0次
【推荐2】根据表格信息,解答有关问题。
(1)在浓盐酸中加入少量KMnO4剧烈反应,产生黄绿色有刺激性气味的气体,溶液紫红色褪去,已知该反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑。其中氧化剂是____ ,氧化产物是____ 。每生成71g氯气,则被氧化的还原剂的质量为___ g。
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
滴加适量H2O2,紫红色褪去,并有无色气泡产生;再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
①在配制酸性KMnO4溶液时,能否用盐酸?____ ,原因是____ 。
②KMnO4、H2O2、PbO2的氧化性由强到弱的顺序为_____ 。
(3)根据上述反应能否比较Cl2与H2O2的氧化性强弱?_____ (填“能”或“不能”)。
| 氯气(Cl2) | KMnO4 | PbO2 |
| 有刺激性气味,呈黄绿色,有毒气体 | 易溶于水,溶液呈紫红色,可用于杀菌消毒 | Pb的最高化合价为+4,其稳定化合价为+2,难溶于水,灰色固体 |
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
滴加适量H2O2,紫红色褪去,并有无色气泡产生;再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
①在配制酸性KMnO4溶液时,能否用盐酸?
②KMnO4、H2O2、PbO2的氧化性由强到弱的顺序为
(3)根据上述反应能否比较Cl2与H2O2的氧化性强弱?
您最近一年使用:0次
【推荐3】氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)“维生素 可以将食物中的
可以将食物中的 转化为
转化为 ”,说明维生素
”,说明维生素
___________ 具有(填“氧化性”或“还原性”)。
(2) 常用检查输送
常用检查输送 的管道是否,其反应如下:___
的管道是否,其反应如下:___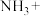 ___
___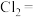 ____
____ ____
____
①配平上述氧化还原反应___________ 。
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为
的反应为 。
。
①该反应中的还原产物是___________ (写化学式),反应中每生成1个 分子,转移电子的数目为
分子,转移电子的数目为___________ 。
②用双线桥标出反应中电子转移的方向和数目___________ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ 。
A. B.
B. C.
C. D.
D.
(1)“维生素
 可以将食物中的
可以将食物中的 转化为
转化为 ”,说明维生素
”,说明维生素
(2)
 常用检查输送
常用检查输送 的管道是否,其反应如下:___
的管道是否,其反应如下:___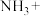 ___
___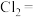 ____
____ ____
____
①配平上述氧化还原反应
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为
的反应为 。
。①该反应中的还原产物是
 分子,转移电子的数目为
分子,转移电子的数目为②用双线桥标出反应中电子转移的方向和数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知 是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究
是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究 的性质,进行了如下实验:
的性质,进行了如下实验:
Ⅰ.配制480mL
 溶液
溶液
(1)用托盘天平称量,需要称取
_________ g。
(2)定容时,若仰视容量瓶刻度线会使配制的 溶液浓度
溶液浓度_________ (填“偏大”、“偏小”或“不变”)。
(3)若在加蒸馏水时,不小心加过了刻度线,此时应该进行的操作是_________ 。
Ⅱ.探究 的性质
的性质
(4)取20mL上述 溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为
溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为_________ 。
(5)再取20mL上述 溶液,逐滴加入新制氯水直至过量,再加入
溶液,逐滴加入新制氯水直至过量,再加入 溶液振荡静置,现象为
溶液振荡静置,现象为_________ 。
(6)有上述实验现象可得到的结论:还原性:
_________  (填“>”“<”或者“=”)
(填“>”“<”或者“=”)
(7)若向10mL上述 溶液通入44.8mL
溶液通入44.8mL (标准状况),反应的离子方程式为
(标准状况),反应的离子方程式为_________ 。
 是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究
是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组为制备并探究 的性质,进行了如下实验:
的性质,进行了如下实验:Ⅰ.配制480mL

 溶液
溶液(1)用托盘天平称量,需要称取

(2)定容时,若仰视容量瓶刻度线会使配制的
 溶液浓度
溶液浓度(3)若在加蒸馏水时,不小心加过了刻度线,此时应该进行的操作是
Ⅱ.探究
 的性质
的性质(4)取20mL上述
 溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为
溶液,加入KSCN溶液,滴入少量新制氯水,溶液的颜色变为(5)再取20mL上述
 溶液,逐滴加入新制氯水直至过量,再加入
溶液,逐滴加入新制氯水直至过量,再加入 溶液振荡静置,现象为
溶液振荡静置,现象为(6)有上述实验现象可得到的结论:还原性:

 (填“>”“<”或者“=”)
(填“>”“<”或者“=”)(7)若向10mL上述
 溶液通入44.8mL
溶液通入44.8mL (标准状况),反应的离子方程式为
(标准状况),反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,请回答下列问题

下列问题:
(1)a点处的氧化产物是_________ (填化学式,下同),还原产物是_______ ,a点对应的离子方程式为_____ 。
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为____ mol,此时反应的离子方程式是_____________ 。
(3)当溶液中的I-为0.4mol时,加入的KIO3为______ mol。
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为____________ 。

下列问题:
(1)a点处的氧化产物是
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为
(3)当溶液中的I-为0.4mol时,加入的KIO3为
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480 mL含NaClO25%,密度为1.19 g/cm3的消毒液。下列说法正确的有______________________ 。
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小
D.需要称量的NaClO固体的质量为140 g
E.定容时俯视刻度线,会使配制溶液浓度偏低
F.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
(2)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是_________ 。(填序号)
(3)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性: NaClO______________________ H2O2(填“>”或“<”);当有0.1molO2生成时,转移电子的物质的量为_________ mol。
II.二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂
(4)KClO3和浓盐酸在一定温度下反应会生成 ClO2和Cl2,该反应的离子方程式________ 。
(5)将ClO2通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式____________ 。
(1)某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480 mL含NaClO25%,密度为1.19 g/cm3的消毒液。下列说法正确的有
A.配制过程只需要四种仪器即可完成
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小
D.需要称量的NaClO固体的质量为140 g
E.定容时俯视刻度线,会使配制溶液浓度偏低
F.上下颠倒摇匀后发现溶液凹液面低于刻度线,应再加水至刻度线
(2)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是
序号 | 实验 | 实验现象 |
1 | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去; b.有大量气泡产生 |
2 | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
II.二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂
(4)KClO3和浓盐酸在一定温度下反应会生成 ClO2和Cl2,该反应的离子方程式
(5)将ClO2通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被还原的元素是(填元素符号)__________ ,被氧化的元素是(填元素符号)_______ ,氧化剂是(填化学式,以下同)________ ,还原剂是_________ ,氧化产物是________ ,还原产物是_________ 。
(2)运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答。
过氧化钠几乎可与所有的常见气态非金属氧化物反应:
如:2Na2O2+2CO2=2Na2CO3+O2↑ Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式:________________ 。
②通过比较可知,当非金属元素处于_________ 价时,其氧化物与过氧化钠反应有O2生成。
(2)运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答。
过氧化钠几乎可与所有的常见气态非金属氧化物反应:
如:2Na2O2+2CO2=2Na2CO3+O2↑ Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式:
②通过比较可知,当非金属元素处于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫、氮两元素的价类二维图。请回答下列问题:
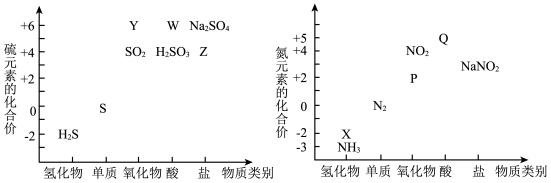
(1)物质Y是 的酸酐,其分子式为
的酸酐,其分子式为___________ 。
(2)大苏打 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
(3)W的浓溶液具有强氧化性、吸水性和脱水性,常用作干燥剂,则下列气体可用W干燥的是________。(填字母)
(4)在化工生产中,需要考虑控制反应条件。工业合成氨通常选择在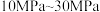 下进行,压强不能过低也不能过高的原因是:
下进行,压强不能过低也不能过高的原因是:___________ 。
(5)已知物质Z是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为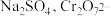 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式___________ 。
(6)将 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共 。待产生的气体全部释放后,向溶液加入
。待产生的气体全部释放后,向溶液加入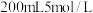 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则物质Q的物质的量浓度是
全部转化成沉淀,则物质Q的物质的量浓度是___________  。
。

(1)物质Y是
 的酸酐,其分子式为
的酸酐,其分子式为(2)大苏打
 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)A. | B. | C. | D. |
A. | B. | C. | D. |
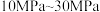 下进行,压强不能过低也不能过高的原因是:
下进行,压强不能过低也不能过高的原因是:(5)已知物质Z是一种可溶性正盐,能被酸性
 溶液氧化为
溶液氧化为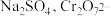 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式(6)将
 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共 。待产生的气体全部释放后,向溶液加入
。待产生的气体全部释放后,向溶液加入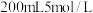 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则物质Q的物质的量浓度是
全部转化成沉淀,则物质Q的物质的量浓度是 。
。
您最近一年使用:0次
【推荐3】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是___________ (填字母,下同)。
A.Fe B.FeCl3
C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是____
A.NaNO2被氧化
B.药品美蓝是还原剂
C.NaNO2是还原剂
D.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:___________ 。
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中FeSO4是___________ (填“氧化剂”或“还原剂”)。
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3
C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.NaNO2被氧化
B.药品美蓝是还原剂
C.NaNO2是还原剂
D.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中FeSO4是
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子方程式:
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
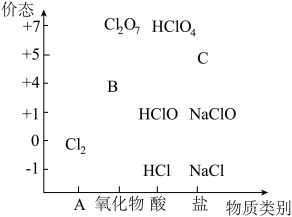
请回答下列问题:
(1)二维图中类别A是_______ ;B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是_______ (填化学式,下同);C的焰色试验呈黄色,则C是_______ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与_______ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_______ 性,可能与(填序号)_______ 发生反应。
(3)实验室常用 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的_______ (填“A”或“B”)作为发生装置,反应的离子方程式为_______ 。

(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。
①该反应说明氧化性:NaClO_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②用单线桥法表示该反应电子转移的方向和数目:________ 。
(5)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为_______ 。

请回答下列问题:
(1)二维图中类别A是
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)实验室常用
 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的
(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。①该反应说明氧化性:NaClO
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②用单线桥法表示该反应电子转移的方向和数目:
(5)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】第一次世界大战的第二次伊普尔战役中,德军在比利时伊普尔运河河畔针对英法联军开启了人类战争史上第一次大规模使用毒气的先例。1915年4 月22日傍晚,英法联军前线战壕的士兵突然看到一股黄绿色气体逐渐袭来,很快数百名英法联军士兵中毒而死,部分跑到山坡上的士兵幸免于难。后来在打扫战场时人们发现,死亡士兵军服的黄铜扣子变成了绿色。
(1)由上述事例可归纳出氯气的性质有___________ 。
(2)按照要求写出以下反应的化学用语:
①铁丝在氯气中燃烧的化学方程式:___________ 。
②工业制备漂白粉的化学方程式:___________ 。
③实验室制取氯气的离子方程式:___________ 。
(3)将新鲜的有色花瓣放入干燥的氯气中可观察到的现象是___________ ,原因是___________ 。
(4)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸___________ ,反应的化学方程式为___________ 。
(1)由上述事例可归纳出氯气的性质有
(2)按照要求写出以下反应的化学用语:
①铁丝在氯气中燃烧的化学方程式:
②工业制备漂白粉的化学方程式:
③实验室制取氯气的离子方程式:
(3)将新鲜的有色花瓣放入干燥的氯气中可观察到的现象是
(4)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室用MnO2氧化密度为1.19 g·cm-3,溶质质量分数为36.5%的HCl溶液,制备氯气。
(1)该反应的离子方程式为:__________________________________________________ ,该盐酸的物质的量浓度为_______________ mol/L。
(2)生成1molCl2时,转移的电子数目为_______________ 。
(3) 8.7gMnO2与足量浓盐酸反应能使_____________ molHCl被氧化:
(4)浓盐酸在反应中显示出来的性质是___________ .(填字母)
a.还原性b.酸性c.氧化性d.挥发性
(5)用氢氧化钠溶液吸收多余的氯气(用离子方程式表示):_____________________ 。
(1)该反应的离子方程式为:
(2)生成1molCl2时,转移的电子数目为
(3) 8.7gMnO2与足量浓盐酸反应能使
(4)浓盐酸在反应中显示出来的性质是
a.还原性b.酸性c.氧化性d.挥发性
(5)用氢氧化钠溶液吸收多余的氯气(用离子方程式表示):
您最近一年使用:0次



