工业烟气可用氯酸氧化法脱硫,涉及反应:_______ _______
_______ _______
_______ =_______
=_______ (未配平)。完成下列填空:
(未配平)。完成下列填空:
(1)写出N原子核外电子排布的轨道表示式_______ 。
(2)用含字母a、b的代数式配平上述化学方程式_______ ,标出电子转移的方向和数目_______ 。该化学方程式配平系数不唯一,请说明理由_______ 。
(3)氯酸是一元强酸,可由氯酸钡溶液和稀硫酸反应得到。写出该反应的化学方程式_______ 。
(4)工业烟气中的 也可用
也可用 和
和 的混合液脱除。
的混合液脱除。
① 脱除
脱除 的离子方程式为
的离子方程式为_______ ;
② 溶液呈碱性的原因是
溶液呈碱性的原因是_______ 。
 _______
_______ _______
_______ =_______
=_______ (未配平)。完成下列填空:
(未配平)。完成下列填空:(1)写出N原子核外电子排布的轨道表示式
(2)用含字母a、b的代数式配平上述化学方程式
(3)氯酸是一元强酸,可由氯酸钡溶液和稀硫酸反应得到。写出该反应的化学方程式
(4)工业烟气中的
 也可用
也可用 和
和 的混合液脱除。
的混合液脱除。①
 脱除
脱除 的离子方程式为
的离子方程式为②
 溶液呈碱性的原因是
溶液呈碱性的原因是
2021·上海普陀·二模 查看更多[1]
更新时间:2021-04-03 18:39:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ、船底防污漆是一种加有防污剂的特种漆。涂装于船底和海洋水下设施之上,通过漆膜中毒料的渗出、扩散或水解,达到防止藤壶、牡蜗等海生物附着的目的。
氧化亚铜( )是一种鲜红色粉末状固体,主要用于制造船底防污漆,用来杀死低级海生动物。几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
)是一种鲜红色粉末状固体,主要用于制造船底防污漆,用来杀死低级海生动物。几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
①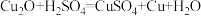
②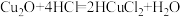
③
(1) 中铜元素的化合价为
中铜元素的化合价为___________ 。
(2)反应①中氧化剂为___________ ,还原剂为___________ 。
(3)反应②___________ (填“是”或“不是”)氧化还原反应;若是请说明转移电子情况,若不是请说明判断依据:___________ 。
(4)请写出反应③的离子方程式:___________ 。
Ⅱ、下面三个方法都可以用来制氯气:
①
②
③ (未配平)
(未配平)
根据以上三个反应,回答下列有关问题:
(5)用单线桥表示反应①电子转移情况___________ 。
(6)已知反应④: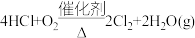 ,该反应也能制得氯气。提醒一下,反应条件越简单反应越容易发生,说明性质越强烈。则
,该反应也能制得氯气。提醒一下,反应条件越简单反应越容易发生,说明性质越强烈。则 、
、 、
、 三种物质氧化性由强到弱的顺序为
三种物质氧化性由强到弱的顺序为___________ 。
Ⅲ、有下列三个在溶液中发生的氧化还原反应:
①
②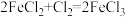
③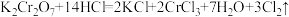
请根据上述反应分析推断后回答下列问题:
(7) 、
、 、
、 、
、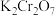 的氧化性由强到弱依次是
的氧化性由强到弱依次是___________ 。
(8) 、
、 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?___________ (填“能”或“不能”),理由是___________ 。
氧化亚铜(
 )是一种鲜红色粉末状固体,主要用于制造船底防污漆,用来杀死低级海生动物。几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:
)是一种鲜红色粉末状固体,主要用于制造船底防污漆,用来杀死低级海生动物。几乎不溶于水,可在酸性溶液中发生反应,与硫酸、盐酸、硝酸反应如下:①
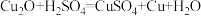
②
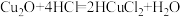
③

(1)
 中铜元素的化合价为
中铜元素的化合价为(2)反应①中氧化剂为
(3)反应②
(4)请写出反应③的离子方程式:
Ⅱ、下面三个方法都可以用来制氯气:
①

②

③
 (未配平)
(未配平)根据以上三个反应,回答下列有关问题:
(5)用单线桥表示反应①电子转移情况
(6)已知反应④:
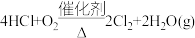 ,该反应也能制得氯气。提醒一下,反应条件越简单反应越容易发生,说明性质越强烈。则
,该反应也能制得氯气。提醒一下,反应条件越简单反应越容易发生,说明性质越强烈。则 、
、 、
、 三种物质氧化性由强到弱的顺序为
三种物质氧化性由强到弱的顺序为Ⅲ、有下列三个在溶液中发生的氧化还原反应:
①

②
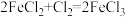
③
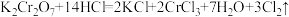
请根据上述反应分析推断后回答下列问题:
(7)
 、
、 、
、 、
、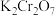 的氧化性由强到弱依次是
的氧化性由强到弱依次是(8)
 、
、 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.现有下列10种物质:①铝,②纯醋酸,③ ,④
,④ ,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧
,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧ ,⑨硝酸钾晶体,⑩乙醇。
,⑨硝酸钾晶体,⑩乙醇。
(1)上述物质中属于非电解质的有_______ (填序号);①②⑥⑦⑨⑩这六种物质中能导电的有_______ (填序号)。
(2)向⑥中加入⑤的离子方程式是_______ 。
(3)⑧在水中的电离方程式为_______ 。
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式_______ 。
(5)用双线桥表示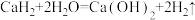 反应电子转移情况:
反应电子转移情况:_______ 。
Ⅱ.利用物质的量的相关知识进行填空:
(6)有一类物质的结构似“鸟巢”,如化学式为 的五硼烷(见下图)。含有
的五硼烷(见下图)。含有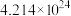 个原子的五硼烷的质量为
个原子的五硼烷的质量为_______ 。
(7)在同温同压下,NO和 两种气体,密度比为
两种气体,密度比为_______ ,若两者质量相等,其体积比为_______ 。
(8)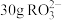 中,核外电子总数比质子总数多
中,核外电子总数比质子总数多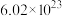 ,则R的摩尔质量为
,则R的摩尔质量为_______ 。
 ,④
,④ ,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧
,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧ ,⑨硝酸钾晶体,⑩乙醇。
,⑨硝酸钾晶体,⑩乙醇。(1)上述物质中属于非电解质的有
(2)向⑥中加入⑤的离子方程式是
(3)⑧在水中的电离方程式为
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应
 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式(5)用双线桥表示
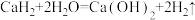 反应电子转移情况:
反应电子转移情况:Ⅱ.利用物质的量的相关知识进行填空:
(6)有一类物质的结构似“鸟巢”,如化学式为
 的五硼烷(见下图)。含有
的五硼烷(见下图)。含有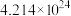 个原子的五硼烷的质量为
个原子的五硼烷的质量为
(7)在同温同压下,NO和
 两种气体,密度比为
两种气体,密度比为(8)
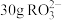 中,核外电子总数比质子总数多
中,核外电子总数比质子总数多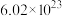 ,则R的摩尔质量为
,则R的摩尔质量为
您最近一年使用:0次
【推荐3】氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)工业干法制备高铁酸钾的第一步反应为: 。该反应中氧化产物为
。该反应中氧化产物为_______ 。
(2)已知下列三个氧化还原反应:①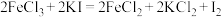 ;②
;② ;③
;③ 。若溶质中
。若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的_______ (从下列三个反应中选择)作氧化剂。
(3)无水情况下, 可以和
可以和 发生如下反应:_______
发生如下反应:_______ _______
_______ _______
_______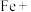 _______
_______ _______
_______ _______
_______ 。配平上述反应方程式,单线桥法标出电子转移的方向和数目
。配平上述反应方程式,单线桥法标出电子转移的方向和数目_______ ;
(4)向含有 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性 ;②KSCN溶液可用于检验
;②KSCN溶液可用于检验 的存在,溶液呈红色。则下列叙述中正确的是
的存在,溶液呈红色。则下列叙述中正确的是_______ 。
①氧化性: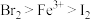
②原溶液中 一定被氧化
一定被氧化
③通入氯气后,原溶液中的 一定被氧化
一定被氧化
④不能确定通入氯气后的溶液中是否还存在
(5)下列转化中,需要加入还原剂才能实现的是_______。
(6)2020年8月初,某海外港口因硝酸铵分解引发剧烈爆炸,已知: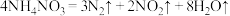 ,则该反应中被还原和被氧化的N原子数之比为
,则该反应中被还原和被氧化的N原子数之比为_______ 。
(7)用如图装置可验证 是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为_______ (填序号)。
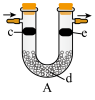
①干燥的有色布条 ②湿润的有色布条 ③浓硫酸 ④碱石灰 ⑤无水
(1)工业干法制备高铁酸钾的第一步反应为:
 。该反应中氧化产物为
。该反应中氧化产物为(2)已知下列三个氧化还原反应:①
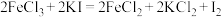 ;②
;② ;③
;③ 。若溶质中
。若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的(3)无水情况下,
 可以和
可以和 发生如下反应:_______
发生如下反应:_______ _______
_______ _______
_______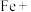 _______
_______ _______
_______ _______
_______ 。配平上述反应方程式,单线桥法标出电子转移的方向和数目
。配平上述反应方程式,单线桥法标出电子转移的方向和数目(4)向含有
 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性 ;②KSCN溶液可用于检验
;②KSCN溶液可用于检验 的存在,溶液呈红色。则下列叙述中正确的是
的存在,溶液呈红色。则下列叙述中正确的是①氧化性:
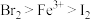
②原溶液中
 一定被氧化
一定被氧化③通入氯气后,原溶液中的
 一定被氧化
一定被氧化④不能确定通入氯气后的溶液中是否还存在

(5)下列转化中,需要加入还原剂才能实现的是_______。
A. | B. |
C. | D. |
(6)2020年8月初,某海外港口因硝酸铵分解引发剧烈爆炸,已知:
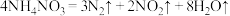 ,则该反应中被还原和被氧化的N原子数之比为
,则该反应中被还原和被氧化的N原子数之比为(7)用如图装置可验证
 是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
①干燥的有色布条 ②湿润的有色布条 ③浓硫酸 ④碱石灰 ⑤无水

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】NaNO2有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。
(1)下列说法正确的是___________(填序号)。
(2)已知NaNO2能发生如下反应:NaNO2+HI=NO+I2+NaI+H2O(未配平)
①从上述反应推知___________ (填序号)。
A.氧化性:I2>NaNO2 B.氧化性:NaNO2>I2
C.还原性:HI>NO D.还原性:I2>HI
②配平上述反应并标出电子转移的方向和数目:___________
NaNO2+HI=NO+I2+NaI+H2O
③写出上述反应的半反应:氧化反应:___________ ;还原反应:___________
(3)根据上述反应,可用试纸和生活中常见的物质进行实验来鉴别NaNO2和NaCl。现供选用的物质有:①白酒;②碘化钾淀粉试纸;③淀粉;④白糖;⑤食醋,进行本实验时,可以选用的物质至少有___________ (填序号)。
(4)某工厂的废液中含有2%~5%的NaNO2,直接排放会造成污染。下列试剂中:①NaCl;②NH4Cl;③HNO3;④浓H2SO4,能使NaNO2转化为N2的是___________ (填序号)。
(1)下列说法正确的是___________(填序号)。
| A.解毒剂美蓝应该具有氧化性 | B.中毒时亚硝酸盐发生氧化反应 |
| C.解毒时高铁血红蛋白被还原 | D.中毒过程中血红蛋白显氧化性 |
①从上述反应推知
A.氧化性:I2>NaNO2 B.氧化性:NaNO2>I2
C.还原性:HI>NO D.还原性:I2>HI
②配平上述反应并标出电子转移的方向和数目:
NaNO2+HI=NO+I2+NaI+H2O
③写出上述反应的半反应:氧化反应:
(3)根据上述反应,可用试纸和生活中常见的物质进行实验来鉴别NaNO2和NaCl。现供选用的物质有:①白酒;②碘化钾淀粉试纸;③淀粉;④白糖;⑤食醋,进行本实验时,可以选用的物质至少有
(4)某工厂的废液中含有2%~5%的NaNO2,直接排放会造成污染。下列试剂中:①NaCl;②NH4Cl;③HNO3;④浓H2SO4,能使NaNO2转化为N2的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图是某儿童微量元素体检报告单的部分数据,根据数据,回答下列问题:
(1)该儿童体内_________ 元素含量偏低。
(2)报告单中“μmol·L-1”是__________ (填“质量”“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的________ 性。
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是_______________________ 。
(5)取补血剂片用研钵研细,加入过量稀硫酸,取澄清液,然后滴加KSCN溶液,若溶液变为红色,则溶液中含有________ (填离子符号),说明补血剂是否变质____________ 。
北京市医疗机构临床检验结果报告单 | ||||
| 分析项目 | 检测结果 | 单位 | 参考范围 | |
| 1 | 锌(Zn) | 115.92 | 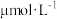 | 66~120 |
| 2 | 铁(Fe) | 6.95↓ | 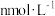 | 7.52~11.82 |
| 3 | 钙(Ca) | 1.68 | 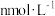 | 1.55~2.10 |
(1)该儿童体内
(2)报告单中“μmol·L-1”是
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是
(5)取补血剂片用研钵研细,加入过量稀硫酸,取澄清液,然后滴加KSCN溶液,若溶液变为红色,则溶液中含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请把符合要求的化学方程式的序号填在下列横线处:
①既属于分解反应又是氧化还原反应的是__________ 。
②属于化合反应,但不是氧化还原反应的是__________ 。
③既属于化合反应又是氧化还原反应的是__________ 。
④属于分解反应,但不是氧化还原反应的是__________ 。
⑤不属于四种基本反应类型,但属于氧化还原反应的是__________ 。
A.2NaHCO3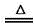 Na2CO3 +H2O+CO2↑ B.2Na + Cl2
Na2CO3 +H2O+CO2↑ B.2Na + Cl2 2NaCl
2NaCl
C.Zn + CuSO4 ZnSO4 + Cu D.2KMnO4
ZnSO4 + Cu D.2KMnO4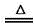 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
E.CaO + CO2 CaCO3 F.4FeS2 +11O2
CaCO3 F.4FeS2 +11O2 2Fe2O3 +8SO2
2Fe2O3 +8SO2
①既属于分解反应又是氧化还原反应的是
②属于化合反应,但不是氧化还原反应的是
③既属于化合反应又是氧化还原反应的是
④属于分解反应,但不是氧化还原反应的是
⑤不属于四种基本反应类型,但属于氧化还原反应的是
A.2NaHCO3
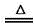 Na2CO3 +H2O+CO2↑ B.2Na + Cl2
Na2CO3 +H2O+CO2↑ B.2Na + Cl2 2NaCl
2NaClC.Zn + CuSO4
 ZnSO4 + Cu D.2KMnO4
ZnSO4 + Cu D.2KMnO4 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑E.CaO + CO2
 CaCO3 F.4FeS2 +11O2
CaCO3 F.4FeS2 +11O2 2Fe2O3 +8SO2
2Fe2O3 +8SO2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学还原稳定法是当前 水体污染修复领域的主要技术。废水中
水体污染修复领域的主要技术。废水中 主要以
主要以 和
和 形式存在,化学还原稳定法去除水中
形式存在,化学还原稳定法去除水中 主要包括铬的还原和固定两个过程。常用的化学还原剂包括硫系还原剂和铁系还原剂。已知:
主要包括铬的还原和固定两个过程。常用的化学还原剂包括硫系还原剂和铁系还原剂。已知: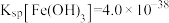 ,
,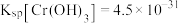 。
。
(1)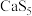 是常用的硫系还原剂,在处理
是常用的硫系还原剂,在处理 时自身转化为单质S。
时自身转化为单质S。
① 具有链状结构,其结构式可表示为
具有链状结构,其结构式可表示为_______ 。
②经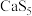 修复的水体pH明显
修复的水体pH明显_______ (填“增大”或“减小”),严重影响土壤及地下水的利用。
(2)铁系还原剂 的还原效率虽不及硫化物,但有利于Cr的固定。
的还原效率虽不及硫化物,但有利于Cr的固定。
①在酸性溶液中, 还原
还原 的离子方程式为
的离子方程式为_______ 。
②Cr的固定途径有两个:其一是难溶性铬铁共沉淀氢氧化物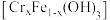 或
或 沉淀的生成;其二是
沉淀的生成;其二是_______ 。
(3)试剂联用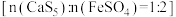 有望实现高效且稳定的修复效果。
有望实现高效且稳定的修复效果。
①待各体系充分反应后,静置2h。实验测得分别使用单一试剂和试剂联用时,溶液中总Cr的去除率随溶液初始pH的变化关系如图1所示。pH>9,随pH增大,试剂联用时溶液中总Cr的去除率上升的原因是_______ 。

②在 存在下,试剂联用处理溶液中
存在下,试剂联用处理溶液中 ,待体系充分反应,静置2h。测得
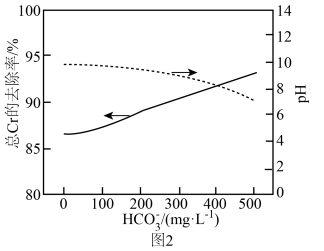
,待体系充分反应,静置2h。测得 浓度对溶液pH以及总Cr去除效果的影响关系如图2所示。随
浓度对溶液pH以及总Cr去除效果的影响关系如图2所示。随 浓度进一步增加,总Cr的去除率明显上升的原因是
浓度进一步增加,总Cr的去除率明显上升的原因是_______ 。
③研究表明,试剂联用效果优于单一试剂主要是由于反应过程中生成了起催化作用的FeS。FeS的生成过程可用化学方程式表示为_______ 。
 水体污染修复领域的主要技术。废水中
水体污染修复领域的主要技术。废水中 主要以
主要以 和
和 形式存在,化学还原稳定法去除水中
形式存在,化学还原稳定法去除水中 主要包括铬的还原和固定两个过程。常用的化学还原剂包括硫系还原剂和铁系还原剂。已知:
主要包括铬的还原和固定两个过程。常用的化学还原剂包括硫系还原剂和铁系还原剂。已知: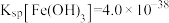 ,
,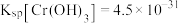 。
。(1)
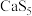 是常用的硫系还原剂,在处理
是常用的硫系还原剂,在处理 时自身转化为单质S。
时自身转化为单质S。①
 具有链状结构,其结构式可表示为
具有链状结构,其结构式可表示为②经
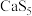 修复的水体pH明显
修复的水体pH明显(2)铁系还原剂
 的还原效率虽不及硫化物,但有利于Cr的固定。
的还原效率虽不及硫化物,但有利于Cr的固定。①在酸性溶液中,
 还原
还原 的离子方程式为
的离子方程式为②Cr的固定途径有两个:其一是难溶性铬铁共沉淀氢氧化物
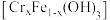 或
或 沉淀的生成;其二是
沉淀的生成;其二是(3)试剂联用
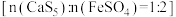 有望实现高效且稳定的修复效果。
有望实现高效且稳定的修复效果。①待各体系充分反应后,静置2h。实验测得分别使用单一试剂和试剂联用时,溶液中总Cr的去除率随溶液初始pH的变化关系如图1所示。pH>9,随pH增大,试剂联用时溶液中总Cr的去除率上升的原因是

②在
 存在下,试剂联用处理溶液中
存在下,试剂联用处理溶液中 ,待体系充分反应,静置2h。测得
,待体系充分反应,静置2h。测得 浓度对溶液pH以及总Cr去除效果的影响关系如图2所示。随
浓度对溶液pH以及总Cr去除效果的影响关系如图2所示。随 浓度进一步增加,总Cr的去除率明显上升的原因是
浓度进一步增加,总Cr的去除率明显上升的原因是
③研究表明,试剂联用效果优于单一试剂主要是由于反应过程中生成了起催化作用的FeS。FeS的生成过程可用化学方程式表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据物质在生产、生活等方面的应用填空。
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈__________ (填字母代号)。
a.浅蓝色 b.浅红色 c.浅绿色
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用__________ 溶液(填字母代号)。
a.NaOH b.H2O2 c.KSCN
(3)电解氧化铝时加入冰晶石的作用为________________ 。
(4)完成乙醇发生催化氧化的化学方程式:2CH3CH2OH+O2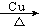
_________________________ 。
(5)常见的酸性锌锰电池的负极材料为Zn,请写出负极的电极反应式:___________________ 。
(6)铝热反应是工业上常用的反应之一,请写出Al与Fe3O4发生铝热反应的化学方程式:___________ 。
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈
a.浅蓝色 b.浅红色 c.浅绿色
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用
a.NaOH b.H2O2 c.KSCN
(3)电解氧化铝时加入冰晶石的作用为
(4)完成乙醇发生催化氧化的化学方程式:2CH3CH2OH+O2
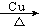
(5)常见的酸性锌锰电池的负极材料为Zn,请写出负极的电极反应式:
(6)铝热反应是工业上常用的反应之一,请写出Al与Fe3O4发生铝热反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)书写对应的化学用语:
①氯化铁溶液可作净水剂,用离子方程式解释其原理为______ 。
②氯碱工业对应的离子方程式为______ 。
(2)常温下,有下列4种溶液
a.pH=11的氨水 b.pH=11的氢氧化钠溶液 c.pH=3的醋酸 d.pH=3的盐酸
①在a和b中分别加入适量的氯化铵晶体后,两种溶液的pH均______ (填“增大”“减小”或“不变”)。
②将溶液a和d按比例混合后溶液恰好为中性,所得溶液中离子浓度从大到小排列的顺序为______ 。
(3)聚丙烯酸钠、涤纶的结构简式如图:

①合成聚丙烯酸钠的单体的结构简式是______ 。
②合成涤纶的单体有两种,其中能和 反应的单体的结构简式是
反应的单体的结构简式是______ 。
(1)书写对应的化学用语:
①氯化铁溶液可作净水剂,用离子方程式解释其原理为
②氯碱工业对应的离子方程式为
(2)常温下,有下列4种溶液
a.pH=11的氨水 b.pH=11的氢氧化钠溶液 c.pH=3的醋酸 d.pH=3的盐酸
①在a和b中分别加入适量的氯化铵晶体后,两种溶液的pH均
②将溶液a和d按比例混合后溶液恰好为中性,所得溶液中离子浓度从大到小排列的顺序为
(3)聚丙烯酸钠、涤纶的结构简式如图:

①合成聚丙烯酸钠的单体的结构简式是
②合成涤纶的单体有两种,其中能和
 反应的单体的结构简式是
反应的单体的结构简式是
您最近一年使用:0次
【推荐1】在水溶液中:YO3n-+3S2-+6H+=Y-+3S +3H2O
(1)YO3n-中Y元素的化合价是:_______
(2)Y元素原子的最外层电子数是:_____
(3)比较S2-和Y-的还原性:____
(1)YO3n-中Y元素的化合价是:
(2)Y元素原子的最外层电子数是:
(3)比较S2-和Y-的还原性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次



