键角NH3___________ PH3,原因是______________________ 。
2023高三·全国·专题练习 查看更多[1]
(已下线)07 常考题空7 结构决定性质——解释原因类简答题 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-04-25 16:31:43
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】硒化物(如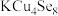 )可用于太阳能电池、光传感器,热电发电与制冷等。回答下列问题:
)可用于太阳能电池、光传感器,热电发电与制冷等。回答下列问题:
(1)基态Se原子核外电子排布式为[Ar]___________ 。
(2)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为___________
(3)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物 、
、 及
及 分子的键角从大到小顺序为
分子的键角从大到小顺序为___________ 。
(4)TMTSF( )中共价键的类型是
)中共价键的类型是___________ ,每个分子中含___________ 个 键。
键。
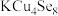 )可用于太阳能电池、光传感器,热电发电与制冷等。回答下列问题:
)可用于太阳能电池、光传感器,热电发电与制冷等。回答下列问题:(1)基态Se原子核外电子排布式为[Ar]
(2)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为
(3)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物
 、
、 及
及 分子的键角从大到小顺序为
分子的键角从大到小顺序为(4)TMTSF(
 )中共价键的类型是
)中共价键的类型是 键。
键。
您最近一年使用:0次
【推荐2】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________ 。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________ 。人一旦吸入b气体后,就易引起中毒,是因为__________ 而中毒。
(3)c是双核单质,写出其电子式____________ 。c分子中所含共价键的类型为_______ (填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________ 。
(4)d是四核化合物,其结构式为______________ ;d分子内所含共价键有________ 个σ键,________ 个π键;σ键与π键的强度大小关系为σ___ π(填“>”、“<”或“=”),原因是:__________ 。
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为
(2)b是双核化合物,常温下为无色无味气体。b的化学式为
(3)c是双核单质,写出其电子式
(4)d是四核化合物,其结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)在H-S、H-Cl两种共价键中,键的极性较强的是_______ ,键长较长的是_______ 。在四种酸①HClO4;②H2SO4;③HNO2;④HClO中,酸性由弱到强的顺序为_______ 。(用序号表示)
(2)下列气态分子①BeCl2;②BCl3;③CCl4;④H2O中,其键角由大到小的顺序为_______ 。(用序号表示)
(3)SO2与CO2在相同条件下两者在水中的溶解度较大的是____ (写分子式),理由是_____ 。
(1)在H-S、H-Cl两种共价键中,键的极性较强的是
(2)下列气态分子①BeCl2;②BCl3;③CCl4;④H2O中,其键角由大到小的顺序为
(3)SO2与CO2在相同条件下两者在水中的溶解度较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】表为周期表的一部分,其中的编号代表对应的元素。
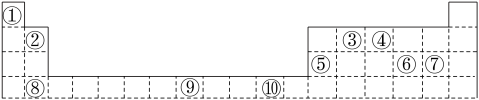
请回答下列问题:
(1)表中属于d区的元素是________ (填编号)。
(2)写出元素⑧的基态原子的电子排布式__________________________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为________ 对。
(4)元素④的氢化物的分子构型为________ ,中心原子的杂化形式为________ 。
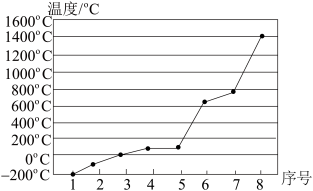
(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________ (填元素符号);其中电负性最大的是________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑧的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为

(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)N、H两元素按原子数目比l∶3和2∶4构成分子A和B,A的中心原子的杂化方式是________ ,A的电子式为____________ ,B的结构式为____________ 。
(2)NO3-的空间构型为________ ;写出NO3-互为等电子体的一种分子的化学式______ 。
(3)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为______ ,每个Ba2+与_____ 个O2-配位。
(2)NO3-的空间构型为
(3)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)两种有机物的相关数据如表:
HCON(CH3)2的相对分子质量比HCONH2的大,但其沸点反而比HCONH2的低,主要原因是_______ 。
(2)四种晶体的熔点数据如表:
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是_______ 。
(3)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
(4)气态三氧化硫以单分子形式存在,其分子的空间结构为_______ 形,其中共价键的类型有_______ 种;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。

(1)两种有机物的相关数据如表:
| 物质 | HCON(CH3)2 | HCONH2 |
| 相对分子质量 | 73 | 45 |
| 沸点/℃ | 153 | 220 |
HCON(CH3)2的相对分子质量比HCONH2的大,但其沸点反而比HCONH2的低,主要原因是
(2)四种晶体的熔点数据如表:
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 熔点/℃ | -183 | -90 | -127 | >1000 |
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是
(3)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(4)气态三氧化硫以单分子形式存在,其分子的空间结构为

您最近一年使用:0次



