根据所学知识填空:
(1)在下列物质中,属于晶体的是____ ,属于非晶体的是____ ;
A.玻璃 B.雪花 C.橡胶 D.铁块 E.单晶硅 F.沥青
(2)晶体中的微粒与晶胞的关系为:
①凡处于立方体顶点的微粒,同时为____ 个晶胞共有;
②凡处于立方体棱上的微粒,同时为____ 个晶胞共有;
③凡处于立方体面上的微粒,同时为____ 个晶胞共有;
④凡处于立方体体心的微粒,同时为____ 个晶胞共有。
(1)在下列物质中,属于晶体的是
A.玻璃 B.雪花 C.橡胶 D.铁块 E.单晶硅 F.沥青
(2)晶体中的微粒与晶胞的关系为:
①凡处于立方体顶点的微粒,同时为
②凡处于立方体棱上的微粒,同时为
③凡处于立方体面上的微粒,同时为
④凡处于立方体体心的微粒,同时为
2019高二下·全国·专题练习 查看更多[1]
(已下线)2019年4月24日 《每日一题》选修3-晶胞的概念
更新时间:2019-04-26 18:10:33
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】在离子晶体中,阴阳离子按一定规律在空间排列,如图(1)所示即是NaCl的晶体结构,这两种离子在空间三个互相垂直的方向上都是等距离排列的。
(1)在晶体中,每个Na+离子周围与它最接近的、且距离相等的Cl-共有_________ 个;
每个Na+离子周围与它最接近的、且距离相等的Na+共有__________ 个。而Na+离子数目与Cl-离子数目之比为______________ 。
在离子晶体中,阴阳离子具有球对称的电子云。它们可以被看成是不等径的刚性圆球,并彼此相切(如图⑵所示)。离子键的键长是相邻阴阳离子的半径之和(如图⑶所示),已知a为常数。

试回答下列问题:
(2)NaCl晶体中离子键的键长为______________________ 。Na+离子半径与Cl-离子半径比r+/r- =____________ 。(已知 √2=1.414 , √3=1.732, √5=2.236)
(3)NaCl晶体中不存在分子,但在温度达到1413℃时,NaCl晶体形成气体,并以分子形式存在,现有29.25gNaCl晶体,强热使温度达到1450℃,测得气体体积为5.6L(已折算为标准状况),则此时氯化钠气体的分子式为_______________________ 。
(4)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分数为__________________ 。
(1)在晶体中,每个Na+离子周围与它最接近的、且距离相等的Cl-共有
每个Na+离子周围与它最接近的、且距离相等的Na+共有
在离子晶体中,阴阳离子具有球对称的电子云。它们可以被看成是不等径的刚性圆球,并彼此相切(如图⑵所示)。离子键的键长是相邻阴阳离子的半径之和(如图⑶所示),已知a为常数。

试回答下列问题:
(2)NaCl晶体中离子键的键长为
(3)NaCl晶体中不存在分子,但在温度达到1413℃时,NaCl晶体形成气体,并以分子形式存在,现有29.25gNaCl晶体,强热使温度达到1450℃,测得气体体积为5.6L(已折算为标准状况),则此时氯化钠气体的分子式为
(4)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
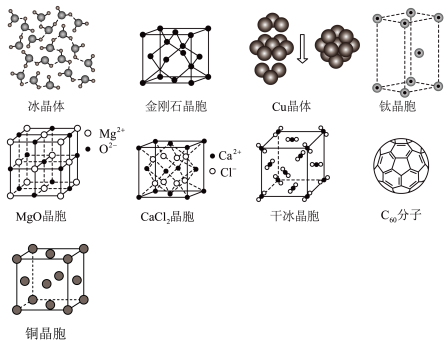
【推荐2】各图为几种分子、晶体或晶胞的结构示意图。
请回答下列问题:
(1)这些物质对应的晶体中,构成晶体的粒子之间主要以范德华力结合形成的晶体是_____ 、C60晶体;构成晶体的粒子之间主要以氢键结合形成的晶体是_____ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_____ 。
(3)每个Cu晶胞中实际占有_____ 个Cu原子,每个MgO晶胞中实际占有_____ 个镁离子,CaCl2晶体中每个Ca2+周围距离最近且相等的Cl-有_____ 个。
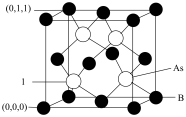
(4)超高热导率半导体材料-砷化硼(BAs)的晶胞结构如图所示,已知阿伏加德罗常数的值为NA,若晶胞的棱长为acm,则晶胞的密度为______ g•cm-3(列出含a、NA的计算式即可)。

请回答下列问题:
(1)这些物质对应的晶体中,构成晶体的粒子之间主要以范德华力结合形成的晶体是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(3)每个Cu晶胞中实际占有
(4)超高热导率半导体材料-砷化硼(BAs)的晶胞结构如图所示,已知阿伏加德罗常数的值为NA,若晶胞的棱长为acm,则晶胞的密度为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。某氮化铁的晶胞结构如图所示:
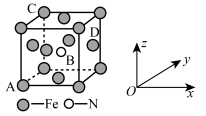
(1)在晶胞中,原子分数坐标A为(0,0,0);B为( ) , ,
, );C为(0,1,1),则D为
);C为(0,1,1),则D为____________ 。
(2)若该晶体的密度是ρ g·cm-3,则晶胞中两个最近的Fe的核间距为__________ (用含NA、ρ的代数式表示,不必化简)。
(3)在该晶胞结构中,Cu可以完全替代a位置Fe或者b位置Fe(见图1),形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的是______ (填“Cu替代a位置Fe型”或“Cu替代b位置Fe型”),替代后不稳定物质的化学式为______ 。


(1)在晶胞中,原子分数坐标A为(0,0,0);B为
 ,
, );C为(0,1,1),则D为
);C为(0,1,1),则D为(2)若该晶体的密度是ρ g·cm-3,则晶胞中两个最近的Fe的核间距为
(3)在该晶胞结构中,Cu可以完全替代a位置Fe或者b位置Fe(见图1),形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国考古人员在秦陵挖掘的宝剑,到现们还是锋利无比,原因是剑锋上面覆盖了一层铬。
(1)写出Cr的外围电子排布式_______ 。与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是__________ 。
(2)根据下表Cr原子的能级电离能(I:k]/mol)数据,解释原子逐级电离能增大的原因:_______ 。
(2)CrCl3·6H2O有三种水合异构体,蓝绿色的[Cr(H2O)5C1]Cl2·6H2O,绿色的[Cr(H2O)4C12]Cl·6H2O和紫色的______ ,其中Cr的配体水分子也可以被NH3置换,如[Cr(NH3)5Cl]2+,则NH3的VSEPR模型为_____ ,N的杂化方式为________ ,写出NH3的一种等电子体___________ 。
(4)CrO3能将CH3CH2OH氧化为乙醛,二者的相对分子质量相近,但乙醇的沸点比乙醛高,原因是___________ 。
(5)Cr晶体的堆积模型是体心立方堆积。
①下列金属晶体也采取这种堆积模型的是__________
A.Na B.Po C.Mg D.Cu
②晶胞中Cr的配位数为_________
③已知Cr的相对原子质量为M,Cr的密度为ρg/cm3,阿伏伽德罗常数用NA表示,则Cr的原子半径是__ pm.(写出表达式即可)
(1)写出Cr的外围电子排布式
(2)根据下表Cr原子的能级电离能(I:k]/mol)数据,解释原子逐级电离能增大的原因:
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 652.9 | 1590.6 | 2987 | 4743 | 6702 | 8744.9 | 15455 |
(4)CrO3能将CH3CH2OH氧化为乙醛,二者的相对分子质量相近,但乙醇的沸点比乙醛高,原因是
(5)Cr晶体的堆积模型是体心立方堆积。
①下列金属晶体也采取这种堆积模型的是
A.Na B.Po C.Mg D.Cu
②晶胞中Cr的配位数为
③已知Cr的相对原子质量为M,Cr的密度为ρg/cm3,阿伏伽德罗常数用NA表示,则Cr的原子半径是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
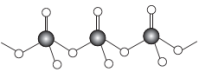
【推荐2】直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为___ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是___________ 。C60和金刚石都是碳的同素异形体,二者中熔点较高的是____________ 。
(2)化合物A (H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
3CH4+2(HB=NH)3+ 6H2O→3CO2+6H3BNH3制得。下列有关的叙述不正确的是_______ 。(填标号)
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道的电子排布有关。一般地,若为d 0或d10排布时无颜色;若为d1~d9排布时有颜色;如[Cu(H2O)4]2+显蓝色。据此判断25号元素Mn形成的络合离子[Mn(H2O)6]2+________ (填“有”或“无”)颜色 。
(4)H-C≡C-COOH分子内含有的σ键、π键的个数依次为_________ ,其中碳原子的杂化方式为_____ 。
(5)CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(6)某元素的原子的M能层为全充满状态,且N层电子只有一种运动状态,其单质晶体中微粒的堆积方式是下图中________ (选填“甲”、“乙”或“丙”); 若该晶体中晶胞的边长为acm,则该晶体的密度为_____ g /cm3(写出含a的表达式,用NA表示阿伏伽德罗常数)。

(1)O、Si、N元素的电负性由大到小的顺序是
(2)化合物A (H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
3CH4+2(HB=NH)3+ 6H2O→3CO2+6H3BNH3制得。下列有关的叙述不正确的是
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道的电子排布有关。一般地,若为d 0或d10排布时无颜色;若为d1~d9排布时有颜色;如[Cu(H2O)4]2+显蓝色。据此判断25号元素Mn形成的络合离子[Mn(H2O)6]2+
(4)H-C≡C-COOH分子内含有的σ键、π键的个数依次为
(5)CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是
(6)某元素的原子的M能层为全充满状态,且N层电子只有一种运动状态,其单质晶体中微粒的堆积方式是下图中

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列有关晶体的叙述不正确的有___________ (填序号)。
①固体物质一定是晶体
②铁、冰、玻璃是晶体
③缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体晶体体现了晶体的自范性
④晶体的熔点一定比非晶体的熔点高
⑤晶体和非晶体的本质区别是晶体中粒子在微观空间里呈现周期性的有序排列
⑥区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验
①固体物质一定是晶体
②铁、冰、玻璃是晶体
③缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体晶体体现了晶体的自范性
④晶体的熔点一定比非晶体的熔点高
⑤晶体和非晶体的本质区别是晶体中粒子在微观空间里呈现周期性的有序排列
⑥区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验
您最近一年使用:0次



