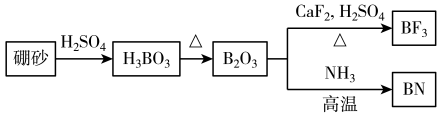
氮化硼(BN)是-种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1) 在BF3分子中,F-B-F的键角是_____ ,B原子的杂化轨道类型为_____ ,BF3和过量NaF作用可生成NaBF4, 的立体结构为
的立体结构为______ 。
(2)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为_____ (填“极性键”或“非极性键”),层间作用力为_____ 。

请回答下列问题:
(1) 在BF3分子中,F-B-F的键角是
 的立体结构为
的立体结构为(2)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
19-20高二下·内蒙古赤峰·期末 查看更多[2]
更新时间:2020-08-30 20:52:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)若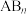 型分子的中心原子上有一对孤电子对未能成键,当
型分子的中心原子上有一对孤电子对未能成键,当 时,其分子的空间结构为
时,其分子的空间结构为______ ,中心原子的杂化方式为______ ;当 时,其分子的空间结构为
时,其分子的空间结构为______ 形,中心原子的杂化方式为______ 。
(2) 、
、 、
、 、
、 中,
中, 都是以
都是以 杂化轨道与O成键,则
杂化轨道与O成键,则 呈
呈______ 形, _呈
_呈_____ 形, 呈
呈______ 形, 呈
呈______ 形。
(3)“笑气”( )是人类最早应用于医疗的麻醉剂之一。
)是人类最早应用于医疗的麻醉剂之一。
有关理论认为 与
与 分子具有相似的结构(包括电子式);又已知
分子具有相似的结构(包括电子式);又已知 分子中氧原子只与一个氮原子相连,则
分子中氧原子只与一个氮原子相连,则 的电子式可表示为
的电子式可表示为______ ,由此可知它______ (填“含有”或“不含”)非极性键。
(4) 分子的空间结构是平面正方形。它有两种空间异构体——俗称顺铂和反铂,其结构简式为
分子的空间结构是平面正方形。它有两种空间异构体——俗称顺铂和反铂,其结构简式为
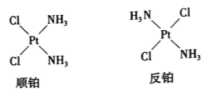
①试对顺铂和反铂的水溶性作出预测______ 。
② 分子是否具有手性
分子是否具有手性______ ?
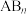 型分子的中心原子上有一对孤电子对未能成键,当
型分子的中心原子上有一对孤电子对未能成键,当 时,其分子的空间结构为
时,其分子的空间结构为 时,其分子的空间结构为
时,其分子的空间结构为(2)
 、
、 、
、 、
、 中,
中, 都是以
都是以 杂化轨道与O成键,则
杂化轨道与O成键,则 呈
呈 _呈
_呈 呈
呈 呈
呈(3)“笑气”(
 )是人类最早应用于医疗的麻醉剂之一。
)是人类最早应用于医疗的麻醉剂之一。有关理论认为
 与
与 分子具有相似的结构(包括电子式);又已知
分子具有相似的结构(包括电子式);又已知 分子中氧原子只与一个氮原子相连,则
分子中氧原子只与一个氮原子相连,则 的电子式可表示为
的电子式可表示为(4)
 分子的空间结构是平面正方形。它有两种空间异构体——俗称顺铂和反铂,其结构简式为
分子的空间结构是平面正方形。它有两种空间异构体——俗称顺铂和反铂,其结构简式为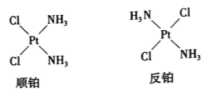
①试对顺铂和反铂的水溶性作出预测
②
 分子是否具有手性
分子是否具有手性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二氧化氯(ClO2)是一种常用的饮用水消毒剂。
(1)ClO2分子中的键角约为120°。ClO2易溶于水的原因是___ 。ClO2得到一个电子后形成 ,
, 的空间构型是
的空间构型是___ 。
(2)某ClO2泡腾片的有效成分为NaClO2、NaHSO4、NaHCO3,其溶于水时反应可得到ClO2溶液,并逸出大量气体。NaClO2和NaHSO4反应生成ClO2和Cl-的离子方程式为___ ,逸出气体的主要成分是___ (填化学式)。
(3)ClO2消毒时会产生少量的ClO ,可利用FeSO4将ClO
,可利用FeSO4将ClO 转化为Cl-除去。控制其他条件相同,
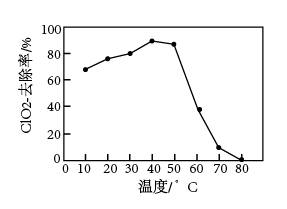
转化为Cl-除去。控制其他条件相同, 去除率随温度变化如图所示。温度高于50℃时,
去除率随温度变化如图所示。温度高于50℃时, 去除率降低的可能原因是
去除率降低的可能原因是___ 。
(4)测定某水样中 浓度的方法如下:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
浓度的方法如下:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:ClO +I-+H+—H2O+I2+Cl-(未配平)
+I-+H+—H2O+I2+Cl-(未配平)
I2+S2O —I-+S4O
—I-+S4O (未配平)
(未配平)
计算水样中ClO 的浓度(写出计算过程)
的浓度(写出计算过程)___ 。
(1)ClO2分子中的键角约为120°。ClO2易溶于水的原因是
 ,
, 的空间构型是
的空间构型是(2)某ClO2泡腾片的有效成分为NaClO2、NaHSO4、NaHCO3,其溶于水时反应可得到ClO2溶液,并逸出大量气体。NaClO2和NaHSO4反应生成ClO2和Cl-的离子方程式为
(3)ClO2消毒时会产生少量的ClO
 ,可利用FeSO4将ClO
,可利用FeSO4将ClO 转化为Cl-除去。控制其他条件相同,
转化为Cl-除去。控制其他条件相同, 去除率随温度变化如图所示。温度高于50℃时,
去除率随温度变化如图所示。温度高于50℃时, 去除率降低的可能原因是
去除率降低的可能原因是
(4)测定某水样中
 浓度的方法如下:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
浓度的方法如下:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。已知:ClO
 +I-+H+—H2O+I2+Cl-(未配平)
+I-+H+—H2O+I2+Cl-(未配平)I2+S2O
 —I-+S4O
—I-+S4O (未配平)
(未配平)计算水样中ClO
 的浓度(写出计算过程)
的浓度(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)基态 原子中,核外电子排布式为
原子中,核外电子排布式为________ ,核外电子占据的最高能层电子的电子云轮廓图形状为_______ ,它在周期表中的位置为_______ ,与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有____ 种。
(2) 与
与 形成
形成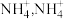 中
中 键角比
键角比 中
中 键角大,原因是
键角大,原因是______ , 中
中 键角
键角__  中
中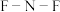 键角(填写“大于”“小于”或“等于”)。
键角(填写“大于”“小于”或“等于”)。
(3)比较①乙酸②甲酸③二氯乙酸的酸性由强到弱的顺序为_______ (填序号);比较① ②
② ③
③ 的熔点由低到高的顺序为
的熔点由低到高的顺序为________ (填序号);比较①晶体硅 ②晶体锗 ③ ④
④ 的熔点由低到高的顺序为
的熔点由低到高的顺序为_______ (填序号)。
(4)在周期表中,与 化学性质最相似的邻族元素是
化学性质最相似的邻族元素是______ ,该元素的最高正价氧化物对应的水化物与氢氧化钠反应的离子方程式为______ 。
(5) 等是有机反应中重要的中间体。碳正离子
等是有机反应中重要的中间体。碳正离子 可以通过
可以通过 在“超强酸”中获得1个
在“超强酸”中获得1个 而得到,而
而得到,而 失去
失去 可得
可得 。
。
① 是反应性很强的正离子,是缺电子的,其电子式是
是反应性很强的正离子,是缺电子的,其电子式是______ 。
② 中4个原子是共平面的,3个键角相等,键角应是
中4个原子是共平面的,3个键角相等,键角应是_______ 。
(1)基态
 原子中,核外电子排布式为
原子中,核外电子排布式为(2)
 与
与 形成
形成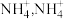 中
中 键角比
键角比 中
中 键角大,原因是
键角大,原因是 中
中 键角
键角 中
中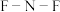 键角(填写“大于”“小于”或“等于”)。
键角(填写“大于”“小于”或“等于”)。(3)比较①乙酸②甲酸③二氯乙酸的酸性由强到弱的顺序为
 ②
② ③
③ 的熔点由低到高的顺序为
的熔点由低到高的顺序为 ④
④ 的熔点由低到高的顺序为
的熔点由低到高的顺序为(4)在周期表中,与
 化学性质最相似的邻族元素是
化学性质最相似的邻族元素是(5)
 等是有机反应中重要的中间体。碳正离子
等是有机反应中重要的中间体。碳正离子 可以通过
可以通过 在“超强酸”中获得1个
在“超强酸”中获得1个 而得到,而
而得到,而 失去
失去 可得
可得 。
。①
 是反应性很强的正离子,是缺电子的,其电子式是
是反应性很强的正离子,是缺电子的,其电子式是②
 中4个原子是共平面的,3个键角相等,键角应是
中4个原子是共平面的,3个键角相等,键角应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国硒含量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸(H2SeO3)进而制备单质硒。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为___________ 。
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应___________ 。
(3)基态Se原子电子占据最高能级的电子云轮廓图为___________ 形。 号的空间结构为
号的空间结构为___________ 形。
(4)关于硒单质及其化合物说法正确的是___________ (填标号)。
a.硒单质在常温下呈固态 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.键角: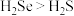 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下, 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:

 的
的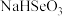 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为___________ ,计算反应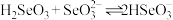 的平衡常数K=
的平衡常数K=___________ 。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应
(3)基态Se原子电子占据最高能级的电子云轮廓图为
 号的空间结构为
号的空间结构为(4)关于硒单质及其化合物说法正确的是
a.硒单质在常温下呈固态 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.键角:
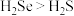 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下,
 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:
 的
的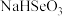 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为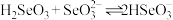 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1) 中,
中, 的轨道杂化方式为
的轨道杂化方式为___________ ;列举与 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:___________ 、___________ (填化学式)。
(2)用价电子对互斥理论推断 分子中,
分子中, 原子的轨道杂化方式为
原子的轨道杂化方式为___________ , 分子中
分子中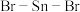 的键角
的键角___________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)下列物质中具有旋光性的是___________(填标号)。
(1)
 中,
中, 的轨道杂化方式为
的轨道杂化方式为 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:(2)用价电子对互斥理论推断
 分子中,
分子中, 原子的轨道杂化方式为
原子的轨道杂化方式为 分子中
分子中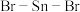 的键角
的键角 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。(3)下列物质中具有旋光性的是___________(填标号)。
A.乙醇( ) ) | B.1, 二氧丙烷( 二氧丙烷( ) ) |
C.乙酸( ) ) | D.乳酸(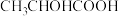 ) ) |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硅材料在生活中占有重要地位。请回答:
(1) 分子的空间结构(以
分子的空间结构(以 为中心)名称为
为中心)名称为___________ ,分子中氮原子的杂化轨道类型是___________ 。 受热分解生成
受热分解生成 和
和 ,其受热不稳定的原因是
,其受热不稳定的原因是___________ 。
(2)由硅原子核形成的三种微粒,电子排布式分别为:①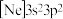 、②
、② 、③
、③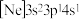 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(1)
 分子的空间结构(以
分子的空间结构(以 为中心)名称为
为中心)名称为 受热分解生成
受热分解生成 和
和 ,其受热不稳定的原因是
,其受热不稳定的原因是(2)由硅原子核形成的三种微粒,电子排布式分别为:①
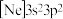 、②
、② 、③
、③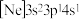 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.微粒半径:③>②>① | B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ | D.得电子能力:①>② |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知下列微粒:①CH4 ②CH2=CH2③CH≡ CH④NH3 ⑤NH4+ ⑥BF3 ⑦H2O ⑧H2O2。试回答下列问题。
(1)分子空间构型为正四面体形的是__________ (填序号,下同)。
(2)中心原子为sp3杂化的是__________ ,中心原子为sp2杂化的是__________ ,中心原子为sp1杂化的是__________ 。
(3)所有原子共平面(含共直线)的是__________ ,共直线的是__________ 。
(1)分子空间构型为正四面体形的是
(2)中心原子为sp3杂化的是
(3)所有原子共平面(含共直线)的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上极为丰富的元素。
(1)下列氮原子的能量最低的是___________。
(2)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一,有关理论认为N2O与CO2具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为___________ ,其空间构型是___________ 。
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是___________ 。
(4)氮可以形成多种离子,如N3-、NH 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。
①写出N2H 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键___________ 。
②N2H 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:___________ 。
(5)I (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为___________ 。
(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是___________ 。
(1)下列氮原子的能量最低的是___________。
A.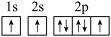 | B.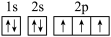 | C.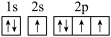 | D.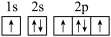 |
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是
(4)氮可以形成多种离子,如N3-、NH
 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。①写出N2H
 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键②N2H
 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:(5)I
 (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.有四种化合物W、X、Y、Z,它们是由短周期元素A、B、C、D、E中的两种元素组成。已知
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为__________ ,W为_________ ,X的结构式________ Y的电子式为______________ 。
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:________________ ,
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图__________________ ,
(3)乙烯分子中有__________ 个σ键,___________ π键。
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图
(3)乙烯分子中有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据所学知识点,完成以下填空。
(1)基态P原子的价电子轨道表示式_______ 。
(2)基态K原子的简化电子排布式为_______ ,其能量最高的电子所在的能级是_______ ,该能级的原子轨道呈_______ 形。
(3)基态Ni原子核外电子的运动状态有_______ 种,基态 中未成对的电子数与成对电子数之比为
中未成对的电子数与成对电子数之比为_______ 。
(4) 的VSEPR模型和空间构型分别为
的VSEPR模型和空间构型分别为_______ 、_______ 。
(5)一氯乙烷( )和四氟乙烯(
)和四氟乙烯( )分子中C的杂化轨道类型分别为
)分子中C的杂化轨道类型分别为_______ 和_______ 。
(6) 分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为
分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为_______ , 分子为
分子为_______ (填“极性分子”或“非极性分子”)。
(1)基态P原子的价电子轨道表示式
(2)基态K原子的简化电子排布式为
(3)基态Ni原子核外电子的运动状态有
 中未成对的电子数与成对电子数之比为
中未成对的电子数与成对电子数之比为(4)
 的VSEPR模型和空间构型分别为
的VSEPR模型和空间构型分别为(5)一氯乙烷(
 )和四氟乙烯(
)和四氟乙烯( )分子中C的杂化轨道类型分别为
)分子中C的杂化轨道类型分别为(6)
 分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为
分子中各原子都满足最外层8电子结构,分子中σ键与π键数目之比为 分子为
分子为
您最近一年使用:0次

 ,却能溶解约40体积
,却能溶解约40体积 ,请从价层电子对的角度入手进行解释
,请从价层电子对的角度入手进行解释





