按要求回答以下内容。
(1)Cu基态原子的价电子排布式_______ ; 它位于周期表的_______ 区。
(2)基态S原子电子占据最高能级的电子云轮廓图为_______ 形; SO2分子中的中心原子杂化方式为_______ ,SO 的空间结构为
的空间结构为_______ 。
(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置_______ ; 基态Ti原子的电子排布式 _______ 。
(4)H2O2的空间结构示意图如下。
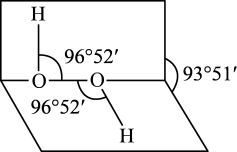
①下列关于H2O2的说法中正确的是_______ (填字母)。
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是_______ 。
(1)Cu基态原子的价电子排布式
(2)基态S原子电子占据最高能级的电子云轮廓图为
 的空间结构为
的空间结构为(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置
(4)H2O2的空间结构示意图如下。

①下列关于H2O2的说法中正确的是
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是
更新时间:2022-04-28 10:08:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】该反应曾用于检测司机是否酒后驾驶:2Cr2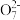 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
(1)基态Cr3+的核外电子排布式为_______ ;配合离子[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______ (填元素符号)。
(2)CH3COOH中C原子的杂化轨道类型为_______ 和_______ ;1molCH3COOH分子中含有σ键的数目为_______ 。
(3)H2O与CH3CH2OH可以任意比例互溶,原因是_______ 、_______ (回答两点)。
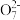 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH(1)基态Cr3+的核外电子排布式为
(2)CH3COOH中C原子的杂化轨道类型为
(3)H2O与CH3CH2OH可以任意比例互溶,原因是
您最近一年使用:0次
【推荐2】磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子核外电子排布式是____________ 。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2→6CaSiO3+P4O10 10C+P4O10→P4+10CO,每生成1 mol P4时,就有________ mol电子发生转移。
(1)磷元素的原子核外电子排布式是
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2→6CaSiO3+P4O10 10C+P4O10→P4+10CO,每生成1 mol P4时,就有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:_____________________ 。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为____________ 。
(3)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:____________ 。
(4)写出3p轨道上有2个未成对电子的元素符号:________ 。
(5)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为____________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为
(3)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:
(4)写出3p轨道上有2个未成对电子的元素符号:
(5)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气: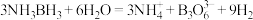 。
。 的结构为
的结构为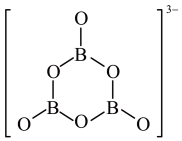 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为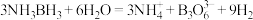 。
。 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)Sn为ⅣA族元素,单质Sn与干燥 反应生成
反应生成 ,常温常压下
,常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为_______ 。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(1)Sn为ⅣA族元素,单质Sn与干燥
 反应生成
反应生成 ,常温常压下
,常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ;SO2的空间构型为___________ (用文字描述)。
(2)Fe2+基态核外电子排布式为___________ 。
(3)H2O分子中的键角___________  离子中的键角(填“大于”、“等于”、“小于”)。
离子中的键角(填“大于”、“等于”、“小于”)。
(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(5)N元素的电负性___________ O元素的电负性(填“大于”、“等于”、“小于”)。
 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(2)Fe2+基态核外电子排布式为
(3)H2O分子中的键角
 离子中的键角(填“大于”、“等于”、“小于”)。
离子中的键角(填“大于”、“等于”、“小于”)。(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=
(5)N元素的电负性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有 、
、 、
、 、
、 、
、 、
、 六种分子,试回答下列问题:
六种分子,试回答下列问题:
(1)由非极性键构成的分子是______ 。
(2)由极性键构成的具有正四面体形结构的分子是______ 。
(3)由极性键构成的具有V形结构的分子是______ 。
 、
、 、
、 、
、 、
、 、
、 六种分子,试回答下列问题:
六种分子,试回答下列问题:(1)由非极性键构成的分子是
(2)由极性键构成的具有正四面体形结构的分子是
(3)由极性键构成的具有V形结构的分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)根据价层电子对互斥模型, 分子中心原子孤电子对数是
分子中心原子孤电子对数是_______ , 分子的空间构型是
分子的空间构型是_______ 。
(2)气态三氧化硫以单分子形式存在,属于_______ 分子(填“极性”、“非极性”),固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
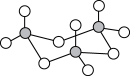
(3) 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,写出一个与 VEEPR模型相同的离子
VEEPR模型相同的离子_______ 。
(4)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:
B.两元素的电负性: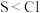
C.高价含氧酸的酸性: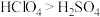
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应: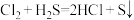
(1)根据价层电子对互斥模型,
 分子中心原子孤电子对数是
分子中心原子孤电子对数是 分子的空间构型是
分子的空间构型是(2)气态三氧化硫以单分子形式存在,属于

(3)
 中心原子的价层电子对数为
中心原子的价层电子对数为 VEEPR模型相同的离子
VEEPR模型相同的离子(4)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:

B.两元素的电负性:
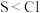
C.高价含氧酸的酸性:
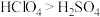
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:
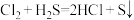
您最近一年使用:0次
【推荐3】从硝酸工业中排放的氮氧化物NOx是一种大气污染物。最常见的吸收法是利用NaOH溶液吸收,发生以下方程:
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:___________ 。
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
(3)C、N、O的第一电离能大小为___________ ,其原因是___________ 。
①NO+NO2=N2O3
②N2O3+2NaOH=2NaNO2+H2O
③2NO2+2NaOH=NaNO2+___________+___________
实验表明,反应②发生的速率大于反应③发生的速率。
(1)补全方程式③并标出电子转移数目:
2NO2+2NaOH=NaNO2+___________+___________
(2)NO2的分子构型和分子的极性分别为___________。
| A.直线形,非极性 | B.角形,极性 | C.平面三角形,非极性 | D.三角锥形,极性 |
您最近一年使用:0次



