地下管线穿过不同的地质结构及潮湿程度不同的土壤带时,由于氧气浓度存在差别,会引起金属管道的腐蚀。其原理如图所示,下列说法正确的是
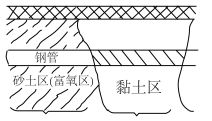

| A.黏土区钢管作正极 |
| B.电子由砂土区钢管流向黏土区钢管 |
| C.每消耗22.4LO2最终可生成铁锈1mol |
D.砂土区钢管表面发生的电极反应可能为 |
23-24高三上·广东江门·阶段练习 查看更多[3]
更新时间:2023-10-02 17:55:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】负载有Pt和Ag的活性炭,可选择性去除Cl-实现废酸的纯化,其工作原理如图所示。下列说法错误的是

| A.Pt作原电池正极 |
| B.电子由Ag经活性炭流向Pt |
| C.负极的电极方程式:Ag-e-+Cl-=AgCl↓ |
| D.每消耗11.2L的O2,最多去除2molCl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验小组中甲同学按图完成实验,发现电流计指针偏转,乙同学将图中盐桥(琼脂和饱和氯化钾)换成U形铜丝代替盐桥,发现电流计指针也发生偏转,以下说法正确的是
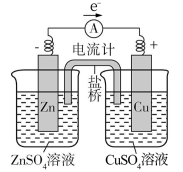

| A.甲同学实验过程中,ZnSO4溶液中阴离子总浓度不会发生改变 |
| B.甲同学实验过程中,Zn片被氧化,铜片被还原 |
| C.乙同学将盐桥换成铜丝后,导线中电流方向不会发生变化 |
| D.乙同学将盐桥换成铜丝后,U形铜丝的两端电极反应类型一致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于如图所示装置的叙述,错误的是
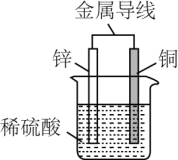

| A.铜是正极,质量不断增加 |
| B.锌片质量逐渐减少 |
| C.电流从铜片经导线流向锌片 |
| D.正极的电极反应式:2H++2e-=H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一种熔融碳酸盐燃料电池原理示意图如图。下列有关该电池的说法正确的是
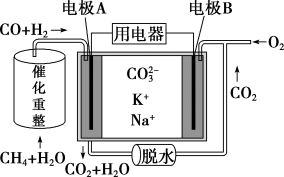

| A.反应CH4+H2O=3H2+CO,每消耗1 mol CH4转移8mol电子 |
| B.电极A上H2参与的电极反应为H2+2OH-_2e-=2H2O |
C.电池工作时,CO 向电极B移动 向电极B移动 |
D.电极B上发生的电极反应为O2+2CO2+4e-=2CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应方程式为:Zn+Ag2O=ZnO+2Ag,其中一个电极反应为:Zn+2OH--2e-=ZnO+H2O;下列叙述正确的是
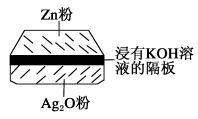

| A.在使用过程中,电解质KOH被不断消耗 |
| B.Zn是正极,Ag2O是负极 |
| C.每转移2mole-,有232gAg2O被还原 |
| D.使用过程中,电子由Ag2O极经外电路流向Zn极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有一种MCPC型燃料电池,该电池所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应为:2H2+O2=2H2O,负极反应为H2+ -2e-=H2O+CO2。下列说法中正确的是
-2e-=H2O+CO2。下列说法中正确的是
 -2e-=H2O+CO2。下列说法中正确的是
-2e-=H2O+CO2。下列说法中正确的是| A.正极反应为4OH--4e-=2H2O+O2↑ |
B.放电时 向负极移动 向负极移动 |
C.放电时,电池中 的物质的量将逐渐减少 的物质的量将逐渐减少 |
| D.电路中的电子经正极、负极、熔融的K2CO3后再流回正极,形成闭合回路 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
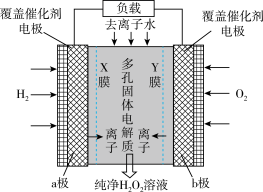
【推荐2】2019年《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示(已知:H2O2 H++HO
H++HO ,Ka=2.4×10-12)。下列说法错误的是( )
,Ka=2.4×10-12)。下列说法错误的是( )
 H++HO
H++HO ,Ka=2.4×10-12)。下列说法错误的是( )
,Ka=2.4×10-12)。下列说法错误的是( )
| A.X膜为阳离子交换膜 |
| B.每生成1molH2O2外电路通过4mole- |
| C.催化剂可加快单位时间内反应中电子的转移数目 |
| D.a极上的电极反应为:H2-2e-=2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于金属防腐的相关描述正确的是
| A.铁与锌接在一起后,投入盐酸中铁就不再被腐蚀 |
| B.纯铁在空气中不会发生电化学腐蚀 |
| C.石墨连电源负极,铁连电源正极,铁不易被腐蚀 |
| D.铜线与铝线相接,铜易腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用下列实验装置进行相应实验,装置正确且能达到相应实验目的的是
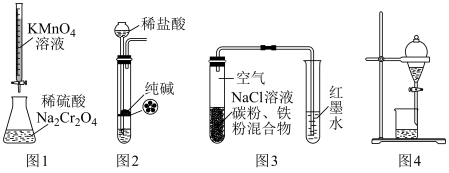

| A.用图1所示装置测定Na2C2O4溶液的物质的量浓度 |
| B.用图2所示装置均匀制取纯净的二氧化碳气体 |
| C.用图3所示装置检验该条件下铁发生了析氢腐蚀 |
| D.用图4所示装置分离乙酸乙酯与NaOH的水溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是
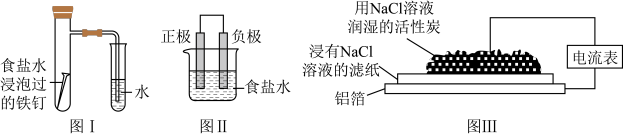
| A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑ |
| D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
您最近一年使用:0次

 +H2O
+H2O 2Fe2++
2Fe2++ +2H+,如图所示是一套电化学实验装置,图中C、D 均为铂电极,U 为盐桥,G 是灵敏电流计,其指针总是偏向电源负极。A 杯中为FeCl3溶液,B 杯中为Na2SO3溶液。以下关于该装置的说法错误的是(
+2H+,如图所示是一套电化学实验装置,图中C、D 均为铂电极,U 为盐桥,G 是灵敏电流计,其指针总是偏向电源负极。A 杯中为FeCl3溶液,B 杯中为Na2SO3溶液。以下关于该装置的说法错误的是(
 Cd(OH)2 + 2Ni(OH)2,其电解质溶液为KOH溶液。有关该电池的下列说法不正确的是
Cd(OH)2 + 2Ni(OH)2,其电解质溶液为KOH溶液。有关该电池的下列说法不正确的是

