回答下列问题:
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)9.03×1023个CO2的物质的量是_______ ,在标准状况下的体积为_______ 。
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为_______ ,所含氧原子数之比为_______ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=_______ 。
(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为_______ 。
(6)FeCl2溶液通入氯气的反应,用离子方程式表示_______ 。
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为_______ ,该反应中被还原的物质是_______ (填化学式)。
(1)NaClO中Cl的化合价为
(2)9.03×1023个CO2的物质的量是
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
(6)FeCl2溶液通入氯气的反应,用离子方程式表示
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为
更新时间:2023/10/05 11:15:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】物质的量是联系宏观和微观的桥梁,也是定量研究化学的基础。
Ⅰ.甲烷(CH4)是一种无色无味的气体,是天然气的主要成分。
(1)现有2 mol CH4,它的摩尔质量是_______ ,要把CH4完全燃烧,消耗氧气_______ g。
(2)标准状况下,CH4的密度为_______ (保留3位有效数字)。如果11.2 L CH4中含有x个氢原子,则阿伏加德罗常数的值为_______ 。
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为_______ ,密度之比为_______ 。若把质量相等的这两种气体混合,则混合气体的平均相对分子质量为_______ (保留2位有效数字)。
(4)某沼气成分是CH4和CO2.取2 L该沼气与4 L O2点燃充分反应后,除去水分,剩余气体的体积为3 L。该沼气中CH4和CO2的物质的量之比为_______ (气体体积均在同温同压下测定)。
Ⅱ.溶液中所含溶质的多少可用不同的浓度来表示。
(5)下列各溶液中,Na+ 浓度最小的是_______
(6)98%的浓硫酸(密度为1.84 g·mL-1),可采取不同的形式表示。以下根据表示方法的定义,错误 的是_______
Ⅰ.甲烷(CH4)是一种无色无味的气体,是天然气的主要成分。
(1)现有2 mol CH4,它的摩尔质量是
(2)标准状况下,CH4的密度为
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为
(4)某沼气成分是CH4和CO2.取2 L该沼气与4 L O2点燃充分反应后,除去水分,剩余气体的体积为3 L。该沼气中CH4和CO2的物质的量之比为
Ⅱ.溶液中所含溶质的多少可用不同的浓度来表示。
(5)下列各溶液中,Na+ 浓度最小的是_______
| A.4L 0.5 mol·L-1 NaCl 溶液 | B.1L 0.3 mol·L-1 Na2SO4 溶液 |
| C.8L 0.4 mol·L-1 NaOH 溶液 | D.2L 0.15 mol·L-1 Na3PO4 溶液 |
| A.物质的量浓度:单位体积溶液中含溶质的物质的量:18.4 mol·L-1 |
| B.质量浓度:单位体积溶液中含溶质的质量:1.84 kg·L-1 |
C.把浓硫酸当作硫酸的水合物,用化学式表示:H2SO4·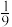 H2O H2O |
D.把浓硫酸当作复合氧化物,用化学式表示:SO3· H2O H2O |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾 ,碘酸钾和碘化钾在酸性溶液中能发生反应:
,碘酸钾和碘化钾在酸性溶液中能发生反应: 。
。
(1)该反应中,氧化剂是_______ (填化学式),氧化产物和还原产物的物质的量之比是_______ 。
Ⅱ.钠元素在自然界中以多种化合物的形式存在。
(2) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)“侯氏制碱法”曾为世界制碱工业做出了突出贡献,某化学兴趣小组在实验室中模拟侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图:
,实验流程如图: 通入饱和氨盐水中,该反应的化学方程式为
通入饱和氨盐水中,该反应的化学方程式为_______ 。
②实验室模拟“侯氏制碱法”,下列操作未涉及的是_______ (填标号)。
(4)标准状况下,现有a.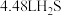 b.
b. 个
个 分子 c.
分子 c.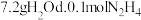 四种物质,其中物质的量最大的是
四种物质,其中物质的量最大的是_______ (填标号,下同);质量最小的是_______ ;含 个数最多的是
个数最多的是_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾
 ,碘酸钾和碘化钾在酸性溶液中能发生反应:
,碘酸钾和碘化钾在酸性溶液中能发生反应: 。
。(1)该反应中,氧化剂是
Ⅱ.钠元素在自然界中以多种化合物的形式存在。
(2)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与
与 反应的化学方程式:
反应的化学方程式:(3)“侯氏制碱法”曾为世界制碱工业做出了突出贡献,某化学兴趣小组在实验室中模拟侯氏制碱法制备
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图:
,实验流程如图: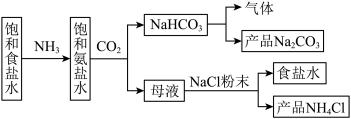
 通入饱和氨盐水中,该反应的化学方程式为
通入饱和氨盐水中,该反应的化学方程式为②实验室模拟“侯氏制碱法”,下列操作未涉及的是
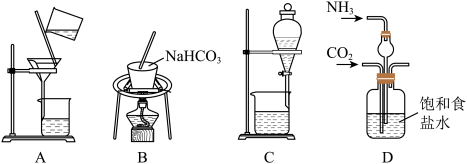
(4)标准状况下,现有a.
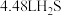 b.
b. 个
个 分子 c.
分子 c.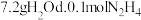 四种物质,其中物质的量最大的是
四种物质,其中物质的量最大的是 个数最多的是
个数最多的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
(1)49gH2SO4中氧原子数为_______ 。
(2)16g物质A中含有的分子数为3.01×1023,则A的摩尔质量为_______ 。
(3)在标准状况下,1.7gNH3与标准状况下_______ LH2S含有相同数目的氢原子。
(4)0.17gOH-中质子的物质的量为_______ ,电子的微粒数为_______ 个。
(5)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的分子数为_______ 。
(6)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中SO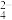 的物质的量浓度为
的物质的量浓度为_______ 。
(7)标准状况下,等质量的氧气与臭氧的体积之比为_______ ,氧原子个数之比为_______ 。
(8)同温同压下,容器A中充满CO2气体,容器B中充满N2,若V(A)∶V(B)=3∶2,则两容器中的气体密度比为_______ 。
(1)49gH2SO4中氧原子数为
(2)16g物质A中含有的分子数为3.01×1023,则A的摩尔质量为
(3)在标准状况下,1.7gNH3与标准状况下
(4)0.17gOH-中质子的物质的量为
(5)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的分子数为
(6)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中SO
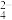 的物质的量浓度为
的物质的量浓度为(7)标准状况下,等质量的氧气与臭氧的体积之比为
(8)同温同压下,容器A中充满CO2气体,容器B中充满N2,若V(A)∶V(B)=3∶2,则两容器中的气体密度比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列10种物质:①铝;②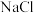 ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨
;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨ ;⑩蔗糖。
;⑩蔗糖。
(1)按物质的树状分类法填写表格的空白处:
(2)写出⑨在水中的电离方程式___________ 。
(3)上述10种物质中,有两种物质之间发生的反应可用 表示,该离子反应对应的化学方程式为
表示,该离子反应对应的化学方程式为___________ 。
(4)写出⑤与少量③反应的离子方程式___________ 。
(5)写出⑧与⑨反应的离子方程式___________ 。
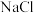 ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨
;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨ ;⑩蔗糖。
;⑩蔗糖。(1)按物质的树状分类法填写表格的空白处:
| 类别 | 金属单质 | 氧化物 | 电解质 | 非电解质 | |
| 属于该类的物质(填标号) | ① | ⑥⑦⑧ |
(3)上述10种物质中,有两种物质之间发生的反应可用
 表示,该离子反应对应的化学方程式为
表示,该离子反应对应的化学方程式为(4)写出⑤与少量③反应的离子方程式
(5)写出⑧与⑨反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硅、硫和氮等元素的踪迹。
I.利用下列物品回答问题:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片
(1)直接使用了硅单质的是_______ (填标号,下同)。
(2)直接使用了二氧化硅的是_______ 。
II.硫、氮的氧化物是大气的主要污染物,汽车尾气、工业废气、烟道气等中均含有硫或氮元素的氧化物,主要以 和
和 的形式存在。
的形式存在。
(3)下列关于 和
和 的叙述中正确的是_______(填标号)。
的叙述中正确的是_______(填标号)。
(4)质量相同的 和
和 的物质的量之比为
的物质的量之比为_______ 。
(5) 能被酸性
能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_______ 。
(6)利用氨水可以将 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
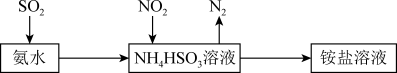
用氨水吸收 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式:_______ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为_______ 。
I.利用下列物品回答问题:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片
(1)直接使用了硅单质的是
(2)直接使用了二氧化硅的是
II.硫、氮的氧化物是大气的主要污染物,汽车尾气、工业废气、烟道气等中均含有硫或氮元素的氧化物,主要以
 和
和 的形式存在。
的形式存在。(3)下列关于
 和
和 的叙述中正确的是_______(填标号)。
的叙述中正确的是_______(填标号)。| A.两种气体都无色有毒,且都可用水吸收以消除对空气的污染 |
B.实验室制备 、 、 时,均可用向上排空气的方法收集 时,均可用向上排空气的方法收集 |
| C.两种气体都具有强氧化性,因此都能够使品红溶液褪色 |
D. 与 与 反应转化为 反应转化为 ,属于氮的固定 ,属于氮的固定 |
 和
和 的物质的量之比为
的物质的量之比为(5)
 能被酸性
能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(6)利用氨水可以将
 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
用氨水吸收
 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①H2O②Cu③BaCO3④Fe(OH)3胶体⑤酒精⑥CO2⑦稀硫酸⑧NaHSO4固体
(1)以上物质中属于混合物的是___ (填序号,下同),属于电解质的是___ 。
(2)向④中逐滴滴加⑦,可观察到的现象是___ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)__ 。
(5)关于NaHSO4固体:通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热融化时只能电离出两种不同的离子。
①NaHSO4在水溶液中的电离方程式为___ 。
②NaHSO4在熔融状态下的电离方程式为__ 。
Ⅰ.现有以下物质:①H2O②Cu③BaCO3④Fe(OH)3胶体⑤酒精⑥CO2⑦稀硫酸⑧NaHSO4固体
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)
(5)关于NaHSO4固体:通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热融化时只能电离出两种不同的离子。
①NaHSO4在水溶液中的电离方程式为
②NaHSO4在熔融状态下的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】“中国芯”的主要原料是高纯单晶硅,反应SiCl4(g)+2H2(g) Si(s)+4HCl(g)可用于纯硅的制备:
Si(s)+4HCl(g)可用于纯硅的制备:
(1)氯元素的一个原子中含18个中子,该氯原子是___________ (用化学符号表示)。Si原子的结构示意图是___________ 。
(2)反应物SiCl4中硅的化合价是___________ ,被氧化的元素是___________ (写元素名称)。
(3)用双线桥法表示该反应电子转移的方向和数目:SiCl4(g)+2H2(g) Si(s)+4HCl(g)
Si(s)+4HCl(g)
______________________
(4)将反应生成的HCl气体通入到适量水中制取盐酸。若要制取500mL1mol·L-1的盐酸,则需要HCl的体积(标准状况下)是___________ 。
 Si(s)+4HCl(g)可用于纯硅的制备:
Si(s)+4HCl(g)可用于纯硅的制备:(1)氯元素的一个原子中含18个中子,该氯原子是
(2)反应物SiCl4中硅的化合价是
(3)用双线桥法表示该反应电子转移的方向和数目:SiCl4(g)+2H2(g)
 Si(s)+4HCl(g)
Si(s)+4HCl(g)(4)将反应生成的HCl气体通入到适量水中制取盐酸。若要制取500mL1mol·L-1的盐酸,则需要HCl的体积(标准状况下)是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识回答下列问题:
(1)黄铁矿(主要成分为 ,其中Fe为+2价)的燃烧是工业上制硫酸时得到
,其中Fe为+2价)的燃烧是工业上制硫酸时得到 的途径之一,其反应为
的途径之一,其反应为 。
。
① 中硫元素的化合价为
中硫元素的化合价为___________ 价,该化合物中
___________ 。
②该反应中氧化剂与还原剂的质量之比为___________ 。
③该反应的氧化产物为___________ (填化学式)。
(2)次磷酸( )是一种精细的磷化工产品,具有较强的还原性,
)是一种精细的磷化工产品,具有较强的还原性, 可与溶液中的
可与溶液中的 发生反应,生成物为Ag和
发生反应,生成物为Ag和 ,从而可用于化学镀银。
,从而可用于化学镀银。
已知: 和
和 在溶液中均以分子的形成存在。
在溶液中均以分子的形成存在。
① 的相对分子质量为
的相对分子质量为___________ ,该分子中的磷原子和氧原子的个数之比为___________ 。
②该反应中 体现了
体现了___________ (填“还原”或“氧化”)性。
③该反应的离子方程式为___________ 。
(1)黄铁矿(主要成分为
 ,其中Fe为+2价)的燃烧是工业上制硫酸时得到
,其中Fe为+2价)的燃烧是工业上制硫酸时得到 的途径之一,其反应为
的途径之一,其反应为 。
。①
 中硫元素的化合价为
中硫元素的化合价为
②该反应中氧化剂与还原剂的质量之比为
③该反应的氧化产物为
(2)次磷酸(
 )是一种精细的磷化工产品,具有较强的还原性,
)是一种精细的磷化工产品,具有较强的还原性, 可与溶液中的
可与溶液中的 发生反应,生成物为Ag和
发生反应,生成物为Ag和 ,从而可用于化学镀银。
,从而可用于化学镀银。已知:
 和
和 在溶液中均以分子的形成存在。
在溶液中均以分子的形成存在。①
 的相对分子质量为
的相对分子质量为②该反应中
 体现了
体现了③该反应的离子方程式为
您最近一年使用:0次
【推荐3】氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:S+2KNO3+3C K2S+3CO2↑+N2↑。在此反应中,还原剂为
K2S+3CO2↑+N2↑。在此反应中,还原剂为___________ (填化学式),还原产物是___________ (填化学式),当该反应转移3mol电子时,产生气体的体积为___________ L(标况下)。
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为___________ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:S+2KNO3+3C
 K2S+3CO2↑+N2↑。在此反应中,还原剂为
K2S+3CO2↑+N2↑。在此反应中,还原剂为(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮、硫、氯是重要的非金属元素,根据它们的性质回答下列问题:
(1)农业生产中常用到的氮肥是铵盐,检验某化肥中铵盐的方法是将待检物取出少量放入试管中,然后___________ (填标号);
A.加热,用红色石蕊试纸放在试管口检验
B.加入氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
C.加入碱溶液,加热,再滴入酚酞试液
(2)下列物质中,既能与盐酸反应又能与NaOH溶液反应的是___________ (填标号);
①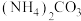 ②
② ③
③
(3)许多氯的化合物是重要的杀菌消毒剂,其中漂白粉的主要成分为 和
和 ,其中有效成分为
,其中有效成分为___________ 。
(1)农业生产中常用到的氮肥是铵盐,检验某化肥中铵盐的方法是将待检物取出少量放入试管中,然后
A.加热,用红色石蕊试纸放在试管口检验
B.加入氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
C.加入碱溶液,加热,再滴入酚酞试液
(2)下列物质中,既能与盐酸反应又能与NaOH溶液反应的是
①
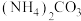 ②
② ③
③
(3)许多氯的化合物是重要的杀菌消毒剂,其中漂白粉的主要成分为
 和
和 ,其中有效成分为
,其中有效成分为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: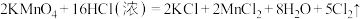 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: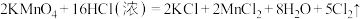 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近一年使用:0次



