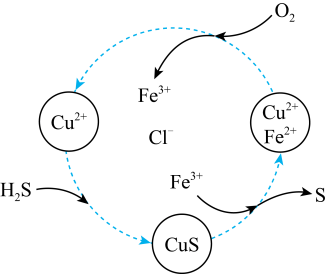
按要求完成下列化学用语
(1)碳酸氢钠的电离方程式_______ 。
(2)氢氧化铜的电离方程式_______ 。
(3)Na与水反应离子方程式_______ 。
(4)Na2O2与二氧化碳反应的化学方程式_______ 。
(5)工业制备漂白粉的化学方程式_______ 。
(6)过量碳酸氢钠溶液与澄清石灰水反应的离子方程式_______ 。
(7)Na2CO3溶液与少量盐酸反应离子方程式_______ 。
(1)碳酸氢钠的电离方程式
(2)氢氧化铜的电离方程式
(3)Na与水反应离子方程式
(4)Na2O2与二氧化碳反应的化学方程式
(5)工业制备漂白粉的化学方程式
(6)过量碳酸氢钠溶液与澄清石灰水反应的离子方程式
(7)Na2CO3溶液与少量盐酸反应离子方程式
更新时间:2022-11-04 09:09:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】我国空间站基本建成,宇航员常年在轨工作。宇航员所需氧气,是通过电解水来制备的。对空间站有害的 是通过LiOH、KOH和
是通过LiOH、KOH和 吸收的。
吸收的。
(1)Li的原子结构示意图为___________ 。
(2)电解水时加入KOH以增强导电性,KOH的电离方程式为___________ 。
(3) 与
与 反应和
反应和 与
与 反应相似。
反应相似。 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(4)宇航员一天大约消耗标况下560 L的氧气,若全部由电解水提供,需要电解水___________ g。
 是通过LiOH、KOH和
是通过LiOH、KOH和 吸收的。
吸收的。(1)Li的原子结构示意图为
(2)电解水时加入KOH以增强导电性,KOH的电离方程式为
(3)
 与
与 反应和
反应和 与
与 反应相似。
反应相似。 与
与 反应的化学方程式为
反应的化学方程式为(4)宇航员一天大约消耗标况下560 L的氧气,若全部由电解水提供,需要电解水
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列十种物质:①H2②铝 ③甲烷 ④CO2 ⑤H2SO4⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨盐酸 ⑩Al2(SO4)3
(1)上述物质中属于电解质的有:_____________________ 。(填序号)
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-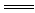 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为_________________ 。
(3)⑩在水中的电离方程式为__________________ ,17.1g该物质溶于水配成250mL溶液,物质的量浓度为_______________ mol·L-1。
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2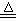 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是___________ (填化学式),还原剂与氧化剂的物质的量之比是_________ 。写出该反应的离子方程式_____________________________ 。
(1)上述物质中属于电解质的有:
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-
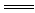 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为(3)⑩在水中的电离方程式为
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2
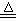 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列物质①NaHSO4、②H2O、③NaOH、④BaSO4、⑤NH3、⑥CO2、⑦CH3COOH、⑧CH3OH、⑨Fe、⑩氯化钠溶液
(1)属于非电解质的是______ ;属于强电解质的是______ ;既不是电解质也不是非电解质,且常温下能导电的物质是______ (均填序号)。
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
①写出H2SO3的第二步电离方程式______ 。
②试比较 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:______ 。
③写出少量CO2与NaClO反应的离子方程式______ 。
(1)属于非电解质的是
(2)已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
| 物质 | H2CO3 | H2SO3 | HClO | |
| 电离平衡常数 | Ka1 | 4.40×10-7 | 1.54×10-2 | 2.95×10-8 |
| Ka2 | 5.61×10-11 | 1.02×10-7 | ||
②试比较
 、
、 和HCIO的酸性强弱:
和HCIO的酸性强弱:③写出少量CO2与NaClO反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I、(1) 4.9gH3PO4的物质的量为____ ,其中含有____ molH,含有______ 个O,含磷元素___ g,若它可与6gNaOH完全反应生成正盐,则H3PO4为_____ 元酸。
(2)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为____ , 该金属元素为______ 。
II、有一包白色固体,可能含有CaCO3、Na2S04、KNO3、CuSO4、BaCl2五种物质中的一种或几种,现进行如下实验:
(1)取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
(2)继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
(3)取少量(2)中的溶液滴加Ba(NO3)2为溶液,有白色沉淀生成,加稀硝酸沉淀不溶。
根据上述实验现象判断:该白色固体中一定含有____ ,一定不含有____ ,可能含有_____ 。
III、小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.504gNaHCO3, 2片小苏打片和胃酸完全中和,被中和的H+是___ mol。
(2)胃舒平每片含0.234gAl(OH)3。写出胃舒平中和胃酸的离子反应方程式___ , 中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式盐。取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,则该碱式盐样品中氢氧根与碳酸根的物质的量之比为_____ 。
(2)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为
II、有一包白色固体,可能含有CaCO3、Na2S04、KNO3、CuSO4、BaCl2五种物质中的一种或几种,现进行如下实验:
(1)取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
(2)继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
(3)取少量(2)中的溶液滴加Ba(NO3)2为溶液,有白色沉淀生成,加稀硝酸沉淀不溶。
根据上述实验现象判断:该白色固体中一定含有
III、小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.504gNaHCO3, 2片小苏打片和胃酸完全中和,被中和的H+是
(2)胃舒平每片含0.234gAl(OH)3。写出胃舒平中和胃酸的离子反应方程式
(3)达喜的化学成分是铝和镁的碱式盐。取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,则该碱式盐样品中氢氧根与碳酸根的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的化学方程式,是离子反应的写离子方程式。
(1)把 通入水中
通入水中_______ ;
(2)实验室利用 固体、
固体、 固体混合加热制备
固体混合加热制备
_______ ;
(3) 的催化氧化
的催化氧化_______ ;
(4) 溶于水
溶于水_______ ;
(5) 被烧碱溶液吸收生成两种钠盐
被烧碱溶液吸收生成两种钠盐_______ ;
(6)物质的量之比为 的
的 和
和 混合气体恰好被烧碱溶液吸收生成一种钠盐
混合气体恰好被烧碱溶液吸收生成一种钠盐_______ ;
(7) 和稀
和稀 的反应
的反应_______ ;
(8) 和浓
和浓 的反应
的反应______ ;
(9)C和浓 的反应
的反应_______ ;
(10)浓硝酸见光分解_______ 。
(1)把
 通入水中
通入水中(2)实验室利用
 固体、
固体、 固体混合加热制备
固体混合加热制备
(3)
 的催化氧化
的催化氧化(4)
 溶于水
溶于水(5)
 被烧碱溶液吸收生成两种钠盐
被烧碱溶液吸收生成两种钠盐(6)物质的量之比为
 的
的 和
和 混合气体恰好被烧碱溶液吸收生成一种钠盐
混合气体恰好被烧碱溶液吸收生成一种钠盐(7)
 和稀
和稀 的反应
的反应(8)
 和浓
和浓 的反应
的反应(9)C和浓
 的反应
的反应(10)浓硝酸见光分解
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某化学课外小组用Cl2和NaOH固体制取84消毒液。请回答下列问题:
(1)制取84消毒液的离子方程式为__________ 。
(2)制取时需要0.4 mol·L-1的NaOH溶液450mL,配制时用托盘天平称量NaOH固体的质量为_______ ,配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、_______ 。
(3)该消毒液也可用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出化学反应方程式:_________ 。
(4)该消毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,某同学向溶液中滴加紫色石蕊试液,出现________ 现象,证明消毒液已失效。
(1)制取84消毒液的离子方程式为
(2)制取时需要0.4 mol·L-1的NaOH溶液450mL,配制时用托盘天平称量NaOH固体的质量为
(3)该消毒液也可用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出化学反应方程式:
(4)该消毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,某同学向溶液中滴加紫色石蕊试液,出现
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
(1)写出生成黄绿色气体的化学方程式:__________________________________________ 。
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)__________ (填“能”或“不能”)同时使用,其原因是_________________________________ 。
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石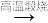


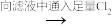 漂白粉溶液
漂白粉溶液  漂白粉
漂白粉
①请写出在制取漂白粉的实验过程中发生的氧化还原反应的化学方程式:___________________________ 。
②当通入氯气较快时,反应产物为 、
、 和
和 ,已知每消耗1
,已知每消耗1
 的同时消耗1
的同时消耗1
 ,请写出此反应的化学方程式:
,请写出此反应的化学方程式:_______________________________________ 。
(1)写出生成黄绿色气体的化学方程式:
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石
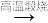


 漂白粉溶液
漂白粉溶液  漂白粉
漂白粉①请写出在制取漂白粉的实验过程中发生的氧化还原反应的化学方程式:
②当通入氯气较快时,反应产物为
 、
、 和
和 ,已知每消耗1
,已知每消耗1
 的同时消耗1
的同时消耗1
 ,请写出此反应的化学方程式:
,请写出此反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.钠及其化合物有广泛的应用,请根据题意回答下列问题:
(1)Na是一种非常活泼的金属,实验室一般将钠保存在____ 中。
(2)氢化钠(NaH)可在野外用作生氢剂,其中氢元素的化合价为___ 价。
(3)Na2O2常用作呼吸面具或潜水艇中氧气的来源,请写出Na2O2与CO2反应的化学方程式:____ 。
II.现用0.5 mol•L-1的NaCl溶液配制450 mL0.1 mol•L-1的NaCl溶液,按要求回答下列问题:
(4)应选用的玻璃仪器有烧杯、量筒、玻璃棒、____ 。
(5)容量瓶在使用前,首先要____ 。
(6)需量取0.5 mol•L-1NaCl溶液的体积是____ mL。
(1)Na是一种非常活泼的金属,实验室一般将钠保存在
(2)氢化钠(NaH)可在野外用作生氢剂,其中氢元素的化合价为
(3)Na2O2常用作呼吸面具或潜水艇中氧气的来源,请写出Na2O2与CO2反应的化学方程式:
II.现用0.5 mol•L-1的NaCl溶液配制450 mL0.1 mol•L-1的NaCl溶液,按要求回答下列问题:
(4)应选用的玻璃仪器有烧杯、量筒、玻璃棒、
(5)容量瓶在使用前,首先要
(6)需量取0.5 mol•L-1NaCl溶液的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当容易变质。某实验小组以过氧化钠为研究对象,进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品溶解,___________ (填写实验操作和现象),证明Na2O2已变质。
(2)该实验小组为了测定已变质的过氧化钠中Na2O2的质量分数,称取a g样品,并设计了如图所示的装置。
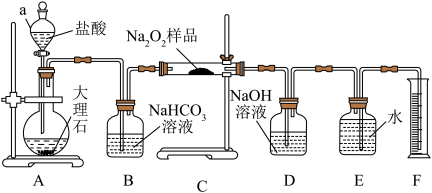
①装置A中仪器a的名称是___________ ,装置B的作用是___________ 。
②将仪器连接好以后,必须进行的操作是___________ 。
③写出装置C中发生反应的化学方程式:___________ 。
④实验结束后,在读取生成气体的体积时,你认为合理的是___________ (填序号)。
a.直接读取体积,不需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平
⑤读出量筒内水的体积后,折算成标准状况下气体的体积为V mL,则该样品中过氧化钠的质量分数为___________ 。
(1)探究一包Na2O2样品是否已经变质:取少量样品溶解,
(2)该实验小组为了测定已变质的过氧化钠中Na2O2的质量分数,称取a g样品,并设计了如图所示的装置。

①装置A中仪器a的名称是
②将仪器连接好以后,必须进行的操作是
③写出装置C中发生反应的化学方程式:
④实验结束后,在读取生成气体的体积时,你认为合理的是
a.直接读取体积,不需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平
⑤读出量筒内水的体积后,折算成标准状况下气体的体积为V mL,则该样品中过氧化钠的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)研究物质时会涉及物质的组成、分类、性质和用途等方面。
①Na2O2属于____________ (填物质的类别),检验其组成中所含阳离子的方法是_____________ 。
②将包有少量____ 色Na2O2固体的棉花放在石棉网上,用滴管向棉花上滴几滴水,观察到的现象是__________________ ,由此得出的结论是_________________________________ 。
③在潜水艇和消防员的呼吸面具中,Na2O2所发生反应的化学方程式为_________________________ ,从氧化剂和还原剂的角度分析,在该反应中Na2O2的作用是___________________ 。某潜水艇上有25人,如果每人每分钟消耗的O2在标准状况下体积为0.80L(标准状况下O2的密度为1.429g/L),假设所需要的O2全部由Na2O2来提供,则该潜水艇一天所需要的Na2O2的物质的量是_____________ 。
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:__________________________________________________ 。
②过量CO2与NaOH溶液:_____________________________________________ 。
③工业制漂白液:______________________________________________________ 。
④生活中漂白粉的漂白原理:____________________________________________ 。
①Na2O2属于
②将包有少量
③在潜水艇和消防员的呼吸面具中,Na2O2所发生反应的化学方程式为
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:
②过量CO2与NaOH溶液:
③工业制漂白液:
④生活中漂白粉的漂白原理:
您最近一年使用:0次