过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当容易变质。某实验小组以过氧化钠为研究对象,进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品溶解,___________ (填写实验操作和现象),证明Na2O2已变质。
(2)该实验小组为了测定已变质的过氧化钠中Na2O2的质量分数,称取a g样品,并设计了如图所示的装置。
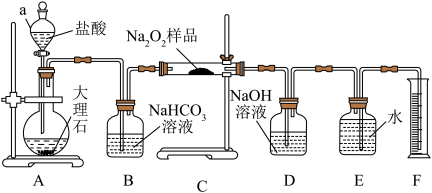
①装置A中仪器a的名称是___________ ,装置B的作用是___________ 。
②将仪器连接好以后,必须进行的操作是___________ 。
③写出装置C中发生反应的化学方程式:___________ 。
④实验结束后,在读取生成气体的体积时,你认为合理的是___________ (填序号)。
a.直接读取体积,不需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平
⑤读出量筒内水的体积后,折算成标准状况下气体的体积为V mL,则该样品中过氧化钠的质量分数为___________ 。
(1)探究一包Na2O2样品是否已经变质:取少量样品溶解,
(2)该实验小组为了测定已变质的过氧化钠中Na2O2的质量分数,称取a g样品,并设计了如图所示的装置。

①装置A中仪器a的名称是
②将仪器连接好以后,必须进行的操作是
③写出装置C中发生反应的化学方程式:
④实验结束后,在读取生成气体的体积时,你认为合理的是
a.直接读取体积,不需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平
⑤读出量筒内水的体积后,折算成标准状况下气体的体积为V mL,则该样品中过氧化钠的质量分数为
更新时间:2023-10-03 16:44:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与我们的生活、生产、环境等息息相关。回答下列问题:
(1)明矾的化学式为KAl(SO4)·12H2O,它常用于净水。明矾放入水中起净水作用的物质是___________ 。明矾与过量NaOH溶液反应的离子方程式是___________ 。
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ 性,该转化反应中Fe3+作___________ 剂。
(3)某无土栽培用的营养液中,c(NH ):c(SO
):c(SO ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为___________ 。
(4)汽车燃料中一般不含氮元素,尾气中所含NO是如何产生的?___________ 。能减少或有效控制汽车尾气污染有效且可行的措施是___________ 。
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2(微溶于水)都可与水发生反应生成碱和氧气。写出Na2O2与水反应的化学方程式:___________ 。这两种物质中选___________ 作为供氧剂更好,理由是___________ 。
(1)明矾的化学式为KAl(SO4)·12H2O,它常用于净水。明矾放入水中起净水作用的物质是
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)某无土栽培用的营养液中,c(NH
 ):c(SO
):c(SO ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为(4)汽车燃料中一般不含氮元素,尾气中所含NO是如何产生的?
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2(微溶于水)都可与水发生反应生成碱和氧气。写出Na2O2与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据要求,写出化学方程式或者离子方程式;
(1)氯气和石灰乳反应制取漂白粉的化学方程式___________ ;
(2)过氧化钠和水反应的化学方程式___________ ;
(3)写出 和足量
和足量 反应的离子方程式
反应的离子方程式___________ ;
(4)碘盐中的 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式___________ ;
(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式___________ ;
(6)铜和浓硫酸加热反应的化学方程式___________ 。
(1)氯气和石灰乳反应制取漂白粉的化学方程式
(2)过氧化钠和水反应的化学方程式
(3)写出
 和足量
和足量 反应的离子方程式
反应的离子方程式(4)碘盐中的
 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式
(6)铜和浓硫酸加热反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】对比分析钠及其化合物的特点,请完成下列空白。
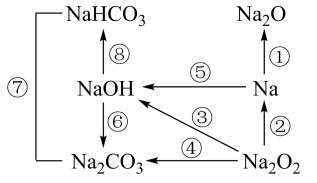
(1)如图所示转化关系中属于氧化还原反应的有_______ 个,其中可用于呼吸面具或潜水艇供氧的反应的化学方程式是_______ ;_______ 。
(2)日常生活中常用到苏打和小苏打,鉴别它们的方法有多种。例如:
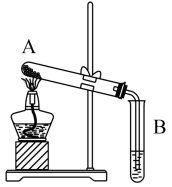
方法①:如图所示装置,这是根据它们具有不同的_______ 性质加以鉴别的。实验过程中,可以观察到的现象为A试管口_______ ,试管B中_______ ,试管A中发生反应的化学方程式是_______ 。用_______ 的方法可以除去混在Na2CO3粉末中少量的NaHCO3。
方法②:取等物质的量的苏打和小苏打分别于试管中,再分别加入足量盐酸充分反应,比较现象得出先出现气泡者为_______ 。请写出相关反应的离子方程式:_______ 。
(3)测定Na2CO3(含氯化钠杂质)样品中Na2CO3的质量分数:①称取m g样品放入烧杯内加水溶解;②加入过量的氯化钙溶液充分反应;③过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为_______ 。
(1)如图所示转化关系中属于氧化还原反应的有

(2)日常生活中常用到苏打和小苏打,鉴别它们的方法有多种。例如:
方法①:如图所示装置,这是根据它们具有不同的

方法②:取等物质的量的苏打和小苏打分别于试管中,再分别加入足量盐酸充分反应,比较现象得出先出现气泡者为
(3)测定Na2CO3(含氯化钠杂质)样品中Na2CO3的质量分数:①称取m g样品放入烧杯内加水溶解;②加入过量的氯化钙溶液充分反应;③过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如下图所示(反应条件和部分产物已略去)。
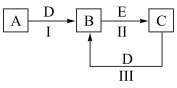
(1)若气体A的水溶液呈碱性,气体B在空气中会变为红棕色,反应II的其中一种产物能引起温室效应。
①A的电子式为___________ 。
②反应I的化学方程式是___________ 。反应II的化学方程式是___________ 。
(2)若A是常用于呼吸面具中的淡黄色固体,D是常见的温室气体,C中的阴、阳离子均为10电子微粒。
①A中阳离子与阴离子的个数比是___________ ;C中所含化学键的类型是___________ 。
②若工业上用E制作漂白粉,写出反应II的离子方程式:___________ 。

(1)若气体A的水溶液呈碱性,气体B在空气中会变为红棕色,反应II的其中一种产物能引起温室效应。
①A的电子式为
②反应I的化学方程式是
(2)若A是常用于呼吸面具中的淡黄色固体,D是常见的温室气体,C中的阴、阳离子均为10电子微粒。
①A中阳离子与阴离子的个数比是
②若工业上用E制作漂白粉,写出反应II的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。完成下列填空:
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出M原子核外能量最高的电子的电子排布式:___________ 。
②常温下,不能与R单质发生反应的是_______ (选填序号)。
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高。可由下列反应制得:SiO2+C+N2 Si3N4+CO
Si3N4+CO
①Si3N4中氮元素的化合价为-3,请解释Si3N4中氮元素化合价为负价的原因__________________ 。
②C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:______________________ 。
③配平上述反应的化学方程式,并标出电子转移的数目和方向。_______________ 。
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:
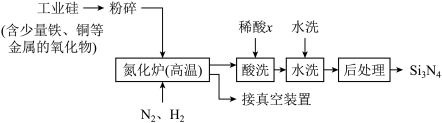
①将工业硅粉碎的目的是______________________________ 。
②适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。 可能是
可能是______ (选填:“盐酸”“硝酸”或“硫酸”),理由是_____________________ 。
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出M原子核外能量最高的电子的电子排布式:
②常温下,不能与R单质发生反应的是
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高。可由下列反应制得:SiO2+C+N2
 Si3N4+CO
Si3N4+CO①Si3N4中氮元素的化合价为-3,请解释Si3N4中氮元素化合价为负价的原因
②C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:
③配平上述反应的化学方程式,并标出电子转移的数目和方向。
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:

①将工业硅粉碎的目的是
②适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。
 可能是
可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按照如图的生产流程可以制得氧化铁(铁红颜料)和硫酸钾。
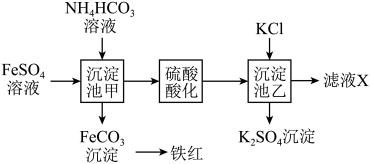
(1)沉淀池甲中反应后生成碳酸亚铁、硫酸铵水和一种温室气体,写出该反应的化学方程式_______ 。
(2)该流程中加硫酸酸化的目的是____________ 。
(3)在沉淀池乙中还要加入有机溶剂丙醇,其原因可能是___________________ 。

(1)沉淀池甲中反应后生成碳酸亚铁、硫酸铵水和一种温室气体,写出该反应的化学方程式
(2)该流程中加硫酸酸化的目的是
(3)在沉淀池乙中还要加入有机溶剂丙醇,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液)。
根据该表回答问题:
(1)第Ⅲ组中有一种物质能与第________ 组中的所有物质反应,这种物质是________ 。
(2)不跟第Ⅰ组中所有物质发生反应的是第________ 组物质中的________ 且能与第Ⅲ组中所有物质发生反应,其化学方程式分别为___________ 、____________ 、___________ 。
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | Fe | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Mg | NaOH | MgCl2 |
根据该表回答问题:
(1)第Ⅲ组中有一种物质能与第
(2)不跟第Ⅰ组中所有物质发生反应的是第
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组的同学欲除去固体氯化钠中混有的氯化钙,请据如下实验方案回答问题。
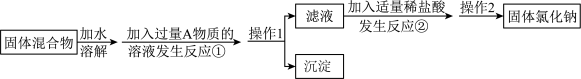
(1)操作1的名称是_________ ;
(2)反应①中加入略过量的A物质的目的是_________________________ ;判断A已过量的实验操作方法是________________________ 。
(3)写出反应②的化学方程式:______________________________ 。如果加入盐酸过量,则对所得到的氯化钠的纯度_________ (填“有”或“没有”)影响。
(4)实验时称取样品的质量为185.0g,经过操作1后,测得沉淀(不溶于水)的质量为50.0g,则样品中NaCl的质量分数是_________ 。

(1)操作1的名称是
(2)反应①中加入略过量的A物质的目的是
(3)写出反应②的化学方程式:
(4)实验时称取样品的质量为185.0g,经过操作1后,测得沉淀(不溶于水)的质量为50.0g,则样品中NaCl的质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】水是生命之源,它与我们的生活密切相关。
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理_____________________________________________________________ 。
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:__________________________________________ 。
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为______________ g。
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。
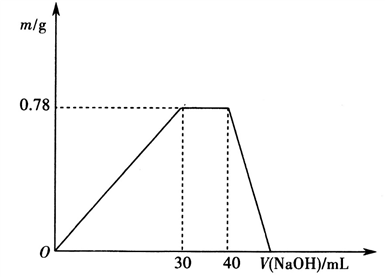
根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有_________________ (写离子符号)。
②c(NaOH)=_____________________ 。
③NO3-是否存在?_______ (填“存在”、“不存在”或“不确定”),理由是_____________________________________________________
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。

根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有
②c(NaOH)=
③NO3-是否存在?
您最近一年使用:0次


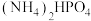 ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备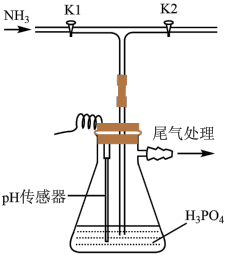
 的作用为
的作用为 ,打开
,打开

