水是生命之源,它与我们的生活密切相关。
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理_____________________________________________________________ 。
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:__________________________________________ 。
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为______________ g。
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。
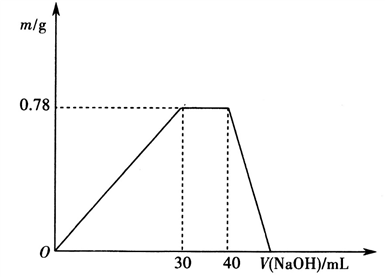
根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有_________________ (写离子符号)。
②c(NaOH)=_____________________ 。
③NO3-是否存在?_______ (填“存在”、“不存在”或“不确定”),理由是_____________________________________________________
(1)自来水厂常用高铁酸钾(K2FeO4)改善水质。简述高铁酸钾用于杀菌消毒同时又起到净水作用的原理
(2)电镀废水中含有剧毒的NaCN,加入NaClO处理该碱性废水时生成Na2CO3、NaCl和N2。
①写出该反应的离子方程式:
②处理a m3含NaCN bmg·L-1的废水,至少需要NaClO的质量为
(3)某工业废水中可能含有Na+、Mg2+、A13+、Fe3+、NH4+、CO32-、SO42-、NO3-中的几种,为确定其成分,设计如下实验:
a.取该废水进行焰色反应实验,火焰为黄色;
b.另取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到4.66g白色沉淀;
c.另取10mL该废水于试管中,滴加NaOH溶液,产生沉淀的质量随所加NaOH溶液体积的变化关系如下图所示(不考虑沉淀的溶解和损失)。

根据上述实验和图表数据回答:
①该工业废水中一定不存在的离子有
②c(NaOH)=
③NO3-是否存在?
更新时间:2017-11-24 20:12:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)在由水电离产生的H+的浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是________ 。
①K+、Cl-、NO 、S2- ②K+、Fe2+、I-、SO
、S2- ②K+、Fe2+、I-、SO ③Na+、Cl-、NO
③Na+、Cl-、NO 、SO
、SO
④Na+、Cu2+、Cl-、HCO ⑤K+、Ba2+、Cl-、NO
⑤K+、Ba2+、Cl-、NO
(2)不能影响水的电离平衡的操作是________。
(1)在由水电离产生的H+的浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO
 、S2- ②K+、Fe2+、I-、SO
、S2- ②K+、Fe2+、I-、SO ③Na+、Cl-、NO
③Na+、Cl-、NO 、SO
、SO
④Na+、Cu2+、Cl-、HCO
 ⑤K+、Ba2+、Cl-、NO
⑤K+、Ba2+、Cl-、NO
(2)不能影响水的电离平衡的操作是________。
| A.向水中投入一小块金属钠 |
| B.将水加热煮沸 |
| C.向水中通入CO2气体 |
| D.向水中加食盐晶体 |
您最近一年使用:0次
【推荐2】150mL某无色溶液中可能含有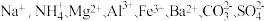 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:
①向第一份中加入足量的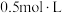 -1稀盐酸,生成0.448L气体(已换算成标准状况下);
-1稀盐酸,生成0.448L气体(已换算成标准状况下);
②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl2溶液,得到沉淀6.27g,加入足量(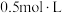 -1稀盐酸充分反应后,剩余沉淀2.33g。
-1稀盐酸充分反应后,剩余沉淀2.33g。
根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取_______ mL浓盐酸,若在量取浓盐酸时俯视刻度线,则会导致配制的稀盐酸的浓度_______ (填“偏高”、“偏低”或“不变”)。
(2)实验②中生成气体的离子方程式为_______ 。
(3)实验③中沉淀部分溶解的化学方程式为_______ ,剩余沉淀的化学式为_______ 。
(4)原溶液中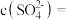
_______ 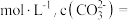
_______ 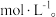
(5)经分析,溶液中一定存在Na+,理由是_______ 。
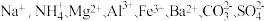 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:①向第一份中加入足量的
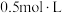 -1稀盐酸,生成0.448L气体(已换算成标准状况下);
-1稀盐酸,生成0.448L气体(已换算成标准状况下);②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl2溶液,得到沉淀6.27g,加入足量(
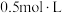 -1稀盐酸充分反应后,剩余沉淀2.33g。
-1稀盐酸充分反应后,剩余沉淀2.33g。根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取
(2)实验②中生成气体的离子方程式为
(3)实验③中沉淀部分溶解的化学方程式为
(4)原溶液中
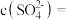
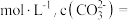
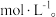
(5)经分析,溶液中一定存在Na+,理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO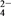 、CO
、CO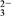 ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色
②D的焰色反应呈黄色
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀
请回答下列问题:
(1)五种盐中,一定没有的阳离子是________ ;
(2)这五种盐分别是(写分子式)
A_________________ B________________ C_________________
D_________________ E________________
(3)若要检验B中所含的阳离子,正确的实验方法是_________________________________
 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO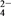 、CO
、CO ,已知:
,已知:①五种盐均溶于水,水溶液均为无色
②D的焰色反应呈黄色
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀
请回答下列问题:
(1)五种盐中,一定没有的阳离子是
(2)这五种盐分别是(写分子式)
A
D
(3)若要检验B中所含的阳离子,正确的实验方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.在含有146gHCl和120gMgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生的沉淀质量(g)与加入Ba(OH)2的质量(g)之间的关系如图所示,回答下列问题:
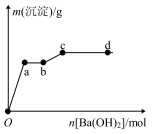
(1)Oa段生成的沉淀为___________ (填化学式)。
(2)写出ab段发生反应的离子方程式___________ 。
(3)bc段,沉淀质量继续增加,请用离子方程式解释原因___________ 。
(4)写出c点溶液中溶质的化学式___________ 。
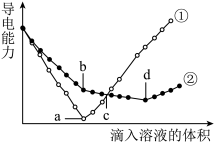
(5)在两份相同的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是

(1)Oa段生成的沉淀为
(2)写出ab段发生反应的离子方程式
(3)bc段,沉淀质量继续增加,请用离子方程式解释原因
(4)写出c点溶液中溶质的化学式
(5)在两份相同的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是

A.b点溶液大量存在的离子是Na+、OH-、 |
| B.bd段发生的离子方程式OH-+H+ =H2O |
| C.c点,两溶液中含有相同量的OH- |
| D.a、d两点对应的溶液均显中性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、Al3+、NH4+、Cl-、CO32-和SO42-。现每次取100.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.896L(标准状况下)
②第三份加入足量BaCl2溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。
请回答:
(1)c(CO32-)=______ 。
(2)K+是否存在?_________ ;若存在,浓度范围是___________ (若不存在,则不必回答第2问)。
(3)根据以上实验,不能判断哪种离子是否存在?若存在,这种离子如何进行检验?______ 。
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.896L(标准状况下)
②第三份加入足量BaCl2溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。
请回答:
(1)c(CO32-)=
(2)K+是否存在?
(3)根据以上实验,不能判断哪种离子是否存在?若存在,这种离子如何进行检验?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组对NaHSO4的性质进行了如下探究。
(1)下列关于NaHSO4的说法中正确的是___________。
(2)取少量的NaHSO4溶液,滴加2-3滴石蕊试液,现象是___________ 。
(3)向NaHSO4溶液中滴加NaHCO3溶液,反应的离子方程式为___________ 。在两份相同的Ba(OH)2溶液中,分别滴入相同浓度的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
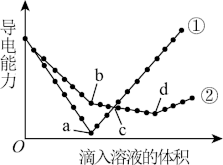
(4)图中①代表滴加___________ (填化学式)溶液的曲线,导电能力变化的原因是___________ 。
(5)b点溶液中大量存在的离子是___________ 。
(6)___________ 点对应的溶液呈中性(填a、b、c、d,下同);___________ 点对应的溶液中Ba2+恰好沉淀完全。
(7)写出bd段发生的离子方程式___________ 。
(1)下列关于NaHSO4的说法中正确的是___________。
| A.因为NaHSO4是离子化合物,所以NaHSO4固体能够导电 |
| B.NaHSO4固体中正离子和负离子的个数比是2∶1 |
| C.NaHSO4固体熔化时破坏的是离子键和共价键 |
| D.NaHSO4固体溶于水时破坏的是离子键和共价键 |
(3)向NaHSO4溶液中滴加NaHCO3溶液,反应的离子方程式为

(4)图中①代表滴加
(5)b点溶液中大量存在的离子是
(6)
(7)写出bd段发生的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。完成下列填空:
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:___________________________ 。
(2)上述反应中,氧化剂是_____________ ,每转移1 mol电子,生成Cl2_____ L(标准状况)。
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:_________________ 。
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序__________ 。
(5)上述氧化还原反应体系中,属于第三周期元素的简单离子半径由大到小的顺序为________
(6)氯原子的最外层电子的轨道式为___________ ,氯原子核外有_______ 不同运动状态的电子。
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:
(2)上述反应中,氧化剂是
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序
(5)上述氧化还原反应体系中,属于第三周期元素的简单离子半径由大到小的顺序为
(6)氯原子的最外层电子的轨道式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氨氮废水中的氮元素多以 、
、 的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
(1)某研究团队设计的处理流程如下:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。
请用离子方程式表示加NaOH溶液时所发生的反应:_______ 。
②过程Ⅱ:在微生物的作用下实现 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为_______ 。
③过程Ⅲ:在一定条件下向废水中加入甲醇( ),实现
),实现 转化,称为反硝化过程。
转化,称为反硝化过程。 中碳元素的化合价为
中碳元素的化合价为_______ ,当甲醇与6mol  完全反应,转化成
完全反应,转化成 时,消耗的甲醇的质量为
时,消耗的甲醇的质量为_______ 。
(2)折点氯化法是将氯气通入氨氮废水中达到某一点,在该点时水中游离氯含量最低,而氨氮的浓度降为零,该点称为折点,该状态下的氯化称为折点氯化。当氯气与氨氮的物质的量之比至少为_______ 时即“折点”。
 、
、 的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。(1)某研究团队设计的处理流程如下:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。
请用离子方程式表示加NaOH溶液时所发生的反应:
②过程Ⅱ:在微生物的作用下实现
 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为③过程Ⅲ:在一定条件下向废水中加入甲醇(
 ),实现
),实现 转化,称为反硝化过程。
转化,称为反硝化过程。 中碳元素的化合价为
中碳元素的化合价为 完全反应,转化成
完全反应,转化成 时,消耗的甲醇的质量为
时,消耗的甲醇的质量为(2)折点氯化法是将氯气通入氨氮废水中达到某一点,在该点时水中游离氯含量最低,而氨氮的浓度降为零,该点称为折点,该状态下的氯化称为折点氯化。当氯气与氨氮的物质的量之比至少为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组利用以下装置探究氯气与氨气之间的反应。其中装置A、F分别为氨气和氯气的发生装置,装置C为纯净、干燥的氯气与氨气发生反应的装置。回答下列问题:
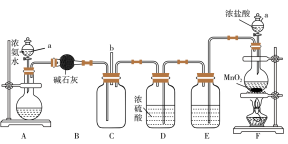
(1)装置F中的圆底烧瓶加热时要垫___________ 。装置A的圆底烧瓶中盛放的固体物质可选用___________ (填字母)。
a.氯化钠 b.氢氧化钠 c.碳酸钙
(2)装置B、D的作用均为___________ 。从装置C的b处逸出的尾气中含有少量 ,为防止其污染环境,可将尾气通过盛有
,为防止其污染环境,可将尾气通过盛有___________ 溶液的洗气瓶。
(3)装置F的圆底烧瓶中发生反应的离子方程式为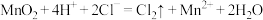 ,在这个反应中氧化剂与还原剂的物质的量之比
,在这个反应中氧化剂与还原剂的物质的量之比___________ ,还原产物与氧化产物的物质的量之比___________ 。装置E的作用是除去 中的HCl,洗气瓶中盛放的试剂为
中的HCl,洗气瓶中盛放的试剂为___________ 。
(4)写出足量铜和稀硝酸反应方程式:___________ ,该反应中表现酸性的硝酸与做氧化剂的硝酸物质的量之比为___________ 。

(1)装置F中的圆底烧瓶加热时要垫
a.氯化钠 b.氢氧化钠 c.碳酸钙
(2)装置B、D的作用均为
 ,为防止其污染环境,可将尾气通过盛有
,为防止其污染环境,可将尾气通过盛有(3)装置F的圆底烧瓶中发生反应的离子方程式为
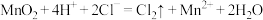 ,在这个反应中氧化剂与还原剂的物质的量之比
,在这个反应中氧化剂与还原剂的物质的量之比 中的HCl,洗气瓶中盛放的试剂为
中的HCl,洗气瓶中盛放的试剂为(4)写出足量铜和稀硝酸反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】三水乳酸亚铁晶体[(CH3CHOHCOO)2Fe•3H2O,Mr=288]是一种很好的补铁剂,易溶于水,吸收效果比无机铁好。可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是______ (填字母),原因是_______________________ 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是__________________ 。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是_____________________ 。
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是______________________________________ 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是_______________ 。
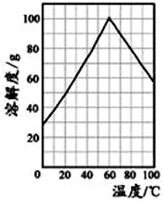
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液____________ ,得到FeSO4·7H2O晶体。
(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是____________________ 。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol•L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)219.7mL。滴定反应为Ce4++Fe2+═Ce3++Fe3+,则产品中乳酸亚铁晶体的质量分数为__________ 。
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液

(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是
您最近一年使用:0次
【推荐2】烧杯中盛有CuCl2和HCl的混合溶液100 g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。

(1)写出bc段的化学方程式___________ 。
(2)求c点溶质的质量分数___________ ? (保留小数点后一位)。

(1)写出bc段的化学方程式
(2)求c点溶质的质量分数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学在生产生活中都具有重要的作用和意义。
(1)图1为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图,该电池的负极反应式为_________ 。


(2)制备焦亚硫酸钠(Na2S2O5)可采用三室膜电解技术,装置如图2所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为_______ 。电解后,____ 室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。
(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
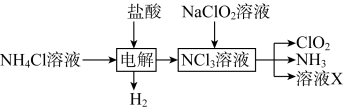
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2,电解时发生反应的化学方程式为________________ 。溶液X中大量存在的阴离子有________________ 。
(4)测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸。将一定量的混合气体通入混合溶液中充分吸收。
Ⅱ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),以淀粉溶液为指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。
①锥形瓶内ClO2与碘化钾反应的离子方程式为__________________ 。
②测得混合气中ClO2的质量为______ 。
③测定混合气中ClO2的含量的操作中可能使测定结果偏低的是____ (填字母)。
a.滴定管未润洗就直接注入硫代硫酸钠标准液
b.滴定管读取标准液体积时,开始仰视读数,滴定结束时俯视读数
c.锥形瓶用蒸馏水洗净后没有干燥
(1)图1为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图,该电池的负极反应式为


(2)制备焦亚硫酸钠(Na2S2O5)可采用三室膜电解技术,装置如图2所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为
(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2,电解时发生反应的化学方程式为

(4)测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸。将一定量的混合气体通入混合溶液中充分吸收。
Ⅱ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),以淀粉溶液为指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。
①锥形瓶内ClO2与碘化钾反应的离子方程式为
②测得混合气中ClO2的质量为
③测定混合气中ClO2的含量的操作中可能使测定结果偏低的是
a.滴定管未润洗就直接注入硫代硫酸钠标准液
b.滴定管读取标准液体积时,开始仰视读数,滴定结束时俯视读数
c.锥形瓶用蒸馏水洗净后没有干燥
您最近一年使用:0次



