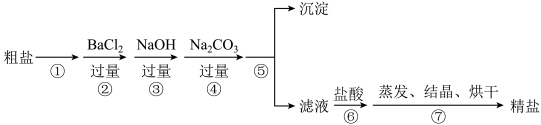
通过海水晾晒可以得到粗盐,粗盐除含有NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,下图是粗盐提纯的实验流程(每次所加的试剂均过量)。
下列说法不正确的是

下列说法不正确的是
| A.步骤①和⑤的操作分别是溶解、过滤 |
| B.步骤③中试剂NaOH不能换成KOH |
| C.步骤④可以与步骤②互换顺序 |
| D.步骤⑥加盐酸时需用pH试纸测定溶液呈中性或微酸性 |
更新时间:2023-10-07 11:43:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某工业废水中存在大量的Na+、Cl-、Cu2+、SO ,欲除去其中的Cu2+、SO
,欲除去其中的Cu2+、SO (为使离子完全沉淀,沉淀剂需要过量),设计工艺流程如图所示:
(为使离子完全沉淀,沉淀剂需要过量),设计工艺流程如图所示:
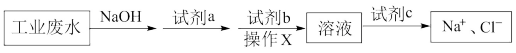
下列说法不正确 的是( )
 ,欲除去其中的Cu2+、SO
,欲除去其中的Cu2+、SO (为使离子完全沉淀,沉淀剂需要过量),设计工艺流程如图所示:
(为使离子完全沉淀,沉淀剂需要过量),设计工艺流程如图所示: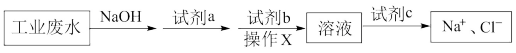
下列说法
| A.NaOH的作用是除去Cu2+ | B.试剂a为Na2CO3,试剂b为BaCl2 |
| C.流程图中,操作x为过滤 | D.试剂c为盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有 、
、 、
、 和
和 杂质。粗盐制得精盐的过程如下:
杂质。粗盐制得精盐的过程如下:
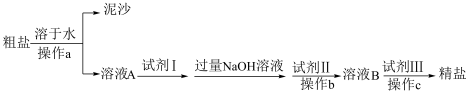
下列说法错误的是
 、
、 、
、 和
和 杂质。粗盐制得精盐的过程如下:
杂质。粗盐制得精盐的过程如下:
下列说法错误的是
A.试剂I是足量 溶液 溶液 |
| B.操作a所需的玻璃仪器有烧杯,漏斗、玻璃棒 |
C.试剂Ⅱ为碳酸钠,其作用为除去溶液中的 和过量的试剂I 和过量的试剂I |
| D.用pH试纸检验溶液B,可发现溶液B显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作正确的是
| A.用酒精萃取碘水中的碘 |
| B.蒸馏时,应将温度计水银球浸入液体中 |
| C.蒸发时,不可将溶液蒸干,当蒸发皿中出现较多固体时,停止加热,利用余热将液体蒸干 |
| D.用分液漏斗分离植物油和水,植物油应用烧杯在分液漏斗下口接 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下表中的实验操作不能 达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别苯和甲苯 | 分别加入酸性高锰酸钾溶液,观察颜色变化 |
| B | 检验溴乙烷中的溴元素 | 将溴乙烷与 溶液混合加热,静置,待溶液分层后,取上层清液用稀硝酸酸化,再加入 溶液混合加热,静置,待溶液分层后,取上层清液用稀硝酸酸化,再加入 溶液 溶液 |
| C | 分离甲醇(沸点65℃)、正丙醇(沸点97℃) | 将混合溶液放入蒸馏烧瓶进行加热,分别收集相应的馏分 |
| D | 比较乙酸、碳酸、苯酚的酸性强弱 | 向碳酸钠固体中加入乙酸,将产生的气体通入苯酚钠溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确 的是
| A.除去氯化钾中少量硝酸钾可用蒸发结晶、趁热过滤的方法 |
| B.摩尔盐晶体表面附着的水分可用少量酒精洗去 |
| C.在燃煤中添加适量石灰石可降低酸雨的危害 |
| D.潮湿的环境下合金都易发生电化学腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图是工业利用菱镁矿 (含杂质
(含杂质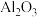 、
、 )制取镁的工艺流程。
)制取镁的工艺流程。

下列有关说法正确的是
 (含杂质
(含杂质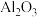 、
、 )制取镁的工艺流程。
)制取镁的工艺流程。
下列有关说法正确的是
A.沉淀混合物为 和 和 |
| B.酸浸池中也可改用稀硫酸浸取 |
C.实验室将 溶液加热浓缩、冷却结晶、过滤、洗涤、干燥可得 溶液加热浓缩、冷却结晶、过滤、洗涤、干燥可得 晶体 晶体 |
| D.工业上常采用电解法在阴极上制取镁,为保护镁,电解时应该在无水无氧环境下进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】为提纯含少量正丁醛杂质的1-丁醇粗品,某研究小组设计如下路线:

已知:①R-CHO + NaHSO3(饱和)→ RCH(OH)SO3Na↓
②乙醚沸点为34 ℃,密度为0.714 g/cm3;1-丁醇沸点为118 ℃
下列说法正确的是

已知:①R-CHO + NaHSO3(饱和)→ RCH(OH)SO3Na↓
②乙醚沸点为34 ℃,密度为0.714 g/cm3;1-丁醇沸点为118 ℃
下列说法正确的是
| A.操作1用到的玻璃仪器有烧杯、漏斗和玻璃棒 |
| B.操作2中,乙醚可以用乙醇代替 |
| C.操作2分液时,有机层从分液漏斗下口放出 |
| D.操作3是蒸馏,蒸馏温度要求略高于118 ℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在实验室粗盐的提纯实验中,玻璃棒的使用不具有的作用是
| A.在溶解过程中搅拌 | B.在蒸发过程中搅拌 |
| C.在过滤时引流 | D.使固体析出 |
您最近一年使用:0次

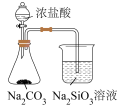

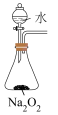
 溶液便可鉴别亚硝酸钠和食盐
溶液便可鉴别亚硝酸钠和食盐 沸点为
沸点为 和甲苯
和甲苯 沸点为
沸点为 的混合物
的混合物

