某教授团队设计了具有Se空位的Ni3Se4电极,由此设计的某种电解池如图,在M电极可收集到NH3和少量H2,下列说法中错误的是


| A.N电极为阳极,发生氧化反应 |
B.M电极上的电极反应之一为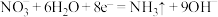 |
| C.若以铅蓄电池为电源,则M电极与Pb电极相连 |
| D.当电路中有0.4mol电子通过时,则生成的NH3在标准状况下的体积为1.12L |
更新时间:2023-09-09 22:05:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某工厂采用如图装置处理化石燃料开采、加工过程产生的H2S废气,已知电解池中的两个电极均为惰性电极。下列说法不正确的是( )


| A.电极 a 为阳极 |
| B.若交换膜为阳离子交换膜,b 电极区会产生红褐色沉淀 |
| C.反应池中处理H2S的反应是H2S +2Fe3+ = 2Fe2+ +S↓+2H+ |
| D.若交换膜为质子交换膜,则NaOH溶液的浓度逐渐变大,需要定期更换 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
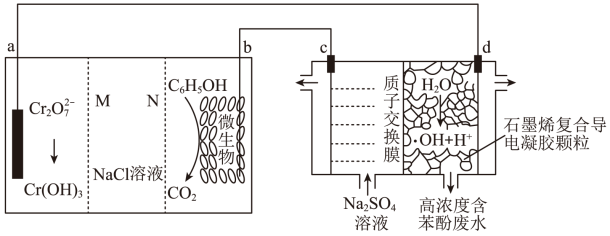
【推荐2】我国科学家设计了一种利用废水中的 将苯酚氧化为
将苯酚氧化为 和
和 的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基(
的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基( )的氧化性仅次于氟气。下列说法正确的是
)的氧化性仅次于氟气。下列说法正确的是
 将苯酚氧化为
将苯酚氧化为 和
和 的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基(
的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基( )的氧化性仅次于氟气。下列说法正确的是
)的氧化性仅次于氟气。下列说法正确的是
| A.电子转移方向:c电极→导线→b电极 |
B.d电极的电极反应为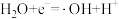 |
C.右侧装置中,c、d两电极产生气体的体积比(相同条件下)为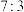 |
D.若a电极上有 参与反应,理论上 参与反应,理论上 溶液中有 溶液中有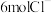 通过阴离子膜进入a电极区溶液 通过阴离子膜进入a电极区溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中。下列分析正确的是


| A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B.K1闭合,石墨棒周围溶液pH逐渐升高 |
| C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D.K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由相同金属电极及其不同浓度的盐溶液组成的电池称为浓差电池,电子由溶液浓度较小的一极流向浓度较大的一极。如图所示装置中,X电极与Y电极初始质量相等。进行实验时,先闭合K2,断开K1,一段时间后,再断开K2,闭合K1,即可形成浓差电池,电流计指针偏转。下列不正确的是


| A.充电前,该电池两电极不存在电势差 |
| B.放电时,右池中的NO3-通过离子交换膜移向左池 |
| C.充电时,当外电路通过0.1 mol电子时,两电极的质量差为10.8 g |
| D.放电时,电极Y为电池的正极 |
您最近一年使用:0次
【推荐1】一种脱除和利用水煤气中CO2方法的如图,下列说法中错误的是


| A.b为电源的正极 |
| B.利用电化学原理,将CO2电催化为C2H4的反应式为2CO2-12e-+12H+=C2H4+4H2O |
C.再生塔中产生CO2的离子方程式为2  H2O+CO2↑+ H2O+CO2↑+ |
D.某温度下,吸收塔中K2CO3溶液吸收一定量的CO2后,c( ):c( ):c( )=1:2,则该溶液的pH=10(该温度下H2CO3的Ka1=4.6×10-7;Ka2=5.0×10-11) )=1:2,则该溶液的pH=10(该温度下H2CO3的Ka1=4.6×10-7;Ka2=5.0×10-11) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式书写正确的是( )
| A.碘化亚铁中通入过量氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| B.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓ |
| C.1mol•L﹣1的NaAlO2溶液和2.5mol•L﹣1的HCl溶液等体积互相均匀混合:2AlO2﹣+5H+=Al3++Al(OH)3↓+H2O |
D.用铜作电极电解CuSO4溶液:2Cu2++2H2O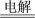 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
您最近一年使用:0次
【推荐1】如图装置,常温下,溶液足量,体积均为100 mL且电解前后溶液的体积变化忽略不计,Ⅰ中溶液为KCl溶液、Ⅱ中溶液为NaNO3溶液、Ⅲ中溶液为CuSO4溶液,当电解一段时间,当某极析出0.32 g Cu时,则Ⅰ、Ⅱ、Ⅲ中溶液pH分别为


| A.12、7、2 | B.1、7、13 | C.13、7、1 | D.7、13、1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】1,5—戊二胺( )是生物法制备尼龙材料的重要原料,利用双极膜(BPM)电渗析产碱技术可将生物发酵液中的1,5—戊二胺硫酸盐(含
)是生物法制备尼龙材料的重要原料,利用双极膜(BPM)电渗析产碱技术可将生物发酵液中的1,5—戊二胺硫酸盐(含 和SO
和SO )转换为1,5—戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是
)转换为1,5—戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是

 )是生物法制备尼龙材料的重要原料,利用双极膜(BPM)电渗析产碱技术可将生物发酵液中的1,5—戊二胺硫酸盐(含
)是生物法制备尼龙材料的重要原料,利用双极膜(BPM)电渗析产碱技术可将生物发酵液中的1,5—戊二胺硫酸盐(含 和SO
和SO )转换为1,5—戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是
)转换为1,5—戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是
| A.a极的电势比b极的低 |
| B.m膜为阳离子交换膜,n膜为阴离子交换膜 |
| C.电解过程中,H2SO4极室溶液的pH逐渐减小 |
| D.b极区每生成11.2L气体(标准状况),理论上可生成2mol1,5—戊二胺 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】氨是非常重要的工业原料,中国合成氨产量位居世界第一位。有人提出常压下以电解法合成氨,装置如图所示,以熔融的NaOH—KOH为电解液,纳米Fe2O3起催化作用,在发生反应时生成中间体Fe。下列说法正确的是


| A.电源b端为负极,惰性电极Ⅱ上发生还原反应 |
| B.生成3.4克NH3理论上放出O2为3.36L |
| C.惰性电极I上发生反应:Fe2O3+3H2O-6e-=2Fe+6OH- |
| D.生成氨气的反应:2Fe+N2+3H2O=Fe2O3+2NH3 |
您最近一年使用:0次

 )吸收一定量
)吸收一定量 气体后,可通过如图装置实现再生。下列说法正确的是
气体后,可通过如图装置实现再生。下列说法正确的是
 大于进液
大于进液 的
的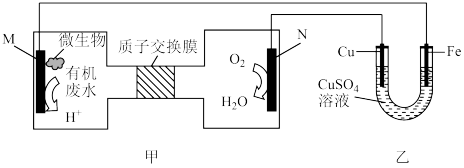
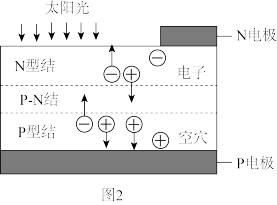
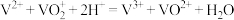 ;图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法正确的是
;图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法正确的是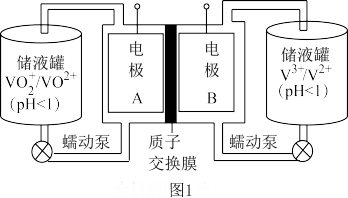
 接太阳能电池的
接太阳能电池的 电极,电极
电极,电极 接
接 电极
电极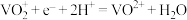
 时,必有
时,必有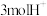 由右侧向左侧迁移
由右侧向左侧迁移

