已知 ,如图是
,如图是 燃烧的反应过程中能量变化示意图。
燃烧的反应过程中能量变化示意图。

从能量变化角度,该反应属于的反应类型是______ 。
A.吸热反应 B.放热反应
 ,如图是
,如图是 燃烧的反应过程中能量变化示意图。
燃烧的反应过程中能量变化示意图。
从能量变化角度,该反应属于的反应类型是
A.吸热反应 B.放热反应
更新时间:2023/10/09 10:26:07
|
相似题推荐
【推荐1】已知某反应A(g)+B(g)⇌C(g)+D(g),反应过程中的能量变化如图所示。
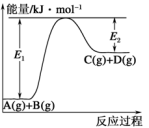
该反应是_______ 反应(填“吸热”或“放热”),该反应的ΔH=_______ kJ·mol-1(用含E1、E2的代数式表示),1mol气体A和1mol气体B具有的总能量比1mol气体C和1mol气体D具有的总能量_______ (填“高”、“低”或“高低不一定”)。

该反应是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】从能量的角度看,断开化学键要__________ ,形成化学键要_______ 。化学反应是释放能量还是吸收能量取决于__________ ,当反应物的总能量高于生成物时,该反应为_____ 反应;当反应物的总能量低于生成物时,该反应为_______ 反应。
您最近半年使用:0次
【推荐3】燃料和能源是化学知识与社会生活联系极为密切的内容,我们要关注矿物能源的合理利用,积极研究、开发新能源。
(1)新能源应该具有原材料易得、燃烧时产生的热量多且不会污染环境的特点,在煤炭、石油、煤气、氢气中,前途广阔的能源是_____ 。
(2)近年来,我国煤矿事故大多是瓦斯爆炸所致。瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸。为避免灾难的发生应采取的切实可行的措施有_____ (填序号)。
①加强安全管理,杜绝明火源 ②降低瓦斯气体的着火点 ③提高通风能力 ④将矿井中的氧气抽去
(3)水煤气的主要成分是一氧化碳和氢气,它是由煤炭和水蒸气反应制得的,已知C(石墨)、CO、H2燃烧的热化学方程式为:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
请回答下列问题:
①根据上述提供的热化学方程式计算,36g水由液态变成气态的热量变化是_____ (填“吸收”或“放出”)_____ 热量。
②写出C(石墨,s)与水蒸气反应生成一氧化碳和氢气的热化学方程式:_____ 。
③作为燃料,水煤气和煤相比有什么优点_____ (任答一点)。
(1)新能源应该具有原材料易得、燃烧时产生的热量多且不会污染环境的特点,在煤炭、石油、煤气、氢气中,前途广阔的能源是
(2)近年来,我国煤矿事故大多是瓦斯爆炸所致。瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸。为避免灾难的发生应采取的切实可行的措施有
①加强安全管理,杜绝明火源 ②降低瓦斯气体的着火点 ③提高通风能力 ④将矿井中的氧气抽去
(3)水煤气的主要成分是一氧化碳和氢气,它是由煤炭和水蒸气反应制得的,已知C(石墨)、CO、H2燃烧的热化学方程式为:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
H2(g)+
 O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH2=-241.8kJ·mol-1CO(g)+
 O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH3=-283.0kJ·mol-1H2(g)+
 O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH4=-285.8kJ·mol-1请回答下列问题:
①根据上述提供的热化学方程式计算,36g水由液态变成气态的热量变化是
②写出C(石墨,s)与水蒸气反应生成一氧化碳和氢气的热化学方程式:
③作为燃料,水煤气和煤相比有什么优点
您最近半年使用:0次



