在N2气氛中,FeSO4·7H2O的脱水热分解过程如图所示:
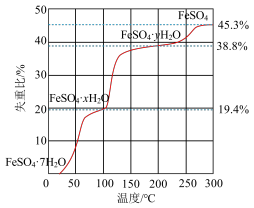
根据上述实验结果,可知
___________ ,
___________ 。

根据上述实验结果,可知


2023高三·全国·专题练习 查看更多[1]
(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2023-11-05 15:08:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】月球含有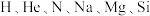 等元素,是人类未来的资源宝库。
等元素,是人类未来的资源宝库。
(1)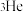 是高效核能原料,其原子核内中子数为
是高效核能原料,其原子核内中子数为_______ 。
(2) 的原子结构示意图为
的原子结构示意图为_______ , 在氧气中完全燃烧所得产物的电子式为
在氧气中完全燃烧所得产物的电子式为_______ 。
(3) 在工业上应用广泛,可由
在工业上应用广泛,可由 制备。
制备。
①月球上某矿石经处理得到的 中含有少量
中含有少量 ,除去
,除去 的离子方程式为
的离子方程式为_______ 。
② 与炭粉和氯气在一定条件下反应可制备
与炭粉和氯气在一定条件下反应可制备 。若尾气可用足量
。若尾气可用足量 溶液完全吸收,则生成的盐为
溶液完全吸收,则生成的盐为_______ (写化学式)。
(4)月球土壤中含有丰富的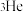 ,从月球土壤中提炼
,从月球土壤中提炼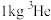 ,同时可得
,同时可得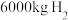 和
和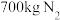 。以所得
。以所得 和
和 为原料经一系列反应最多可生产碳酸氢铵
为原料经一系列反应最多可生产碳酸氢铵_______  。
。
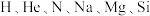 等元素,是人类未来的资源宝库。
等元素,是人类未来的资源宝库。(1)
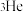 是高效核能原料,其原子核内中子数为
是高效核能原料,其原子核内中子数为(2)
 的原子结构示意图为
的原子结构示意图为 在氧气中完全燃烧所得产物的电子式为
在氧气中完全燃烧所得产物的电子式为(3)
 在工业上应用广泛,可由
在工业上应用广泛,可由 制备。
制备。①月球上某矿石经处理得到的
 中含有少量
中含有少量 ,除去
,除去 的离子方程式为
的离子方程式为②
 与炭粉和氯气在一定条件下反应可制备
与炭粉和氯气在一定条件下反应可制备 。若尾气可用足量
。若尾气可用足量 溶液完全吸收,则生成的盐为
溶液完全吸收,则生成的盐为(4)月球土壤中含有丰富的
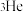 ,从月球土壤中提炼
,从月球土壤中提炼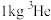 ,同时可得
,同时可得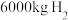 和
和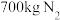 。以所得
。以所得 和
和 为原料经一系列反应最多可生产碳酸氢铵
为原料经一系列反应最多可生产碳酸氢铵 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】
(1)5 mol H2O的质量为______ ,其中含有______ 个水分子,氢原子的物质的量为______ 。
(2)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是______ ,在相同温度和相同压强条件下,体积最大的是______ 。
(1)5 mol H2O的质量为
(2)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列填空:
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______ 。
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是_______ ,密度之比为_______ ,质量之比为_______ 。
(4)写出实验室制氯气的化学方程式_______ ,在此过程中呈酸性的HCl与参加反应的总HCl的质量之比为_______ ,每产生1mol氯气转移电子数为 _______ 。
(5)配平化学方程式:_______ 。
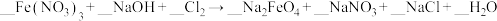
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为
(2)相同质量的CO和CO2,它们所含的原子数之比为
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是
(4)写出实验室制氯气的化学方程式
(5)配平化学方程式:
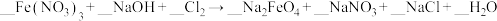
您最近一年使用:0次
【推荐1】生活污水中氮是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180mg/L。
(1)写出NH4Cl电子式:___ 。
(2)氮原子的电子排布式是:___ ,写出与氯同周期,有2个未成对电子的原子的元素符号为___ 、___ 。
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为___ L(计算结果保留两位小数)。
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目___ 。
___ Fe+___ NO3-+___ H+→___ Fe2++___ NH4++___ H2O
(1)写出NH4Cl电子式:
(2)氮原子的电子排布式是:
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的量在计算中有广泛的应用,请完成下列各小题:
(1)标况下6.72 L 分子中所含原子数与
分子中所含原子数与_______ g  分子中所含原子数相等。
分子中所含原子数相等。
(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为_______ ,该溶液可与足量锌反应,产生的 在标准状况下体积为
在标准状况下体积为_______ 。
(3)硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.1 mol/L,硫酸根离子的浓度为0.3 mol/L,则混合溶液中镁离子浓度为_______ 。
(4)V mL 溶液中含
溶液中含 a g,取0.5V mL溶液稀释到2V mL,则稀释后溶液中
a g,取0.5V mL溶液稀释到2V mL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是_______ mol/L。
(5)将8.3 g由铝、锌两种金属组成的混合物加入到200 g稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体27.5 g,则原稀硫酸中溶液的质量分数为_______ 。
(1)标况下6.72 L
 分子中所含原子数与
分子中所含原子数与 分子中所含原子数相等。
分子中所含原子数相等。(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为
 在标准状况下体积为
在标准状况下体积为(3)硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.1 mol/L,硫酸根离子的浓度为0.3 mol/L,则混合溶液中镁离子浓度为
(4)V mL
 溶液中含
溶液中含 a g,取0.5V mL溶液稀释到2V mL,则稀释后溶液中
a g,取0.5V mL溶液稀释到2V mL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是(5)将8.3 g由铝、锌两种金属组成的混合物加入到200 g稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体27.5 g,则原稀硫酸中溶液的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硝酸工业尾气中氮氧化物(NO 和NO2)是主要的大气污染物之一,可用氨氧混合气体进行选择性还原处理。其主要反应原理如下:4NO+4NH3+O2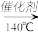 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3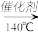 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
(1)尾气中氮氧化物的平均相对原子量为_____________ ;尾气中NO的含量为_____ mg/m3。
(2)要处理5m3的尾气,需要氨氧混合气的体积为_______ L。
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为_____________ mol/L,体积为_____ mL。
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=______
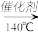 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3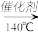 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。(1)尾气中氮氧化物的平均相对原子量为
(2)要处理5m3的尾气,需要氨氧混合气的体积为
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1) 20世纪前,黑火药是世界上唯一的火箭推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为:S+2KNO3+3C═K2S+N2↑+3CO2。
①写出N2的电子式 :___________
②已知SO2和氯水反应会生成两种强酸,其离子方程式为___________
③请设计实验检验上述含氧酸根离子:___________
(2)排放二氧化硫、氮氧化物均会危害环境,必须对它们进行处理。。处理氮氧化物的方法很多,以下列举几种常见方法。
①用过量NaOH溶液吸收NO2气体。所得溶液中除含有NaOH和NaNO2,还含有___________ 。
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。
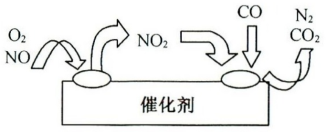
写出净化过程中的总化学反应方程式:___________
③请写出NH3与少量氯气反应的化学方程式:___________
(3)写出过氧化钠与水反应的化学方程式:___________
①写出N2的电子式 :
②已知SO2和氯水反应会生成两种强酸,其离子方程式为
③请设计实验检验上述含氧酸根离子:
(2)排放二氧化硫、氮氧化物均会危害环境,必须对它们进行处理。。处理氮氧化物的方法很多,以下列举几种常见方法。
①用过量NaOH溶液吸收NO2气体。所得溶液中除含有NaOH和NaNO2,还含有
②为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。

写出净化过程中的总化学反应方程式:
③请写出NH3与少量氯气反应的化学方程式:
(3)写出过氧化钠与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求,回答下列问题:
(1)写出离子反应方程式“Ba2+ + SO42- = BaSO4↓”对应的化学反应方程式____________ ;
(2)氧化还原反应“2Na + O2 Na2O2”,氧化产物是
Na2O2”,氧化产物是_______ ;氧化剂是_____ 。
(3)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有___ 。(填氧化性或还原性)
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入_________ 溶液,再加入______ 溶液发现有白色沉淀生成,并由此得出该混合物中含有硫酸盐的结论。
(1)写出离子反应方程式“Ba2+ + SO42- = BaSO4↓”对应的化学反应方程式
(2)氧化还原反应“2Na + O2
 Na2O2”,氧化产物是
Na2O2”,氧化产物是(3)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是_______ ;属于非电解质的是 _______ 。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物_______ ;
②从硝酸钾和氯化钠的混合液中获得硝酸钾_______ ;
③从溴水中提取溴单质_______ ;
④分离水和煤油的混合物_______ ;
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物_______ ;
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是_______ 。
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。
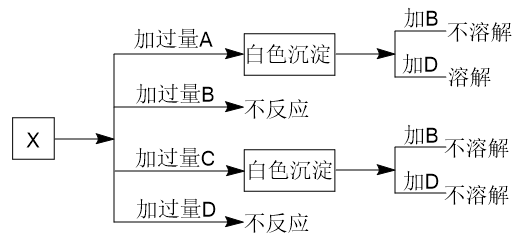
A:_______ B:_______ C:_______ D:_______ X:_______
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物
②从硝酸钾和氯化钠的混合液中获得硝酸钾
③从溴水中提取溴单质
④分离水和煤油的混合物
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。

A:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“价——类”二维图是学习元素化合物知识的好方法,依据图中氮元素及其化合物的转化关系,回答问题:
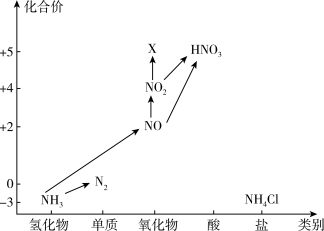
(1)图中,X的化学式为_______
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
②下列试剂能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.CaO固体 D.P2O5固体
③氮分子的电子式为_______ ,硝酸铵具有的化学键类型是_______ 。。
④工业上可采用碱液吸收和氨还原处理含NOx尾气。其中用碱液吸收的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,NO2+2NaOH=NaNO2+NaNO3+H2O。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是_______ 。
A.1molO2和4molNO2 B.1molO2和7molNO
C.1molNO和4molNO2 D.4molNO和4molNO2
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。SCR(选择性催化还原)工作原理:
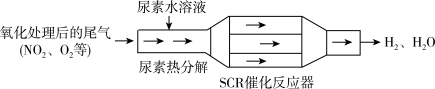
①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式:_______ 。
②尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol−1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L−1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L−1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是_______ 。

(1)图中,X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.CaO固体 D.P2O5固体
③氮分子的电子式为
④工业上可采用碱液吸收和氨还原处理含NOx尾气。其中用碱液吸收的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,NO2+2NaOH=NaNO2+NaNO3+H2O。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是
A.1molO2和4molNO2 B.1molO2和7molNO
C.1molNO和4molNO2 D.4molNO和4molNO2
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。SCR(选择性催化还原)工作原理:

①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式:
②尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol−1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L−1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L−1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚硫酸钠是工业上常用的还原剂,容易被空气氧化成硫酸钠。
完成下列填空:
(1)检验亚硫酸钠样品中是否含有硫酸钠的方法是:取少量亚硫酸钠样品溶于水,然后_________________ 。
(2)称取亚硫酸钠样品,加入过量硫酸标准溶液,煮沸,冷却,用 NaOH 标准溶液和剩余硫酸反应,可测 定样品中亚硫酸钠的含量。取亚硫酸钠样品,加入过量硫酸标准溶液后煮沸,煮沸的目的是_________________________ 。
(3)要配置 100mL0.1000mol/L 的 NaOH 溶液,需要的玻璃仪器有烧杯、玻璃棒和__________________ 。
(4)将 0.700g 亚硫酸钠样品溶解在含 0.00600mol 硫酸标准溶液中,煮沸,冷却,用 0.1000mol/LNaOH 标 准溶液与其反应,恰好反应完时消耗 NaOH 标准溶液 20.00mL。该样品中亚硫酸钠的质量分数为______________ 。
完成下列填空:
(1)检验亚硫酸钠样品中是否含有硫酸钠的方法是:取少量亚硫酸钠样品溶于水,然后
(2)称取亚硫酸钠样品,加入过量硫酸标准溶液,煮沸,冷却,用 NaOH 标准溶液和剩余硫酸反应,可测 定样品中亚硫酸钠的含量。取亚硫酸钠样品,加入过量硫酸标准溶液后煮沸,煮沸的目的是
(3)要配置 100mL0.1000mol/L 的 NaOH 溶液,需要的玻璃仪器有烧杯、玻璃棒和
(4)将 0.700g 亚硫酸钠样品溶解在含 0.00600mol 硫酸标准溶液中,煮沸,冷却,用 0.1000mol/LNaOH 标 准溶液与其反应,恰好反应完时消耗 NaOH 标准溶液 20.00mL。该样品中亚硫酸钠的质量分数为
您最近一年使用:0次
【推荐3】Ⅰ.某地环保部门取一定量某工厂所排酸性废水试样分成甲、乙、丙、丁四份,进行如图所示探究。

已知:废水试样中除H+外可能含有表中的离子:
请回答下列问题:
(1)离子X是_______ (填化学式,下同),离子Y是_______ 。
(2)表中不能确定是否存在的阴离子是_______ ,能证明该阴离子是否存在的简单实验操作为_______ 。
(3)写出废水试样中滴加淀粉KI溶液所发生反应的离子方程式:_______ 。
Ⅱ.某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜,设计的流程如图:

(4)某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下B气体6.72L(其中NO2和NO的体积比为2∶1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比_______ 。
②若测得溶液A中H+的浓度为1mol·L-1,则原硝酸的物质的量浓度为_______ 。(假设反应前后溶液的体积不变)
(5)上述制备方案中产生的气体B,既造成原料的浪费,也污染了环境。请你设计方案解决上述问题_______ 。

已知:废水试样中除H+外可能含有表中的离子:
| 阳离子 | Na+、Mg2+、X |
| 阴离子 | Cl-、SO 、Y、NO 、Y、NO |
请回答下列问题:
(1)离子X是
(2)表中不能确定是否存在的阴离子是
(3)写出废水试样中滴加淀粉KI溶液所发生反应的离子方程式:
Ⅱ.某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜,设计的流程如图:

(4)某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下B气体6.72L(其中NO2和NO的体积比为2∶1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比
②若测得溶液A中H+的浓度为1mol·L-1,则原硝酸的物质的量浓度为
(5)上述制备方案中产生的气体B,既造成原料的浪费,也污染了环境。请你设计方案解决上述问题
您最近一年使用:0次



