已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平,B和D是生活中两种常见的有机物。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
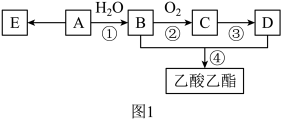
(1)物质B的名称是_______ ,反应①的反应类型是_______ ;
(2)反应④的化学方程式是_______ ;
(3)E是常见的高分子材料,E的结构简式是_______ ;
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。实验时,甲中饱和碳酸钠溶液的作用是(填字母)_______。

(5)写出分子中含有HCOO—的E的同分异构体的结构简式:_______ 。
(6)B的同系物CH3OH制作的燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH→K2CO3+H2O(未配平)。该燃料电池的负极电极反应式为_______ 。

(1)物质B的名称是
(2)反应④的化学方程式是
(3)E是常见的高分子材料,E的结构简式是
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。实验时,甲中饱和碳酸钠溶液的作用是(填字母)_______。

| A.中和乙酸和乙醇 |
| B.中和乙酸并吸收部分乙醇 |
| C.加速酯的生成,提高其产率 |
| D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出 |
(5)写出分子中含有HCOO—的E的同分异构体的结构简式:
(6)B的同系物CH3OH制作的燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH→K2CO3+H2O(未配平)。该燃料电池的负极电极反应式为
更新时间:2023-09-16 09:21:06
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】CH3OH是一种绿色燃料,工业上制备CH3OH发生如下反应:
反应1:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.5kJ/mol
CH3OH(g)+H2O(g) ΔH1=-49.5kJ/mol
反应2:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol
(1)n起始(CO2)∶n起始(H2)=1∶3的混合气体发生反应1和反应2,恒压分别为1MPa、3MPa、5MPa下反应达到平衡时CO2的转化率(α)(曲线a、b、c)以及3MPa时生成CH3OH、CO选择性(S)的变化如图所示(选择性为目标产物在总产物中的比率)。___________ 。
②250℃时,反应2的平衡常数K=___________ 。
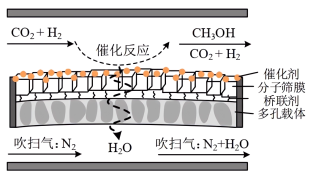
(2)恒压下,n起始(CO2)∶n起始(H2)=1∶3的混合气体以一定流速通入分子筛膜反应器(如图所示),反应相同时间,测得甲醇选择性随温度的变化如图所示。___________ 。
②温度相同时,CH3OH选择性的实验值高于平衡值,其原因可能是___________ 。
③分子筛膜反应器可提高CO2转化率的原因是___________ 。
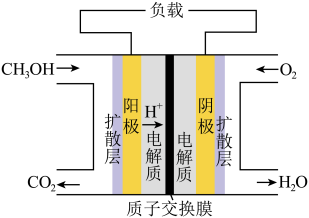
(3)某甲醇燃料电池的工作原理如图所示。负极的电极反应式为___________ 。
反应1:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.5kJ/mol
CH3OH(g)+H2O(g) ΔH1=-49.5kJ/mol反应2:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol(1)n起始(CO2)∶n起始(H2)=1∶3的混合气体发生反应1和反应2,恒压分别为1MPa、3MPa、5MPa下反应达到平衡时CO2的转化率(α)(曲线a、b、c)以及3MPa时生成CH3OH、CO选择性(S)的变化如图所示(选择性为目标产物在总产物中的比率)。
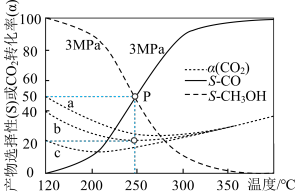
②250℃时,反应2的平衡常数K=
(2)恒压下,n起始(CO2)∶n起始(H2)=1∶3的混合气体以一定流速通入分子筛膜反应器(如图所示),反应相同时间,测得甲醇选择性随温度的变化如图所示。
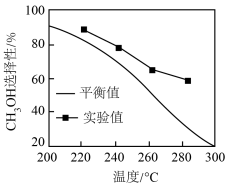
②温度相同时,CH3OH选择性的实验值高于平衡值,其原因可能是
③分子筛膜反应器可提高CO2转化率的原因是
(3)某甲醇燃料电池的工作原理如图所示。负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
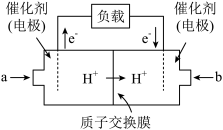
【推荐2】(1)如图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从___ (填“a”或“b”)处通入,电池内部H+向___ (填“左”或“右”)移动。写出电池负极的电极反应式:___ 。
(2)从化学键的角度分析,化学反应的过程就是反应物化学键的破坏和生成物化学键的形成过程。已知:N2(g)+3H2(g) 2NH3(g)ΔH=-93kJ·mol-1,试根据表中所列键能数据计算a的数值
2NH3(g)ΔH=-93kJ·mol-1,试根据表中所列键能数据计算a的数值___ 。
当可逆反应中净生成N—H物质的量为2mol时,反应放热___ 。
(3)工业上可用Na2SO3溶液吸收法处理废气中的SO2,25℃时用1mol·L-1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为___ 。
(已知25℃时:H2SO3的电离常数Ka1=1.3×10-2,Ka2=6.2×10-8)

(2)从化学键的角度分析,化学反应的过程就是反应物化学键的破坏和生成物化学键的形成过程。已知:N2(g)+3H2(g)
 2NH3(g)ΔH=-93kJ·mol-1,试根据表中所列键能数据计算a的数值
2NH3(g)ΔH=-93kJ·mol-1,试根据表中所列键能数据计算a的数值| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ·mol-1) | 436 | a | 945 |
当可逆反应中净生成N—H物质的量为2mol时,反应放热
(3)工业上可用Na2SO3溶液吸收法处理废气中的SO2,25℃时用1mol·L-1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为
(已知25℃时:H2SO3的电离常数Ka1=1.3×10-2,Ka2=6.2×10-8)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】CO2引起的气候变化已经引起了全世界的关注,但同时CO2也是时持续的碳资源,将CO2转化为高附加值的燃料或化学品不仅可以解决CO2的问题,还可变废为宝得到有用的化学品。CO2加氢制甲醇是实现这一过程的理想选择之一、
(1)CO2加氢制甲醇的化学方程式是:CO2(g)+3H2(g) CH3OH(l)+H2O(l) ∆H, 相关物质的燃烧热数据如下表所示:
CH3OH(l)+H2O(l) ∆H, 相关物质的燃烧热数据如下表所示:
回答下列问题:
①∆H=___________ kJ∙mol−1
②320℃时,将含CO2体积分数10%的空气与H2按体积比5:2投入到密闭容器中,同时加入催化剂发生反应(此时体系内各物质均为气态),测得初始时压强为P,反应一段时间后达到平衡,测得CO2的平衡转化率为50%,则平衡时体系的压强为___________ ,反应的平衡常数___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)Fujta等学者开展了在Cu/ZnO催化剂上进行CO2+H2合成甲醇机理的研究。机理如下:
①过程3的化学方程式为___________ ; 研究表明,过程3的活化能小但实际反应速率慢,是控速步骤,导致该步反应速率小的原因可能是___________ 。
A.H2O对该反应有阻碍作用 B. CO2的存在削弱了同一吸附位上H2的吸附
C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②ZnO也有催化作用,催化机理与Cu相似,CH3O−Zn与___________ 反应可获得CH3OH。
(3)科学家设计了一种新的CO2−H2O可循环系统,可以实现温室气体的零排放,同时也回避了H2的难储存问题,装置如下:
①系统中的能量转化形式有___________ 。
②b电极上的电极反应式为___________ ,如果将电解质溶液换为KOH溶液,对合成甲醇造成的不良后果是___________ 。
(1)CO2加氢制甲醇的化学方程式是:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ∆H, 相关物质的燃烧热数据如下表所示:
CH3OH(l)+H2O(l) ∆H, 相关物质的燃烧热数据如下表所示:| 物质 | H2(g) | CH3OH(1) |
| 燃烧热△H (kJ∙mol−1) | −284 | −726 |
①∆H=
②320℃时,将含CO2体积分数10%的空气与H2按体积比5:2投入到密闭容器中,同时加入催化剂发生反应(此时体系内各物质均为气态),测得初始时压强为P,反应一段时间后达到平衡,测得CO2的平衡转化率为50%,则平衡时体系的压强为
(2)Fujta等学者开展了在Cu/ZnO催化剂上进行CO2+H2合成甲醇机理的研究。机理如下:
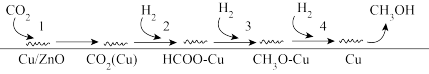
①过程3的化学方程式为
A.H2O对该反应有阻碍作用 B. CO2的存在削弱了同一吸附位上H2的吸附
C.温度变化导致活化能增大 D.温度变化导致平衡常数减小
②ZnO也有催化作用,催化机理与Cu相似,CH3O−Zn与
(3)科学家设计了一种新的CO2−H2O可循环系统,可以实现温室气体的零排放,同时也回避了H2的难储存问题,装置如下:
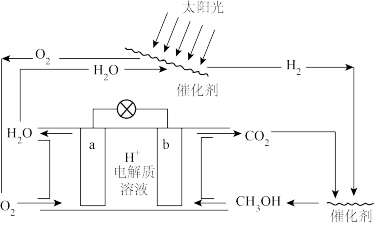
①系统中的能量转化形式有
②b电极上的电极反应式为
您最近一年使用:0次
【推荐1】乙二醇是重要的工艺原料,可由乙烯或合成气等为原料制备,部分合成方法如图所示:

回答下列问题:
(1)A的化学名称为_______ 。
(2)E中官能团的名称为_______ 。
(3)C的分子式为_______ 。
(4)反应②的化学方程式为_______ ,①反应的反应类型为_______ 。

回答下列问题:
(1)A的化学名称为
(2)E中官能团的名称为
(3)C的分子式为
(4)反应②的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐2】已知:
①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;
②2CH3CHO+O2 2CH3COOH,现以A为主要原料合成乙酸乙酯,合成路线如图所示。
2CH3COOH,现以A为主要原料合成乙酸乙酯,合成路线如图所示。
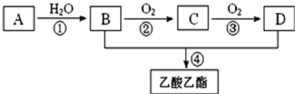
(1)A在一定条件下可以聚合生成一种常见塑料,写出该塑料结构简式___________ ;
(2)B、D分子中的官能团名称分别是___________ ;
(3)①、④的反应类型___________ ,___________ ;
(4)写出下列反应的化学方程式:②___________ ;④___________ 。
①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;
②2CH3CHO+O2
 2CH3COOH,现以A为主要原料合成乙酸乙酯,合成路线如图所示。
2CH3COOH,现以A为主要原料合成乙酸乙酯,合成路线如图所示。
(1)A在一定条件下可以聚合生成一种常见塑料,写出该塑料结构简式
(2)B、D分子中的官能团名称分别是
(3)①、④的反应类型
(4)写出下列反应的化学方程式:②
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐3】从石油和煤中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来 衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式:________ ;
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:___________ ;
(3)在碘水中加入B振荡静置后的现象:_______________ ,该操作叫______________ ;
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_________ ;
反应类型为:_________________ ;
(5)等质量的A、B完全燃烧时消耗O2的物质的量________ (填“A>B”、“A<B”或“A=B”)。
(1)A的结构简式:
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:
(3)在碘水中加入B振荡静置后的现象:
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:
反应类型为:
(5)等质量的A、B完全燃烧时消耗O2的物质的量
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】工业中很多重要的化工原料都来源于石油化工,如下图中的苯、丙烯、有机物A等,其中A能催熟水果,E、G是有水果香味的物质,H是高分子化合物。

请回答下列问题:
(1)F中含氧官能团的名称为___________ ,A的电子式为________ 。
(2)写出下列反应的反应类型:⑤__________ ⑥___________ 。
(3)在实验室里我们可以用如图所示的装置来制取E
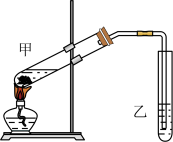
乙试管中所盛试剂的主要作用是_________ ;该装置图中有一个明显的错误是_________ 。
(4)写出下列反应方程式:
反应①___________ ;反应③____________ ;反应④___________ 。

请回答下列问题:
(1)F中含氧官能团的名称为
(2)写出下列反应的反应类型:⑤
(3)在实验室里我们可以用如图所示的装置来制取E

乙试管中所盛试剂的主要作用是
(4)写出下列反应方程式:
反应①
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐2】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
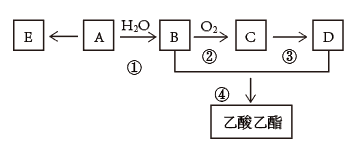
(1)A分子中官能团的名称是_______ ,D中官能团的名称是_______ ;反应①的反应类型是_______ 反应。
(2)反应②的化学方程式是_______ ,反应型:_______ ;反应④的化学方程式是_______ ,反应类型:_______ 。
(3)E是常见的高分子材料,合成E的化学方程式是_______ 。
(4)某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
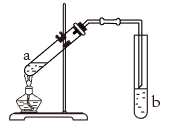
①装置中使用球形干燥管除起到冷凝作用外,另一重要作用是_______ ,b中分离乙酸乙酯必须使用的一种玻璃仪器是_______ 。
②b试管中饱和 溶液的作用是
溶液的作用是_______ (填字母)。
A.降低乙酸乙酯的溶解度
B.除去实验中挥发出来的硫酸
C.除去乙酸乙酯中混有的乙酸和乙醇

(1)A分子中官能团的名称是
(2)反应②的化学方程式是
(3)E是常见的高分子材料,合成E的化学方程式是
(4)某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。

①装置中使用球形干燥管除起到冷凝作用外,另一重要作用是
②b试管中饱和
 溶液的作用是
溶液的作用是A.降低乙酸乙酯的溶解度
B.除去实验中挥发出来的硫酸
C.除去乙酸乙酯中混有的乙酸和乙醇
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】实验室用如图所示的装置制取乙酸乙酯。
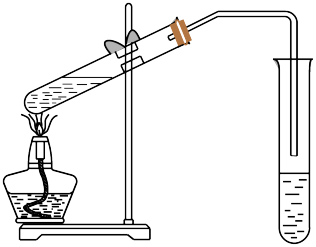
(1)制取乙酸乙酯 加入试剂的顺序为_________ , 然后轻轻振荡试管混合均匀。
(2)装置中通蒸气的导管不能插入饱和的Na2CO3溶液的液面下的原因是_________ 。
(3)浓硫酸的主要作用是:①__________ ;②__________ 。
(4)饱和Na2CO3溶液的作用是________ ,___________ ,_____________ 。
(5)反应生成的乙酸乙酯密度比水____________ 。
(6)书写CH3CO18OH与CH3CH2OH反应的化学方程式__________________________ 。

(1)制取乙酸乙酯 加入试剂的顺序为
(2)装置中通蒸气的导管不能插入饱和的Na2CO3溶液的液面下的原因是
(3)浓硫酸的主要作用是:①
(4)饱和Na2CO3溶液的作用是
(5)反应生成的乙酸乙酯密度比水
(6)书写CH3CO18OH与CH3CH2OH反应的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】根据以下转化关系,完成以下各空:
(1) B和C的结构简式:B_______ C_______ 。
(2)完成以下序号的化学方程式:
②_______ 。
③_______ 。
④_______ 。

(1) B和C的结构简式:B
(2)完成以下序号的化学方程式:
②
③
④
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐2】氟他胺是一种抗肿瘤药,它的一种合成路线如下: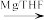 R1MgX
R1MgX
II.醛或酮可与格林试剂R1MgX反应,所得产物经水解可得醇,如_______ 。
(2)写出反应②的化学方程式是_______ 。
(3)1molD被还原成E转移的电子数为_______ 。
(4)用系统命名法命名F的名称是_______ 。
(5)写出H在铜作催化剂加热,发生氧化反应的化学方程式是_______ 。
(6)反应④类型是_______ 。
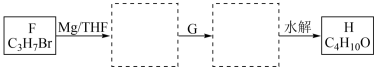
(7)请在F→H流程图的虚线框内填写物质的结构简式:__________ 。
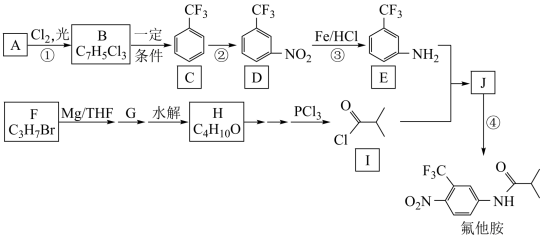
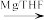 R1MgX
R1MgXII.醛或酮可与格林试剂R1MgX反应,所得产物经水解可得醇,如

III.羧酸与PCl3作用可生成酰氯,如R2COOH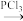

(2)写出反应②的化学方程式是
(3)1molD被还原成E转移的电子数为
(4)用系统命名法命名F的名称是
(5)写出H在铜作催化剂加热,发生氧化反应的化学方程式是
(6)反应④类型是
(7)请在F→H流程图的虚线框内填写物质的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐3】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的电子式______________ ,A的结构简式_______________ ;
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式___________ ,反应类型______________ ;
(3)在碘水中加入B振荡静置后的现象__________________________________ ;
(4)B与Br2在FeBr3催化下反应的化学反应方程式_________________________ ,反应类型___________ 。
(5)等质量的A、B完全燃烧时消耗O2的物质的量____________ (填“A>B”或“A<B”或“A=B”)。
(1)A的电子式
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式
(3)在碘水中加入B振荡静置后的现象
(4)B与Br2在FeBr3催化下反应的化学反应方程式
(5)等质量的A、B完全燃烧时消耗O2的物质的量
您最近一年使用:0次



