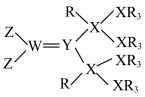
某种单体的结构如图所示。R、W、X、Y、Z为原子序数依次增大的短周期元素,W、X、Y同周期,W的最外层电子数=Y的最外层电子数﹣内层电子数,基态Y原子价层有3个成单电子,Z的最高正价等于Y的原子序数。下列说法不正确的是

A.WZ 呈正四面体 呈正四面体 |
| B.该单体中W与Y之间存在π键,π键电子对由Y提供 |
| C.氢化物沸点:Y>X |
| D.五种元素的单质中,氧化性最强的是Z的单质 |
更新时间:2023-10-10 21:24:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后中,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生,且Z与X属于同一主族。下列说法不正确的是( )
| A.X的简单氢化物的热稳定性比W的强 |
| B.Y的简单离子与X的简单离子具有相同的电子层结构 |
| C.Y分别与X、Z形成化合物中所含化学键类型一定完全相同 |
| D.原子半径:Y>Z>W>X |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
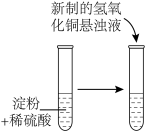
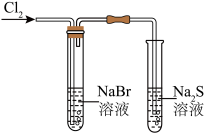
【推荐2】下列实验(部分夹持装置已略去)能达到实验目的的是
|
|
A.实验室制取 | B.检验淀粉在酸性条件下发生了水解 |
|
|
比较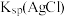 与 与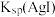 的大小 的大小 | D.比较Cl、Br、S的非金属性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
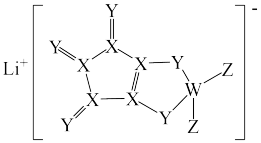
【推荐1】某离子液体结构如图所示。W、X、Y、Z原子序数依次增大,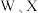 和
和 的原子序数之和为
的原子序数之和为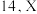 和
和 基态原子的核外未成对电子数之和为
基态原子的核外未成对电子数之和为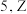 是第四周期元素。下列说法不正确的是
是第四周期元素。下列说法不正确的是
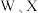 和
和 的原子序数之和为
的原子序数之和为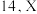 和
和 基态原子的核外未成对电子数之和为
基态原子的核外未成对电子数之和为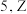 是第四周期元素。下列说法不正确的是
是第四周期元素。下列说法不正确的是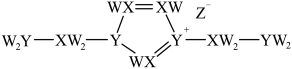
A.该物质的熔点低于 |
B.电负性: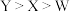 |
| C.W、Y、Z可形成既含离子键又含共价键的化合物 |
| D.已知阳离子环与苯环的结构相似,则环上的两个Y原子的杂化方式不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有X、Y、Z、M四种短周期元素,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法不正确的是( )
| A.简单阳离子的氧化性:Y>X |
| B.气态氢化物的稳定性:Z<M |
| C.简单离子半径由大到小的顺序是:Z>M>Y |
| D.等浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z<Y2Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】观察下列模型并结合有关信息,判断下列说法不正确的是( )
| HCN | S8 | SF6 | B12结构单元 | |
| 结构模型 示意图 |
|
|
|
|
| 备注 | — | 易溶于CS2 | — | 熔点1 873 K |
| A.HCN的结构式为H—C≡N,分子中含有2个σ键和2个π键 |
| B.固态硫S8属于原子晶体 |
| C.SF6是由极性键构成的非极性分子 |
| D.单质硼属原子晶体,结构单元中含有30个B—B键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】卤族元素单质及其化合物应用广泛。海洋是一个巨大的卤素资源宝库,从海水中能获得NaCl,NaCl的晶胞如下图所示。以NaCl为原料可制得Cl2、HClO、ClO2、 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。 
A.1molSO2F2分子中含有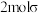 键 键 |
B.Br原子基态核外电子排布式为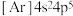 |
C. 和 和 中键角相等 中键角相等 |
D.NaCl晶胞中,每个 周围紧邻且距离相等的 周围紧邻且距离相等的 构成正八面体结构 构成正八面体结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列对应关系不正确的是
| 选项 | 代表物 | 分子类型 | 有无孤电子对 | 空间构型 |
| A | SO2 | AB2 | 无 | 直线形 |
| B | CH2O | AB3 | 无 | 平面三角形 |
| C | H2O | AB2 | 有 | V形 |
| D | NH3 | AB3 | 有 | 三角锥形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、Z、R的原子序数依次增大,Z、R位于同主族。由这四种元素组成一种光学晶体,结构如图所示。该晶体的分子中Y原子最外层达到8电子结构。下列叙述错误的是
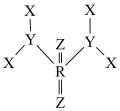

| A.电负性:Z>Y>X |
| B.第一电离能:Y>Z>R |
| C.上述晶体中Y和R的杂化类型相同 |
| D.Y、Z、R的简单氢化物VSEPR模型不相同 |
您最近一年使用:0次



 通入硝酸钡溶液中
通入硝酸钡溶液中 难溶于水
难溶于水


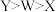



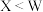
 ,下列化学用语正确的是
,下列化学用语正确的是 元素位于周期表的ds区
元素位于周期表的ds区 的
的 模型:
模型:
 核素符号:
核素符号: