回答下列问题。
(1)相同质量的 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为___________ 。
(2)已知CO、 的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为
的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为___________ ,CO的物质的量为___________ 。
(3)将 的
的 溶液由amL稀释至bmL,稀释后溶液中
溶液由amL稀释至bmL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(4)质量比为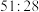 的
的 和CO,其所含的质子数之比为
和CO,其所含的质子数之比为___________ 。
(5)中和浓度为4mol/L,体积为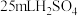 溶液,需要NaOH的质量为
溶液,需要NaOH的质量为___________ 。
(1)相同质量的
 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为(2)已知CO、
 的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为
的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为(3)将
 的
的 溶液由amL稀释至bmL,稀释后溶液中
溶液由amL稀释至bmL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(4)质量比为
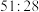 的
的 和CO,其所含的质子数之比为
和CO,其所含的质子数之比为(5)中和浓度为4mol/L,体积为
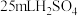 溶液,需要NaOH的质量为
溶液,需要NaOH的质量为
23-24高一上·山东泰安·阶段练习 查看更多[2]
更新时间:2023-10-24 16:54:01
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源。
(1)在汽油中加入适量乙醇作为汽油燃料,可节省___ (填化石燃料的名称)资源,减少汽车尾气的污染。
(2)乙醇在氧气中不完全燃烧会产生大量的有害气体,其反应式为4C2H5OH+XO2=2CO+6CO2+12H2O,则X的值为___ 。
(3)写出乙醇在空气中完全燃烧的化学方程式___ ,46克乙醇不完全燃烧,生成水的质量为___ 克。
(1)在汽油中加入适量乙醇作为汽油燃料,可节省
(2)乙醇在氧气中不完全燃烧会产生大量的有害气体,其反应式为4C2H5OH+XO2=2CO+6CO2+12H2O,则X的值为
(3)写出乙醇在空气中完全燃烧的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学兴趣小组取4.6g Na投入99.6g滴有无色酚酞的水中,充分反应后得到密度为1.04g·cm-3的NaOH溶液。根据所学知识,按要求回答下列问题:
(1)该过程中发生反应的化学方程式为___________ 。
(2)该过程中生成的气体在标准状况下的体积为___________ L;反应过程中转移的电子数约为___________ 。
(3)所得NaOH溶液的物质的量浓度为___________ mol·L-1;从中取出5mL后,剩余NaOH溶液中c(Na+)=___________ mol·L-1。
(4)用量筒量取___________ mL上述所得NaOH溶液,可配得100mL 0.5mol·L-1 NaOH溶液。
(1)该过程中发生反应的化学方程式为
(2)该过程中生成的气体在标准状况下的体积为
(3)所得NaOH溶液的物质的量浓度为
(4)用量筒量取
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)等质量的O2和SO2,物质的量之比为______ ,在相同条件下的体积之比为_____ 。
(2)同温同压下,相同体积的CO2和O2的质量比为__________ 。
(1)等质量的O2和SO2,物质的量之比为
(2)同温同压下,相同体积的CO2和O2的质量比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】完成下列填空
(1)若agCO2含b个原子,则阿伏加德罗常数的值为___________
(2)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为___________
(3)质量比为11∶6的CO2和NO,其物质的量之比为___________ ,它们所含质子数之比为___________ 。
(1)若agCO2含b个原子,则阿伏加德罗常数的值为
(2)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(3)质量比为11∶6的CO2和NO,其物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】将 含杂质
含杂质 的大理石(杂质与盐酸不反应)投入
的大理石(杂质与盐酸不反应)投入 盐酸中恰好完全反应,计算:(写出计算过程)
盐酸中恰好完全反应,计算:(写出计算过程)
(1)反应生成的 的体积(标准状况)
的体积(标准状况)___________
(2)原盐酸的物质的量浓度___________ 。
 含杂质
含杂质 的大理石(杂质与盐酸不反应)投入
的大理石(杂质与盐酸不反应)投入 盐酸中恰好完全反应,计算:(写出计算过程)
盐酸中恰好完全反应,计算:(写出计算过程)(1)反应生成的
 的体积(标准状况)
的体积(标准状况)(2)原盐酸的物质的量浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,“脱水除铵”过程中固体质量与温度的关系如下图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到 ScF3,由图中数据可得x:z=_______ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学用NaHCO3和KHCO3组成的混合物进行实验,三次实验所用盐酸的物质的量浓度相同,体积各为50mL,实验数据如下表。
试计算:
(1)盐酸的物质的量浓度为多少?___________
(2)混合物中的NaHCO3和KHCO3物质的量之比?___________
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2) (标准状况) | 2.24L | 3.36L | 3.36L |
试计算:
(1)盐酸的物质的量浓度为多少?
(2)混合物中的NaHCO3和KHCO3物质的量之比?
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在标准状况下,1.5molCO2的体积为___ L;2.5molO2质量为___ g;将20gNaOH的物质的量为___ mol,将其溶于水配成100mL溶液,该溶液中NaOH物质的量浓度为___ mol/L,其中Na+物质的量浓度为___ mol/L。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】用NA表示阿伏加德罗常数的值,按要求完成下列填空。
(1)0.5 molH2O中含有___________ 个水分子,含有原子___________ 个。
(2)标准状况下VmLCH4气体所含氢原子a个,则NA=___________ 。
(3)相同条件下等质量的CO和CO2气体的体积之比___________ ,密度之比___________ 。
(4)酒后驾驶危害极大,根据国家有关规定,车辆驾驶人员血液中的酒精(C2H5OH)含量达到20mg/100mL以上时,可判定为饮酒驾驶或醉酒驾驶。请参考宣传图片回答问题:

①用物质的量浓度表示酒后驾车判定标准,即饮酒驾驶:___________ 。
②在一次执法过程中,交警部门查到某位机动车驾驶员恰好达到醉酒驾车判定标准,已知成人体内血液总体积平均为5.0L,则该驾驶员体内血液中累积的酒精物质的量至少是___________ 。
(1)0.5 molH2O中含有
(2)标准状况下VmLCH4气体所含氢原子a个,则NA=
(3)相同条件下等质量的CO和CO2气体的体积之比
(4)酒后驾驶危害极大,根据国家有关规定,车辆驾驶人员血液中的酒精(C2H5OH)含量达到20mg/100mL以上时,可判定为饮酒驾驶或醉酒驾驶。请参考宣传图片回答问题:

①用物质的量浓度表示酒后驾车判定标准,即饮酒驾驶:
②在一次执法过程中,交警部门查到某位机动车驾驶员恰好达到醉酒驾车判定标准,已知成人体内血液总体积平均为5.0L,则该驾驶员体内血液中累积的酒精物质的量至少是
您最近一年使用:0次

 可发生反应:
可发生反应: ,现有
,现有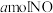 和
和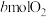 充分反应后,氮原子与氧原子的个数比为
充分反应后,氮原子与氧原子的个数比为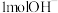 中含有电子数为
中含有电子数为 恰好完全反应,生成Fe的质量为
恰好完全反应,生成Fe的质量为

