室温条件下,将0.1mol⋅L 的NaOH溶液逐滴滴入10mL0.1mol⋅L
的NaOH溶液逐滴滴入10mL0.1mol⋅L HB溶液中。所得溶液pH随NaOH溶液体积的变化如图。
HB溶液中。所得溶液pH随NaOH溶液体积的变化如图。

下列说法正确的是
 的NaOH溶液逐滴滴入10mL0.1mol⋅L
的NaOH溶液逐滴滴入10mL0.1mol⋅L HB溶液中。所得溶液pH随NaOH溶液体积的变化如图。
HB溶液中。所得溶液pH随NaOH溶液体积的变化如图。
下列说法正确的是
A.0.1mol⋅L HB溶液中 HB溶液中 为 为 mol⋅L mol⋅L |
| B.该中和滴定可采用石蕊作为指示剂 |
C.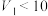 |
| D.b点时,NaOH与HB恰好完全反应 |
更新时间:2023-10-17 22:31:46
|
【知识点】 酸碱中和滴定的综合考查解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,向 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法正确的是
的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法正确的是

 溶液中逐滴加入
溶液中逐滴加入 的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法正确的是
的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法正确的是
A.a点的 | B.b点时, |
C.c点时, | D.c点时,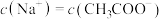 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用0.1000mol/L的NaOH溶液分别滴定20.00mL浓度为c1的 溶液和20.00mL浓度为c2的
溶液和20.00mL浓度为c2的 溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是
溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是

 溶液和20.00mL浓度为c2的
溶液和20.00mL浓度为c2的 溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是
溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点(这两点的横坐标分别为10.60mL和17.20mL)。下列说法不正确的是
A.X曲线代表 ,且c1>c2 ,且c1>c2 |
B. 溶液中, 溶液中,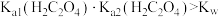 |
C.若a点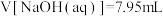 ,则a点有 ,则a点有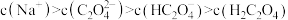 |
D.若b点时溶液中 ,则b点消耗了8.60mLNaOH溶液 ,则b点消耗了8.60mLNaOH溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,向20.00 mL的NaOH溶液中逐滴加入某浓度的CH3COOH溶液。滴定过程中,溶液的pH与滴入CH3COOH溶液的体积关系如图所示,点②时NaOH溶液恰好被中和。则下列说法中,错误的是
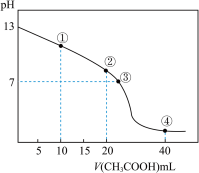

| A.CH3COOH溶液的浓度为0.1 mol·L-1 |
| B.图中点①到点③所示溶液中,水的电离程度先增大后减小 |
| C.点④所示溶液中存在:c(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-) |
| D.滴定过程中会存在:c(Na+)> c(CH3COO-)=c(OH-)> c(H+) |
您最近一年使用:0次



