为了探究化学能与热能的转化,某实验小组设计了如图所示三套实验装置:
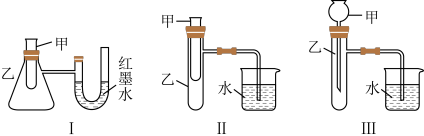
(1)上述三套装置中,不能判断铜与浓硝酸的反应是吸热反应还是放热反应的是_____ (填装置序号)。
(2)某同学选用装置Ⅰ进行实验(实验前装置Ⅰ右侧实验仪器里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀硫酸,右侧仪器中可观察到的现象是_____ ,说明该反应属于_____ (填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是_____ 。
②若观察到烧杯中产生气泡,则说明M溶于水_____ (填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”)。
③若观察到烧杯中的导管内形成一段水柱,则M可能是_____ 。
(4)至少有两种实验方法能证明超氧化钾与水的反应(
 )是放热反应还是吸热反应。
)是放热反应还是吸热反应。
方法①:选择上述装置_____ 进行实验。
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是_____ (填“吸热”或“放热”)反应。
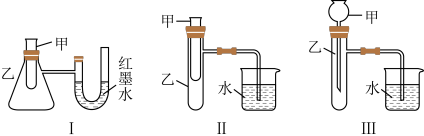
(1)上述三套装置中,不能判断铜与浓硝酸的反应是吸热反应还是放热反应的是
(2)某同学选用装置Ⅰ进行实验(实验前装置Ⅰ右侧实验仪器里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀硫酸,右侧仪器中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯中产生气泡,则说明M溶于水
③若观察到烧杯中的导管内形成一段水柱,则M可能是
(4)至少有两种实验方法能证明超氧化钾与水的反应(
 )是放热反应还是吸热反应。
)是放热反应还是吸热反应。方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是
更新时间:2023-09-24 16:09:58
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】氢气是理想的能源,可由天然气和水反应制备,其主要反应为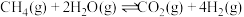 ,反应过程中能量变化如图所示:
,反应过程中能量变化如图所示:
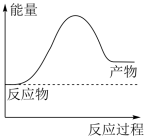
(1)该反应是_______ (填“吸热”或“放热”)反应。
(2)某温度下,在10L恒容密闭容器中充入2mol 和3mol
和3mol 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图所示,5min时反应达到平衡状态。
的物质的量变化如图所示,5min时反应达到平衡状态。
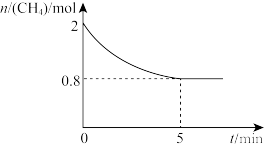
①5min前,该反应的正反应速率_______ (填“大于”、“小于”或“等于”)逆反应速率,逆反应速率不断_______ (填“增大”或“减小”)。
②下列能说明该反应已达到化学平衡状态的是_______ (填字母)。
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,4molC-H键断裂的同时有2molC=O键断裂
③0~5min内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为_______ 
④若要加快化学反应速率,可采用的方法是_______ (填“升高”或“降低”)温度。
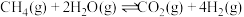 ,反应过程中能量变化如图所示:
,反应过程中能量变化如图所示:
(1)该反应是
(2)某温度下,在10L恒容密闭容器中充入2mol
 和3mol
和3mol 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图所示,5min时反应达到平衡状态。
的物质的量变化如图所示,5min时反应达到平衡状态。
①5min前,该反应的正反应速率
②下列能说明该反应已达到化学平衡状态的是
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,4molC-H键断裂的同时有2molC=O键断裂
③0~5min内,以
 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为
④若要加快化学反应速率,可采用的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知Ca(OH)2的溶解度随温度升高而降低。如下图所示,在试管中放入少许镁条,将试管浸入盛饱和石灰水的烧杯中,再向试管中滴入5mL 5mol · L-1盐酸。
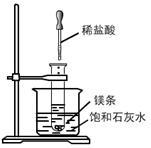
(1)实验中可观察到的现象有:
①_______________________________ ;
②_______________________________________ 。
(2)试管中发生反应的离子方程式为___________________________ 。
(3)由实验推知,镁条和盐酸的总能量______ (填“大于”、“小于”或“等于”)MgCl2溶液和H2的总能量。判断的根据是________________________ 。

(1)实验中可观察到的现象有:
①
②
(2)试管中发生反应的离子方程式为
(3)由实验推知,镁条和盐酸的总能量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I.化学反应中的能量变化通常表现为热量变化,研究热量变化具有重要的意义。
(1)下列变化属于吸热反应的是___________ (填序号)。
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦Ba(OH)2∙8H2O晶体与NH4Cl晶体的反应 ⑧灼热的木炭与CO2的反应 ⑨甲烷在空气中燃烧的反应
(2)工业合成氨反应: 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
①若1mol N2完全反应生成NH3可___________ (填“吸收”或“放出”)热量___________ kJ。
②如果将1mol N2和3mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是___________ 。
Ⅱ.甲醇(CH3OH)是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;___________ (填“正”或“负”)极,该电极反应式为:___________ 。
(4)当电路中通过1mol电子时,在电极B附近消耗O2的体积为___________ L(标准状况);电池工作一段时间后,电解质溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(1)下列变化属于吸热反应的是
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦Ba(OH)2∙8H2O晶体与NH4Cl晶体的反应 ⑧灼热的木炭与CO2的反应 ⑨甲烷在空气中燃烧的反应
(2)工业合成氨反应:
 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:①若1mol N2完全反应生成NH3可
②如果将1mol N2和3mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是
Ⅱ.甲醇(CH3OH)是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;

(4)当电路中通过1mol电子时,在电极B附近消耗O2的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】(1) 现有Na2CO3和NaHCO3两种白色固体物质:
Ⅰ.欲探究Na2CO3和NaHCO3稳定性的相对强弱,两同学分别设计了以下两组装置:
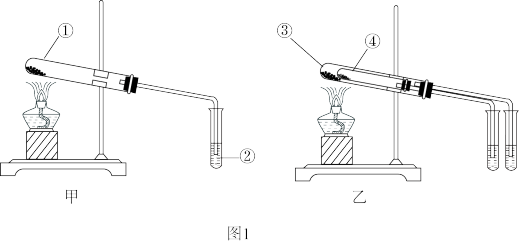
请回答:①如图1中甲图所示,分别用Na2CO3和NaHCO3做实验,试管②中的试剂是_______ (填字母序号)。
A.稀H2SO4 b.NaOH溶液 c.Ca(OH)2溶液
②如图1中乙图所示,试管④中装入的固体应该是_______ (填化学式)。
③通过上述实验,得出的结论是:Na2CO3比NaHCO3的稳定性_______ (填“强”或“弱”)
Ⅱ.等物质的量浓度的两种物质的溶液与同浓度的盐酸反应,反应速率快的是_______ (填化学式)。
(2)甲、乙、丙三位同学分别用如下三套实验装置(如图2)及化学药品(其中碱石灰为固体氢化钠和生石灰的混合物)制取氨气。请回答下列问题:
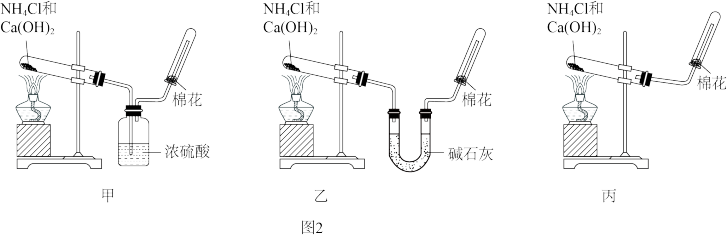
①实验室制取氨气的化学方程式为:_______ ;
②三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(假设他们的实验操作都正确),你认为没有收集到氨气的同学是_______ (填“甲”、“乙”或“丙”),收集不到氨气的主要原因是_______ (用化学方程式表示);
③检验氨气是否收集满的方法是(简述操作方法、现象和结论)_______ 。
Ⅰ.欲探究Na2CO3和NaHCO3稳定性的相对强弱,两同学分别设计了以下两组装置:

请回答:①如图1中甲图所示,分别用Na2CO3和NaHCO3做实验,试管②中的试剂是
A.稀H2SO4 b.NaOH溶液 c.Ca(OH)2溶液
②如图1中乙图所示,试管④中装入的固体应该是
③通过上述实验,得出的结论是:Na2CO3比NaHCO3的稳定性
Ⅱ.等物质的量浓度的两种物质的溶液与同浓度的盐酸反应,反应速率快的是
(2)甲、乙、丙三位同学分别用如下三套实验装置(如图2)及化学药品(其中碱石灰为固体氢化钠和生石灰的混合物)制取氨气。请回答下列问题:

①实验室制取氨气的化学方程式为:
②三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(假设他们的实验操作都正确),你认为没有收集到氨气的同学是
③检验氨气是否收集满的方法是(简述操作方法、现象和结论)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图示的装置进行试验。通入二氧化硫气体,将带余烬的木条插入试管中,木条复燃。
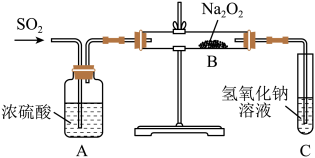
请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成的白色固体中含有Na2SO3和O2该反应的化学方程式为___ 。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3___ 。
(3)第二小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
将B中反应后的固体溶解于水(再加BaCl2溶液)→白色沉淀→(加入稀硝酸)仍有部分白色沉淀不溶解,证明有Na2SO4生成。上述方案是否合理?___ ;请简要说明理由:__ 。
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L,0.1mol/L向该混合液中加入1.92g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是__ (填选项字母)。
A.0.15 B.0.225 C.0.35 D.0.45

请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成的白色固体中含有Na2SO3和O2该反应的化学方程式为
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3
(3)第二小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
将B中反应后的固体溶解于水(再加BaCl2溶液)→白色沉淀→(加入稀硝酸)仍有部分白色沉淀不溶解,证明有Na2SO4生成。上述方案是否合理?
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L,0.1mol/L向该混合液中加入1.92g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是
A.0.15 B.0.225 C.0.35 D.0.45
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】对硝基乙酰苯胺是重要的染料中间体,实验室合成对硝基乙酰苯胺的路线如图(部分反应条件略去)。
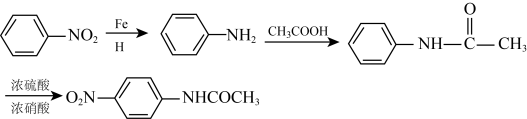
已知:①苯胺(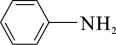 )在空气中极易被氧化;
)在空气中极易被氧化;
② (易溶于水);
(易溶于水);
③实验参数:
Ⅰ.苯胺的制备:
制取的苯胺中混有少量硝基苯杂质,可以采用如下图方案除杂提纯:
混合物 水层
水层 油相
油相 较纯净苯胺
较纯净苯胺
(1)操作1与操作2相同,该操作是___________ ,试剂Y是___________ 。
Ⅱ.乙酰苯胺的制备
反应装置如图所示,向圆底烧瓶内加入4.6mL(约0.05mol)新制备的苯胺和7.5mL(约0.13mol)冰醋酸,及少许锌粉,加热回流1h,充分反应后,趁热将反应液倒入盛有100mL冷水的烧杯中,充分冷却至室温后,减压过滤,制得乙酰苯胺。
(2)加热回流温度适合控制在___________ (填序号)。
a.100℃以下 b.100℃~105℃ c.120℃~180℃ d.305℃~310℃
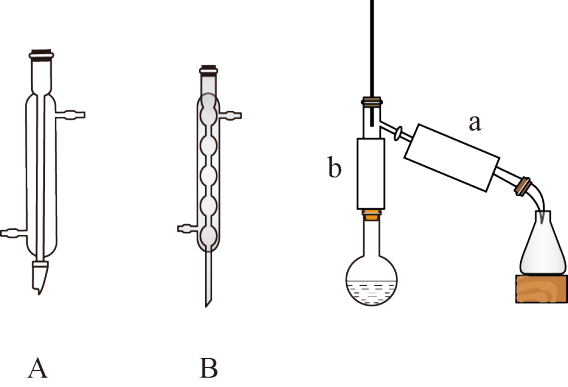
(3)以下A、B两种实验仪器,装置a处所使用的仪器名称为___________ 。
(4)乙酰苯胺中所含官能团的名称为___________ 。
(5)步骤2中加入少量锌粉的作用是___________ 。
Ⅲ.对硝基乙酰苯胺的制备
将步骤Ⅱ新制备的乙酰苯胺加入三颈烧瓶内,并加入冰醋酸溶解,然后加入浓硫酸和浓硝酸的混酸,在冰水浴中保持反应温度不超过5℃,一段时间后经减压过滤、洗涤、干燥等操作,得粗品,纯化后得对硝基乙酰苯胺7.5g。
(6)洗涤晶体宜采用___________ (填序号)。
a.热水洗 b.冷水洗 c.乙醇洗 d.先冷水再乙醇洗
(7)所得产品的核磁共振氢谱有___________ 组峰,本实验的产率是___________ %(保留3位有效数字)。

已知:①苯胺(
 )在空气中极易被氧化;
)在空气中极易被氧化;②
 (易溶于水);
(易溶于水);③实验参数:
| 化合物名称 | 相对分子质量 | 性状 | 熔点/℃ | 沸点/℃ | 溶解度 |
| 冰醋酸 | 60 | 无色透明液体 | 16.6 | 117.9 | 易溶于水,乙醇和乙醚 |
| 苯胺 | 93 | 棕黄色油状液体 | 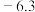 | 184 | 微溶于水,易溶于乙醇和乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 114.3 | 304 | 溶于沸水,微溶于冷水,溶于乙醇和乙醚等有机溶剂 |
| 对硝基乙酰苯胺 | 180 | 白色晶体 | 215.6 | 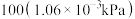 | 溶于热水,几乎不溶于冷水,溶于乙醇和乙醚 |
制取的苯胺中混有少量硝基苯杂质,可以采用如下图方案除杂提纯:
混合物
 水层
水层 油相
油相 较纯净苯胺
较纯净苯胺(1)操作1与操作2相同,该操作是
Ⅱ.乙酰苯胺的制备
反应装置如图所示,向圆底烧瓶内加入4.6mL(约0.05mol)新制备的苯胺和7.5mL(约0.13mol)冰醋酸,及少许锌粉,加热回流1h,充分反应后,趁热将反应液倒入盛有100mL冷水的烧杯中,充分冷却至室温后,减压过滤,制得乙酰苯胺。
(2)加热回流温度适合控制在
a.100℃以下 b.100℃~105℃ c.120℃~180℃ d.305℃~310℃
(3)以下A、B两种实验仪器,装置a处所使用的仪器名称为

(4)乙酰苯胺中所含官能团的名称为
(5)步骤2中加入少量锌粉的作用是
Ⅲ.对硝基乙酰苯胺的制备
将步骤Ⅱ新制备的乙酰苯胺加入三颈烧瓶内,并加入冰醋酸溶解,然后加入浓硫酸和浓硝酸的混酸,在冰水浴中保持反应温度不超过5℃,一段时间后经减压过滤、洗涤、干燥等操作,得粗品,纯化后得对硝基乙酰苯胺7.5g。
(6)洗涤晶体宜采用
a.热水洗 b.冷水洗 c.乙醇洗 d.先冷水再乙醇洗
(7)所得产品的核磁共振氢谱有
您最近一年使用:0次



