实验小组研究 与
与 的反应,装置、步骤和现象如下:
的反应,装置、步骤和现象如下:
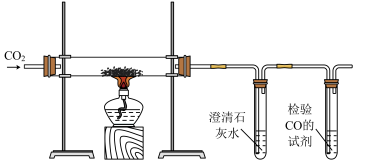
实验步骤和现象:
i.先向硬质玻璃管中加一定量钠,再迅速通入 至澄清石灰水浑浊,然后点燃酒精灯。
至澄清石灰水浑浊,然后点燃酒精灯。
ii.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验 的试剂未见明显变化。
的试剂未见明显变化。
iii.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量 溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
iv.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
 与
与 的反应,装置、步骤和现象如下:
的反应,装置、步骤和现象如下:
实验步骤和现象:
i.先向硬质玻璃管中加一定量钠,再迅速通入
 至澄清石灰水浑浊,然后点燃酒精灯。
至澄清石灰水浑浊,然后点燃酒精灯。ii.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验
 的试剂未见明显变化。
的试剂未见明显变化。iii.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量
 溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。iv.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
A.实验证明 与 与 的反应的氧化产物为 的反应的氧化产物为 ,还原产物为C ,还原产物为C |
B.步骤iii证明 与 与 也可以发生类似于 也可以发生类似于 与 与 的反应 的反应 |
C.步骤iv发生反应的化学方程式为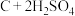 (浓) (浓)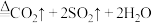 |
D.根据以上实验推测: 与金属K也可以发生反应并被还原 与金属K也可以发生反应并被还原 |
更新时间:2023-11-03 18:28:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列“类比”结果正确的是
| A.实验室用浓硫酸和NaCl固体共热制备HCl,则可用浓硫酸和NaBr固体共热制备HBr |
| B.适量CO2通入Ca(ClO)2溶液中可生成CaCO3和HClO,则适量SO2通入Ca(ClO)2溶液中也可生成CaSO3和HClO |
| C.NH3与HCl反应生成NH4Cl,则H2N—NH2也可以与HCl反应生成N2H6Cl2 |
| D.Fe3Cl8可以改写为FeCl2·2FeCl3;推出Fe3I8可以改写为FeI2·2FeI3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关物质“量”的说法正确的是
| A.相同物质的量的Al和A1(OH)3 分别与等浓度的NaOH溶液反应,至体系中均无固体时,Al(OH)3消耗的碱量较多 |
| B.由Na2CO3和NaHCO3组成的混合物中,若n(Na+):n(C)=7:5,则n(Na2CO3): n(NaHCO3)=2:3 |
| C.反应N2O4+N2H4→N2+H2O中,若有1 mol N2O4参加反应,则有4 mol电子发生转移 |
| D.相同物质的量的浓硫酸分别与足量的铜和氧化铜反应,生成硫酸铜的量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作完全正确的是
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 实验室制备氢氧化铝 | 向盛有硫酸铝溶液的试管中逐滴滴加氢氧化钠至过量 |
| C | 检验溶液中的Fe3+ | 向溶液中滴加几滴硫氰化钾溶液 |
| D | 实验室制备氢氧化亚铁沉淀 | 向盛有硫酸亚铁溶液的试管中逐滴加入氢氧化钠溶液,并边滴加边振荡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式正确的是
A.石灰乳与 溶液混合: 溶液混合: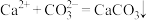 |
B.向 中加入少量 中加入少量 溶液: 溶液: |
C.氯气通入冷的氢氧化钠溶液中: |
D.钠与水的反应: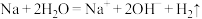 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】化学是一门以实验为基础的学科。下列实验操作能达到目的的是
| 选项 | 目的 | 实验操作 |
| A | 测新制氯水的 | 取一小块试纸在玻璃片上,用洁净且干燥的玻璃棒蘸取待测液涂在试纸的中部,观察颜色并与标准比色卡对比 |
| B | 验证氧化性: | 向 溶液中加入 溶液中加入 溶液后滴加几滴淀粉溶液,溶液变为蓝色 溶液后滴加几滴淀粉溶液,溶液变为蓝色 |
| C | 验证还原性: | 将少量金属钠加入 溶液中,反应产生红色固体 溶液中,反应产生红色固体 |
| D | 证明溶液中一定含有 | 向某无色溶液中加入过量 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于下列各实验装置的叙述中,不正确 的是
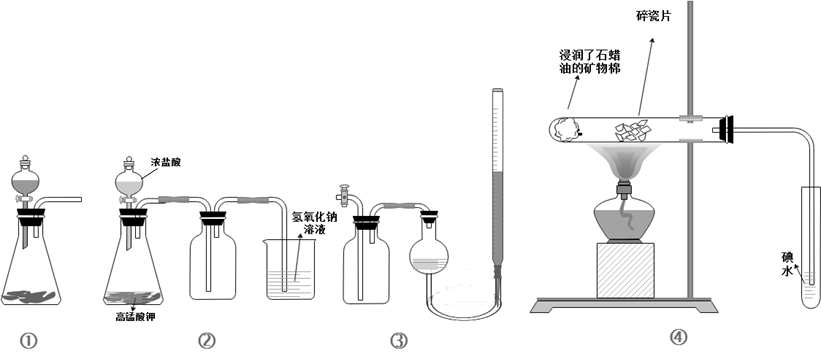

| A.装置①可用于实验室制取少量NH3或O2 |
| B.装置②可用于实验室制备Cl2 |
| C.装里③可用从右侧管处加水的方法检验气密性 |
| D.装置④中若溴水褪色则证明石蜡油分解产生乙烯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】含酚酞的氢氧化钠溶液中慢慢滴加氯水,滴到一定量时,红色突然褪去。某同学为探究该实验现象产生的原因,进行了如下操作,不正确的是
| A.预测原因:氯水中的酸与氢氧化钠溶液发生中和反应,将氢氧化钠消耗完所致 |
| B.实验设计:往褪色后的溶液中继续滴加氢氧化钠溶液,观察溶液是否重新变红 |
| C.解释现象:褪色后的溶液滴加氢氧化钠后不变红,说明不是中和反应所致 |
| D.反思评价:溶液褪色的原因可能是氯水中的氯分子具有漂白性和强氧化性 |
您最近一年使用:0次

 和物质A的反应,实验如下。
和物质A的反应,实验如下。
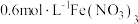 溶液(调
溶液(调 )
)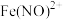 ]
]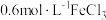 溶液
溶液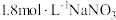 溶液(调
溶液(调 )
)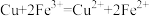
 的原因:
的原因: 还原为
还原为 固体,推测铜粉会溶解
固体,推测铜粉会溶解

