结合下列电化学装置回答问题:
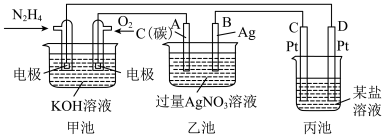
(1)图中甲池是___________ 装置(填“电解池”或“原电池”),其中 移向通
移向通___________ 的一极(填“ ”或“
”或“ ”)。
”)。
(2)写出通入 的电极的电极反应式:
的电极的电极反应式:___________ 。
(3)乙池中总反应的离子方程式为___________ 。
(4)当乙池中B(Ag)极的质量增加5.40g时,丙池也有金属析出,则丙中的某盐溶液可能是___________ (填选项),此时丙池某电极析出___________ g金属。
A. B.
B. C.NaCl D.
C.NaCl D.

(1)图中甲池是
 移向通
移向通 ”或“
”或“ ”)。
”)。(2)写出通入
 的电极的电极反应式:
的电极的电极反应式:(3)乙池中总反应的离子方程式为
(4)当乙池中B(Ag)极的质量增加5.40g时,丙池也有金属析出,则丙中的某盐溶液可能是
A.
 B.
B. C.NaCl D.
C.NaCl D.
更新时间:2023-11-14 19:26:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图装置闭合电键时,电流表A的指针将发生偏转。试回答下列问题。

(1)A池是________ ,Zn的电极名称是________ ;B池是________ ,Pt的电极名称是________ 。
(2)写出下列有关反应:
Zn极上电极反应:___________________________________________ ;
Pt极上电极反应:___________________________________________ 。
(3)B池中的总反应的化学方程式为_________________________________ 。
(4)如果要用B池给铁片上镀上一层Cu,则B池应作何改进___________________________ 。

(1)A池是
(2)写出下列有关反应:
Zn极上电极反应:
Pt极上电极反应:
(3)B池中的总反应的化学方程式为
(4)如果要用B池给铁片上镀上一层Cu,则B池应作何改进
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二甲醚(CH3OCH3)被称为 21 世纪的新型燃料,它清洁、高效、具有优良的环保性能,二甲醚是种无色气体,具有轻微的醚香味,二甲醚可作燃料电池的燃料。
(1)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:___________ 。
(2)用(1)中的燃料电池为电源,以石墨为电极电解500mLNaCl溶液,装置如图甲所示。

①请写出电解过程中总反应的离子方程式___________ 。
②当燃料电池消耗 2.8 LO2 (标准状况下)时,计算此时:NaCl 溶液中c(OH-)=___________ mol/L (假设溶液的体积不变,气体全部从溶液中逸出)。
③短暂电解之后,要使溶液恢复原状,应该向溶液中加入物质___________ (填名称)。
(3)用(1)中的燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图乙所示。
①上述装置中 D电极应连接二甲醚燃料电池的___________ (填“正极”或“负极”),该电解池中离子交换膜为___________ 离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为___________ 。
(1)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:
(2)用(1)中的燃料电池为电源,以石墨为电极电解500mLNaCl溶液,装置如图甲所示。

①请写出电解过程中总反应的离子方程式
②当燃料电池消耗 2.8 LO2 (标准状况下)时,计算此时:NaCl 溶液中c(OH-)=
③短暂电解之后,要使溶液恢复原状,应该向溶液中加入物质
(3)用(1)中的燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图乙所示。
①上述装置中 D电极应连接二甲醚燃料电池的
②该电解池的阳极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学电化学知识,回答有关问题。

(1)图中甲池是____ (填“原电池”或“电解池”)装置,其中OH-移向___ (填“正”或“负”)极。
(2)通入CH3OH一端的电极反应式为_____________________ 。
(3)反应一段时间后,甲池中消耗560mL(标准状况)O2,此时乙池溶液的pH=______ (设此时乙池中溶液的体积为100mL)。
(4)当乙池中Ag电极的质量增加5.4g时,丙池中某电极析出1.6g某金属,则丙池中的某盐可能是__________ (填字母)。
A.MgSO4 B.CuCl2 C.NaCl D.AgNO3

(1)图中甲池是
(2)通入CH3OH一端的电极反应式为
(3)反应一段时间后,甲池中消耗560mL(标准状况)O2,此时乙池溶液的pH=
(4)当乙池中Ag电极的质量增加5.4g时,丙池中某电极析出1.6g某金属,则丙池中的某盐可能是
A.MgSO4 B.CuCl2 C.NaCl D.AgNO3
您最近一年使用:0次
【推荐1】已知下列两个反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅰ的化学平衡常数 与温度的关系如下表所示:
与温度的关系如下表所示:
请回答下列问题:
(1)若反应Ⅱ的化学平衡常数为 ,则
,则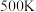 时,
时,
___________ 。
(2)反应Ⅰ的
___________ (填“>”、“<”或“=”)0,依据是:___________ 。
(3)温度为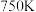 时,向某恒容密闭容器中通入一定量的
时,向某恒容密闭容器中通入一定量的 和
和 进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
(4)工业上利用电解饱和食盐水制取 和
和 ,其化学方程式为:
,其化学方程式为:___________ ,电解结束后溶液
___________ (填“减小”、“不变”或“增大”)。
反应Ⅰ:

反应Ⅱ:

反应Ⅰ的化学平衡常数
 与温度的关系如下表所示:
与温度的关系如下表所示: | 500 | 750 | 1000 | 1300 |
 | 0.5 | 0.64 | 1 | 1.5 |
(1)若反应Ⅱ的化学平衡常数为
 ,则
,则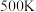 时,
时,
(2)反应Ⅰ的

(3)温度为
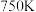 时,向某恒容密闭容器中通入一定量的
时,向某恒容密闭容器中通入一定量的 和
和 进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。| A.容器中的压强不再改变 |
| B.混合气体的密度不再改变 |
C.每断裂 键,同时断裂 键,同时断裂 键 键 |
D. |
 和
和 ,其化学方程式为:
,其化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在150mL 0.2mol/L 硫酸铜溶液中插入两个电极,通电电解(不考虑水蒸发)。
(1)若两极均为铜片,试说明电解过程中浓度将怎样变化_______________ 。
(2)若阳极为纯锌,阴极为铜片,阳极反应式是_______________ 。
(3)如不考虑氢离子在阴极上放电,当电路中有0.04mol e-通过时,阴极增重___ g,阴极上的电极反应式是_________________ 。
(1)若两极均为铜片,试说明电解过程中浓度将怎样变化
(2)若阳极为纯锌,阴极为铜片,阳极反应式是
(3)如不考虑氢离子在阴极上放电,当电路中有0.04mol e-通过时,阴极增重
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据铜锌原电池示意图,回答下列问题:

(1)锌为___________ 极,电极反应式为___________ ;铜为___________ 极,电极反应为___________ ,原电池总离子反应式是___________ 。
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量___________ (填“增加”、“不变”或“减少”);电子从电池的锌极沿导线流向电解池的___________ (填“阴极”或“阳极”,下同);在电解池中Cu2+向___________ 移动,在该电极上析出铜的质量为________ g。

(1)锌为
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学在化学工业中有着广泛应用。
(1)根据图示电化学装置,回答下列问题:
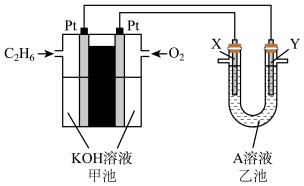
①甲池通入乙烷(C2H6)一极的电极反应式为____ 。
②乙池中,若X、Y都是石墨,A是Na2SO4溶液,实验开始时,同时在两极附近溶液中各滴入几滴紫色石蕊溶液,Y极的电极反应式为____ ;一段时间后,在Y极附近观察到的现象是_____ 。
③乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为0.2L,则Y极的电极反应式_____ ;电解一段时间后,甲池消耗11.2mLO2(标准状况下),则乙池溶液的pH为____ (忽略溶液体积的变化)。
(2)若要用该装置在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:
①Y极的材料是____ ,电极反应式为____ 。
②X极的材料是____ ,电极反应式为____ 。
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阴极反应式为_____ ,阳极的电极反应式为____ 。

(1)根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为
②乙池中,若X、Y都是石墨,A是Na2SO4溶液,实验开始时,同时在两极附近溶液中各滴入几滴紫色石蕊溶液,Y极的电极反应式为
③乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为0.2L,则Y极的电极反应式
(2)若要用该装置在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:
①Y极的材料是
②X极的材料是
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阴极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)装置如图,打开K2,闭合K1。A极可观察到的现象是___ ;B极的电极反应为___ ,打开K1,闭合K2,A极可观察到的现象是_____ ;B极的电极反应为______ 。

(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为_____ ,电解反应的离子方程式为_____ , 实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积_____ L。


(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。

根据要求回答相关问题:
(1)通入甲烷的电极为_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
(2)石墨电极为_______ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液_______ (填“铁极”或“石墨极”)区的溶液先变红。电解的总化学反应方程式为_______ 。
(3)如图丙所示用惰性电极电解 溶液,
溶液, 电极上的电极反应式为
电极上的电极反应式为_______ ,若 电极产生
电极产生 (标准状况)气体,则所得溶液的
(标准状况)气体,则所得溶液的
_______  (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入
(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入_______ (填字母)。
a. b.
b. c.
c. d.
d.
某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
 为阳离子交换膜。
为阳离子交换膜。
根据要求回答相关问题:
(1)通入甲烷的电极为
(2)石墨电极为
(3)如图丙所示用惰性电极电解
 溶液,
溶液, 电极上的电极反应式为
电极上的电极反应式为 电极产生
电极产生 (标准状况)气体,则所得溶液的
(标准状况)气体,则所得溶液的
 (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入
(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
I.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:1、4:1时,NO脱除率随温度变化的曲线如图所示。
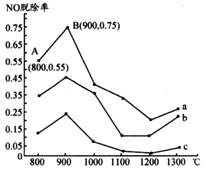
(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A 点到B点经过0.8 s,该时间段内NO的脱除速率为____________ mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是____ ,其理由是___________________
(2)已知在25℃,101 kPa时:
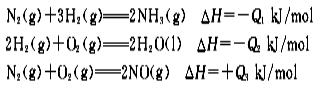
请写出用NH3脱除NO的热化学方程式:____________________________________
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下图:
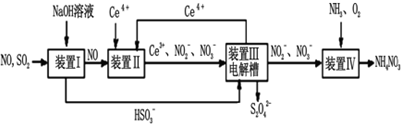
(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为__________________________________
(4)装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1 mol CH4 时,理论上可再生____ mol Ce4+。
I.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:1、4:1时,NO脱除率随温度变化的曲线如图所示。

(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A 点到B点经过0.8 s,该时间段内NO的脱除速率为
②曲线b对应的NH3与NO的物质的量之比是
(2)已知在25℃,101 kPa时:
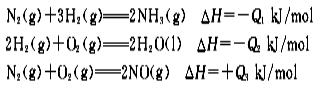
请写出用NH3脱除NO的热化学方程式:
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下图:

(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为
(4)装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1 mol CH4 时,理论上可再生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知装置E为电解池,认真观察下列装置,回答下列问题:
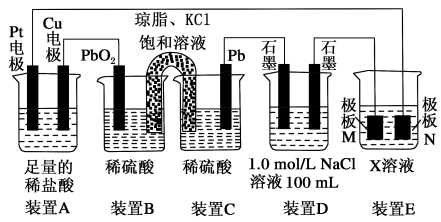
(1)装置D为___ (填“原电池”“电解池”或“电镀池”),装置C中Pb上发生的电极反应方程式为___ 。
(2)装置A中Pt电极的名称为___ (填“正极”“负极”“阴极”或“阳极”),装置A总反应的离子方程式为___ 。
(3)若装置E中的目的是在Cu材料上镀银,则X为___ ,极板N的材料为___ 。
(4)当装置B中PbO2电极质量改变12.8g时,装置D中产生气体的总物质的量为___ 。

(1)装置D为
(2)装置A中Pt电极的名称为
(3)若装置E中的目的是在Cu材料上镀银,则X为
(4)当装置B中PbO2电极质量改变12.8g时,装置D中产生气体的总物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲是燃料电池,通入甲烷的电极作___________ 极(填入“正”或“负”),其电极反应式为___________ 。
(2)乙是___________ 池(填“原电池”或“电解池”),乙装置发生电解的总反应离子方程式为:___________ 。
(3)丙中粗铜作___________ 极(填入“阴”或“阳”),若在标准状况下,有2.24L氧气参加反应,丙装置中析出精铜的质量为___________ g。
(4)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应化学方程式为___________ 。
Ⅱ.工业处理的酸性工业废水常用以下方法:
(5)将含 的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:
的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:___________ ;在酸性环境中,加入适量的NaCl进行电解, 转变为
转变为 的离子方程式为
的离子方程式为___________ 。

(1)甲是燃料电池,通入甲烷的电极作
(2)乙是
(3)丙中粗铜作
(4)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应化学方程式为
Ⅱ.工业处理的酸性工业废水常用以下方法:
(5)将含
 的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:
的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为: 转变为
转变为 的离子方程式为
的离子方程式为
您最近一年使用:0次



